Manejo de la inestabilidad glenohumeral anterior sin lesión ósea glenoidea significativa
Management of anterior glenohumeral instability without significant glenoid bone damage
Resumen:
La inestabilidad glenohumeral es una entidad clínica relevante que cuenta con una alta incidencia y prevalencia. El objetivo de este trabajo es realizar una revisión de los principales aspectos del manejo de las inestabilidades glenohumerales traumáticas anteriores, con afectación exclusiva de partes blandas.
La anamnesis es de gran importancia; ante un primer episodio de luxación debe ir encaminada a investigar características de la luxación y si existen factores de riesgo de recidiva. La anamnesis ante la sospecha de inestabilidad tiene por objetivo ayudar a confirmar el diagnóstico y a establecer su gravedad.
La exploración física junto con las pruebas diagnósticas permiten confirmar el diagnóstico y descartar lesiones asociadas.
El tratamiento tras un primer episodio de luxación glenohumeral es conservador. Se debe considerar el tratamiento quirúrgico tras un primer episodio en aquellos casos que asocien factores de riesgo de recidiva.
El tratamiento de la inestabilidad glenohumeral recurrente es quirúrgico. El tratamiento quirúrgico básicamente se resume en técnicas de partes blandas o técnicas con aporte óseo. La decisión entre realizar unas u otras depende de la magnitud del defecto óseo, por lo que es importante definir ese límite. Clásicamente, se consideraba que un defecto glenoideo del 25% junto con los conceptos de on-track y off-track de las lesiones de Hill Sachs definen los límites para el uso de una técnica de partes blandas o de aporte óseo. Pero en la actualidad se está considerando bajar el límite de defecto óseo glenoideo; cada vez hay más autores que aceptan considerar un defecto de un 20% o incluso un 15% si asocia otros factores de riesgo de recidiva.
En nuestro trabajo describiremos las técnicas quirúrgicas de partes blandas más frecuentes para el tratamiento de inestabilidades sin lesiones óseas relevantes, es decir, que se encuentren por debajo de los límites previamente descritos.
Abstract:
Glenohumeral instability is a clinically relevant condition with a high incidence and prevalence. The present review examines the main management aspects referred to traumatic anterior glenohumeral instability with exclusive soft tissue involvement.
The case history is of great importance; in the event of a first dislocation episode, we should explore the characteristics of the lesion and the presence of risk factors for relapse. When instability is suspected, the case history seeks to help confirm the diagnosis and establish the degree of severity of the condition.
The physical examination and diagnostic tests allow us to confirm the diagnosis and discard associated lesions.
Conservative management is indicated following a first episode of glenohumeral dislocation. Surgical treatment should be considered following a first episode in those cases presenting risk factors for relapse.
Surgery is indicated in patients with recurrent glenohumeral instability. Surgical treatment is basically divided into soft tissue techniques or bone grafting techniques. The decision to use one surgical approach or the other depends on the magnitude of the bone defect; it is therefore important to define this limit. Classically, a glenoid defect of 25% together with the on-track and off-track concepts of Hill Sachs lesions were considered to define the limits for the use of a soft tissue technique or bone grafting technique. Lowering of the limit of the glenoid bone defect is currently being considered, however, an increasing number of authors accept a defect of 20% or even 15% if associated to other risk factors for relapse.
The present study describes the most frequent soft tissue surgical techniques for treating instabilities without relevant bone lesions, i.e., those below the previously described limits.
Introducción
La inestabilidad glenohumeral se define como la incapacidad sintomática de mantener la cabeza humeral centrada en la fosa glenoidea. Puede dar lugar a dolor, impotencia funcional y/o ansiedad subjetiva(1).
El término inestabilidad engloba un amplio espectro de situaciones patológicas: desde casos que presenten solamente aprensión (temor a que el hombro se luxe o se subluxe en determinadas posiciones) o episodios de subluxaciones (pérdida parcial de la congruencia articular, sintomática y que reduce espontáneamente) a pacientes que han sufrido 2 o más episodios de luxación glenohumeral franca (pérdida completa de la congruencia articular que precisa reducción manual)(1). Además, es importante tener en cuenta que algunas inestabilidades se manifiestan simplemente con dolor, sensación de incomodidad y/o fallos articulares que impiden al paciente realizar su actividad deportiva o su trabajo. Este tipo de inestabilidades menos expresivas clínicamente son las que pueden pasar desapercibidas. En ellas pueden encontrarse signos indirectos o lesiones debidas a la propia inestabilidad que no se deben confundir con un proceso patológico primario, tales como lesiones tendinosas de espesor parcial de tipo PASTA (partial articular-side supraspinatus avulsion), lesiones condrales, impingement, compromiso posterointerno del manguito rotador, etc.
Se trata de una entidad clínica relevante con una elevada incidencia, de aproximadamente 23,9/100.000 personas al año(2), que afecta principalmente a personas jóvenes y activas.
Las causas de inestabilidad son múltiples, desde causas congénitas –de tipo displasia glenoidea, hiperlaxitud ligamentosa en trastornos sistémicos como Ehlers-Danlos, etc.– hasta causas adquiridas, que pueden ser traumáticas, con lesión de los elementos estabilizadores, o atraumáticas, con descompensación atraumática progresiva de los mecanismos estabilizadores(3).
El objetivo de este trabajo es realizar una revisión sobre los principales aspectos del manejo de las inestabilidades glenohumerales traumáticas anteriores, con afectación anatomopatológica exclusiva de las partes blandas, es decir, aquellas que cursan sin una pérdida ósea glenoidea relevante asociada. Se focalizará en los aspectos clínicos y radiológicos principales, destacando aquellos más importantes a tener en cuenta, para decidir el tratamiento más adecuado en cada caso.
Anamnesis
La anamnesis es fundamental para realizar el diagnóstico y estimar la gravedad de la inestabilidad. Además, nos permite identificar posibles factores de riesgo de recidiva tras un primer episodio de luxación y factores de mal pronóstico tras el tratamiento de una inestabilidad recurrente.
Hay que distinguir entre la anamnesis que realizamos tras un primer episodio de luxación y la anamnesis en casos de sospecha de inestabilidad.
Anamnesis tras un primer episodio de luxación glenohumeral
Tras un primer episodio de luxación glenohumeral, la anamnesis debe ir dirigida a recopilar datos que nos permitan identificar factores de riesgo de recidiva y el tipo de luxación sufrida, tales como:
- Edad.
- Sexo masculino o femenino.
- Dominancia (si es brazo dominante o no el afectado).
- Tipo de actividades físicas y deportes que practica. Si son de contacto como el rugby, si lo practica a nivel profesional o como aficionado, si realiza movimientos por encima de la cabeza como ocurre con el voleibol o el waterpolo, etc.
- Mecanismo lesional: traumático o no traumático.
- Intensidad del mecanismo lesional.
- Dirección de la luxación.
- Facilidad o dificultad para la reducción de dicho primer episodio de luxación.
- Lesiones asociadas tras la luxación, como pueden ser la frialdad distal en la mano, la alteración sensitiva temporal o permanente de la extremidad, etc.
- Antecedentes de inestabilidad y/o hiperlaxitud de otras articulaciones.
- Antecedentes patológicos relacionados, como son las enfermedades congénitas, sistémicas o cirugías previas.
Es importante destacar algunos de estos factores de riesgo. En un metaanálisis realizado en 2015 sobre los factores de riesgo que más predisponen a la recurrencia tras un primer episodio de luxación glenohumeral, se concluyó que la tasa real de recurrencia después de un primer episodio se estima en un 39% y que los factores de riesgo más importantes son la edad, el sexo, el mecanismo de lesión, la práctica de deportes de contacto u otros, la presencia de lesión ósea glenoidea, la hiperlaxitud y la afectación del plexo axilar(4).
La edad temprana en el momento del primer episodio es uno de los factores de riesgo de recidiva más importantes; la principal hipótesis es que en jóvenes predomina la elasticidad del tejido conectivo de tendones y ligamentos, debido a su específica composición de las fibras colágenas, y estas propiedades se van modificando con la edad(5). Varios autores han constatado que, si el primer episodio de luxación se produce por debajo de los 20 años de edad, la tasa de recurrencia puede ser de hasta un 90%, siendo más frecuente en los primeros 2 años tras la luxación(6). Sin embargo, en mayores de 40 años, la tasa de recurrencia disminuye a un 10-15%(7). Hovelius et al. publicaron un estudio prospectivo en el que mostraban una tasa de recidiva algo menor para cada grupo de edad: menores de 20 años, un 33% de recidiva; edad entre 20 y 30 años, recidiva del 25%; y edad entre 30 y 40 años, un 10% de recidivas, la mayoría en los 2 primeros años(8).
También está considerada como uno de los factores de riesgo más relevantes la presencia de lesiones óseas(9). Estas lesiones están presentes en un porcentaje considerable de casos tras tan solo un único episodio de luxación y afectan directamente a la tasa de recurrencia. Un estudio de Grifith et al. encontró presencia de lesión ósea glenoidea anterior en un 40% de los casos tras un primer episodio de luxación a los que se estudió con tomografía axial computarizada (TAC) y en un 86% de las recurrencias, siendo esta proporcional a la magnitud de la lesión(10). Dickens et al. también encontraron dicha asociación, pero en una tasa menor, un 6,8% de lesión ósea en la glena tras un primer episodio de luxación anterior y una pérdida total ósea de un 22,8% en las recurrencias(11).
Cabe destacar, por último, que los factores de riesgo tienen efecto aditivo sinérgico: si se suman 2 factores de riesgo relevantes como la lesión ósea glenoidea y la edad joven, la tasa de recidiva asciende aún más (72%)(12).
Anamnesis en la sospecha de inestabilidad glenohumeral
La anamnesis ante un paciente con sospecha de inestabilidad glenohumeral tendrá por objetivo ayudar a establecer el diagnóstico adecuado de inestabilidad y definir la gravedad de la misma.
Para el correcto diagnóstico, se debe tener claro cuál es su principal síntoma: luxación, subluxación, dolor, pérdida de rendimiento deportivo, etc. También averiguar en qué posición del brazo aparecen los síntomas, la localización del dolor (si tiene) y si aparece sintomatología en reposo o durante el sueño. Es importante saber si existe un mecanismo lesional, traumático o no, o una acción desencadenante.
Se deben investigar, entre otras, las circunstancias del primer episodio de luxación, si ha requerido reducción asistida, si hay confirmación de imagen del hombro luxado y preguntar también por el número de luxaciones previas, la edad a la que comenzó, si realiza deportes de contacto, si ha tenido cirugías previas en ese hombro, la dominancia, luxaciones de otras articulaciones, la voluntariedad a la hora de reproducir los síntomas, etc., ya que todos ellos son factores de riesgo de recidiva tras el tratamiento.
Exploración física
El objetivo de la exploración es realizar una serie de maniobras que desencadenen la clínica que aqueja al paciente. Hay que identificar la dirección de la inestabilidad (anterior, posterior, inferior) y si es unidireccional, bidireccional o multidireccional, así como la presencia de hiperlaxitud y/o discinesia escapulotorácica, además de descartar lesiones asociadas.
En este artículo, se describen las principales maniobras exploratorias relacionadas con la inestabilidad anterior y la hiperlaxitud.
Maniobras de exploración de inestabilidad anterior
Test de aprensión
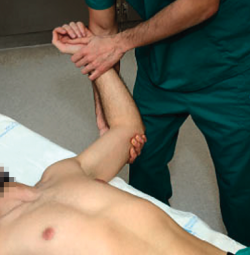
El paciente se coloca en decúbito supino sobre la camilla, con la extremidad a explorar libre y por fuera de la misma. El explorador coge el brazo llevándolo a 90° de abducción, con el codo flexionado y partiendo desde una posición de rotación neutra, va incrementando la rotación externa (Figura 1). Si esto provoca aprensión y dolor en el paciente, indica una inestabilidad anterior, con una sensibilidad del 72% y una especificidad del 96%(13). En ocasiones, la maniobra genera solo dolor, sin sensación real de inestabilidad; en estos casos, el dolor puede generar cierta confusión, pudiendo orientar hacia la presencia de inestabilidad anterior de hombro, pero para ello precisaremos de más maniobras específicas positivas, como la prueba de recolocación que se explica a continuación.
Prueba del recentrado o recolocación de Jobe
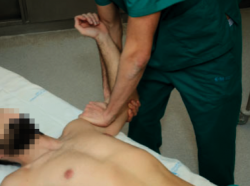
Partiendo de la posición de la maniobra de aprensión positiva, el explorador coloca la mano en la parte anterior de la mitad proximal del brazo aplicando una fuerza en sentido posterior, con objetivo de recentrar la cabeza en la glena; es positiva si desaparece el dolor y la aprensión, y se puede incrementar la rotación externa sin síntomas. (Figura 2). Esta prueba permite diferenciar los hombros dolorosos puros sin inestabilidad (tendrán un test de aprensión previo positivo, con un test de recolocación negativo) de los hombros dolorosos por inestabilidad (en los que ambos test, aprensión y recolocación, serían positivos) y puede indicar una lesión del labrum(14,15). Este test presenta una sensibilidad del 30-81% y una especificidad del 90-92%(13).
Test sorpresa
Partiendo de un test de recolocación positivo y desde esa misma posición, el examinador, súbitamente y sin previo aviso, deja de presionar la extremidad en sentido posterior, volviendo entonces la cabeza humeral, de forma espontánea y rápida, a su posición anterior forzada. Si la maniobra desencadena de nuevo la sensación dolorosa y/o de aprensión, se considera positiva para inestabilidad anterior(15). Este test tiene una sensibilidad del 63,89% y una especificidad del 98,91%(15).
La combinación positiva de los 3 test anteriores ha demostrado un alto valor predictivo positivo (93,6%) y un alto valor predictivo negativo (71,9%)(15).
Maniobras de exploración de la laxitud del hombro
Las siguientes maniobras permiten identificar un exceso de traslación o rotación debido a laxitud de las estructuras capsuloligamentosas, lo cual no tiene por qué ser patológico. De hecho, si aparecen de forma asintomática aislada y bilateral, no se considerarán patológicas.
Cajón anterior
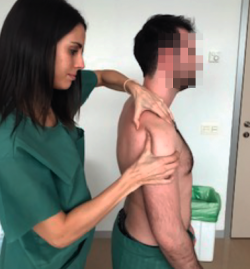
Consiste en empujar la cabeza humeral hacia anterior con una mano mientras con la otra mano se sujeta y bloquea la escápula (Figura 3). Se considera positiva si se objetiva un desplazamiento anterior excesivo de la cabeza humeral con facilidad, en comparación con el hombro contralateral. Se han establecido 3 grados en función del desplazamiento de la cabeza humeral respecto a la glena: en el tipo 1, la traslación llega hasta el borde glenoideo anterior; en el tipo 2, se sobrepasa el borde glenoideo; y en el tipo 3, la traslación excede el borde glenoideo y la cabeza humeral no se reduce espontáneamente. Esta prueba es indicativa de un exceso de laxitud de las estructuras capsuloligamentosas anteriores y tiene una sensibilidad del 53-58% y una especificidad del 85-93%(16).
Load and shift test
Con el paciente tumbado, se sitúa una mano sobre la porción distal del brazo y la otra sobre la proximal. Partiendo de la posición de 20° de abducción y flexión para centrar la cabeza humeral en la glena, se aplica fuerza en dirección axial hacia la glena y realizando una traslación anterior de la cabeza humeral. Será positiva si, al igual que con la prueba del cajón, se detecta una traslación humeral excesiva e indica exceso de laxitud anterior. Tiene una sensibilidad del 72% y una especificidad del 90%(16).
Test o signo de sulcus
Se aplica una tracción del brazo longitudinal en sentido inferior. Será positivo si la cabeza humeral se desplaza en sentido inferior y aparece un surco entre el acromion y la cabeza humeral(17), lo que traduce una laxitud inferior (receso capsular inferior redundante y ambos ligamentos glenohumerales inferiores) (Figura 4). Si es bilateral y asintomático, no se considera patológico.
Según el tamaño del surco, se puede clasificar en: tipo I, de menos de 1 cm; tipo II, de 1-2 cm; y tipo III, mayor de 2 cm.
Test de Gagey
Test de hiperabducción: con una mano se estabiliza la escápula y con la otra se abduce el brazo del paciente. Si presenta un exceso de abducción por encima de 105°, es sugestivo de hiperlaxitud(17). Si presenta una diferencia con el hombro contralateral de más de 20°, es sugestivo de insuficiencia del ligamento glenohumeral inferior. Siempre se debe realizar de forma bilateral comparando ambos hombros.
Es importante aclarar que la presencia de laxitud en el hombro no es sinónimo de hiperlaxitud. Para diagnosticar hiperlaxitud, debe estar presente también en otras articulaciones y para su diagnóstico debe reunir criterios como los de Beighton(18).
A las maniobras exploratorias aquí comentadas, hay que añadir todas aquellas orientadas a la detección de hiperlaxitud, discinesia escapulotorácica y lesiones neurológicas o de manguito rotador que pudieran estar asociadas, y cuya descripción no procede desarrollar en esta guía.
Pruebas de imagen y algoritmo diagnóstico
Radiografía simple
Será la primera prueba a realizar en el estudio diagnóstico de la inestabilidad glenohumeral y en algunos casos la única prueba necesaria.
Las proyecciones anteroposteriores (AP) en el plano escapular y axilar son básicas para valorar la adecuada congruencia articular, el espacio articular y la presencia de posibles lesiones óseas en la cabeza humeral (Hill-Sachs o McLaughlin) y en la glena. Es recomendable añadir proyecciones AP con rotaciones y proyección escapular en Y para visualizar mejor las tuberosidades, la coracoides, el acromion y los defectos óseos(19).
Las lesiones de Hill-Sachs (LHS) pequeñas en la proyección AP solo se aprecian con el hombro en rotación interna (Figura 5 A y B), mientras que las de mayor tamaño se ven tanto en rotación interna como externa(20), aunque la proyección que proporciona una mejor visión de las LHS es la axilar. Para valorar la pérdida ósea glenoidea, se recomienda una proyección axilar o la modificada de Bernageau, con una sensibilidad y especificidad por encima del 90%(20,21).
reaca.28272.fs2009049-figura5.png
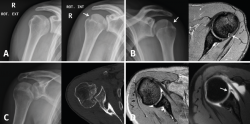
Figura 5. A y B: muestran 2 casos de pacientes con lesión de Hill-Sachs. A: se puede comparar cómo es más fácil visualizar el defecto con el hombro en rotación interna, especialmente si se trata de un defecto pequeño; B: se visualiza la misma lesión de Hill Sachs comparativamente en radiografía simple y resonancia magnética; C: tomografía axial computarizada (TAC) de una lesión de Hill-Sachs inversa; D: lesión de tipo ALPSA en resonancia magnética (RM) convencional y en artro-RM. La artro-RM es útil en caso de dudas diagnósticas, ya que proporciona una información más precisa sobre el tipo y las características de las lesiones capsulolabrales.
En caso de que estas lesiones óseas sean visibles en la radiología simple, significa que son de un tamaño considerable, por lo que estaría indicada la realización de una TAC para cuantificar el defecto.
Tomografía axial computarizada
Se considera el gold standard en la identificación de defectos óseos. Su realización estaría indicada en presencia de lesiones óseas en la radiología simple o con alta sospecha de las mismas.
Las reconstrucciones tridimensionales proporcionan información valiosa sobre la morfología de la glena, así como una medición precisa del tamaño, la ubicación y la profundidad de los defectos de la cabeza humeral (Figura 5C) y la glena(19,22), factores determinantes para la planificación quirúrgica.
Resonancia magnética (RM)
Es la técnica de elección para valorar lesiones de partes blandas y del cartílago. Está indicada en casos de inestabilidad recidivante, en casos de primer episodio de luxación con factores de alto riesgo de recidiva y en casos con sospecha de lesiones asociadas (manguito de los rotadores, condrales…). Permite analizar la presencia y la extensión de lesiones capsulolabrales(23) y articulares.
Se sabe que las lesiones del manguito rotador en pacientes con inestabilidad de hombro aumentan con la edad, habiéndose descrito un 40% entre los 40 y 55 años, un 71% entre los 56 y los 70 años y hasta un 100% por encima de los 70 años(24) Lo que justificaría la indicación de una RM en pacientes mayores de 40 años, para descartar lesiones del manguito de los rotadores.
Ecografía
La ecografía es una prueba de gran utilidad, ya que resulta una técnica rápida y fácil de realizar, que permite descartar lesiones del manguito rotador, especialmente en pacientes con riesgo de tenerlas (mayores de 40 años) y en pacientes en los que se sospechen clínicamente.
Artrorresonancia magnética (artro-RM)
La artro-RM con gadolinio intraarticular tiene mayor sensibilidad y especificidad para el diagnóstico de lesiones del labrum que la RM convencional sin contraste(19), aunque no es una prueba necesaria de rutina si la persona que analiza las imágenes de RM tiene experiencia. Se reserva para los casos en los que la RM convencional nos plantee dudas (Figura 5D) o en pacientes con recidiva posquirúrgica.
Protocolo de pruebas diagnósticas
El esquema a la hora de solicitar las pruebas diagnósticas descritas previamente cambia si se trata de un primer episodio de luxación o si es una sospecha de inestabilidad.
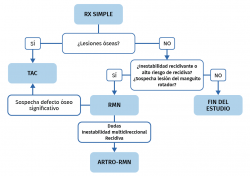
Tras un primer episodio de luxación glenohumeral, se debe comenzar el estudio con unas proyecciones radiológicas básicas, fundamentalmente una AP y una axilar. Con estas pruebas se descartará la presencia de lesiones óseas en la cabeza humeral y la glena. Si hubiera lesiones óseas, la siguiente prueba indicada sería una TAC para el estudio de las mismas. La ecografía se puede utilizar como screening inicial para descartar lesiones del manguito rotador asociadas en pacientes en edad de riesgo. La RM no es necesario que se realice de rutina tras un primer episodio, salvo en casos con factores de alto riesgo de recidiva, en los que queramos ampliar el estudio de cara a una posible actitud quirúrgica o por sospecha de lesiones del manguito asociadas o descritas en la ecografía previa (Figura 6).
Será distinto el protocolo del estudio en el contexto de una inestabilidad recurrente sintomática, en la que irá encaminado a identificar la causa de la misma, determinar de forma precisa el tipo de lesiones que presenta de cara a una correcta planificación quirúrgica en caso de estar indicada y descartar lesiones asociadas. Se debe comenzar el estudio con unas buenas proyecciones radiológicas AP y axilar, y con una RM. Esta nos permitirá realizar el diagnóstico de lesiones del labrum, capsuloligamentosas, condrales, óseas y tendinosas.
En presencia de lesiones óseas en la radiografía simple y/o en la RM, es recomendable realizar una TAC para el estudio de las mismas (Figura 6).
En casos más complejos como recidivas o en los que la RM nos suscite dudas y sea necesario ampliar el estudio estará indicada la artro-RM.
Relevancia de los defectos óseos en la inestabilidad glenohumeral anterior
Defectos óseos en la glena
La relevancia del estudio de las lesiones óseas glenoideas radica en la necesidad de cuantificar la magnitud del defecto óseo, ya que es decisivo a la hora de indicar el tratamiento quirúrgico, es decir, si se realizará una técnica de partes blandas o una técnica con injerto óseo.
Se han propuesto múltiples métodos para realizar mediciones sobre el defecto óseo en la glena: radiografía simple(25), TAC(26), RM(27,28) o artroscopia(29). El método cuantitativo más aceptado hasta el momento para la valoración del defecto óseo es la medición con TAC. Destacan 2 métodos: el método best-fit circle o el método de comparación con el hombro contralateral; de acuerdo con Jeske et al.(30), la diferencia en la superficie glenoidea entre los 2 hombros anatómicamente normales de un mismo individuo es de apenas un 1,8%. Por tanto, se puede utilizar el hombro contralateral como referencia, en caso de que no existiera defecto óseo. En casos en los que el hombro contralateral también sufra de inestabilidad glenohumeral, estaría indicado utilizar el método del best-fit circle(20).
Asimismo, hay 2 formas de expresar el defecto óseo: mediante medición del área o mediante medición lineal de la longitud del defecto. Generalmente, se prefiere la medición lineal del defecto, puesto que es más sencilla y no requiere ningún software especial(31). Con las reconstrucciones en 3 dimensiones (3D) de ambos hombros, se obtiene la visión frontal de la superficie glenoidea, sobre la cual se debe calcular la máxima distancia horizontal (anteroposterior) de la glena en ambos hombros. El defecto glenoideo (d) quedaría definido como diferencia entre la máxima distancia horizontal del hombro contralateral sano (D) menos la máxima distancia horizontal del hombro afectado. La medida de ese defecto óseo (d) se expresa en un porcentaje: d / D × 100 (%).
Establecer cuál es el máximo defecto óseo con el que se puede realizar una reparación de Bankart con bajo riesgo de recidiva no es una cuestión fácil. A lo largo del tiempo se han ido estableciendo diferentes límites por diversos autores. Clásicamente, se ha considerado un defecto en la superficie ósea de la glenoides de un 25% como límite para la utilización de técnicas de partes blandas en el tratamiento de la inestabilidad (por encima de este punto, sería necesaria la utilización de técnicas con injerto óseo como Latarjet o tope óseo con injerto de cresta iliaca o aloinjerto)(32,33). Para Itoi, un defecto del 21% de la longitud superoinferior o del 28% de la anchura de la glena es el límite a partir del cual aumenta la tasa de fallo de una reparación de partes blandas(34,35).
Lo comentado anteriormente es válido para defectos unipolares de la superficie glenoidea (de forma aislada). Sin embargo, la mayoría de los pacientes presentan defectos óseos combinados, que afectan tanto a la glena como a la cabeza humeral(33). En estos casos, defectos más pequeños en la glena combinados con defectos en la cabeza humeral pueden producir fallo en la reparación de partes blandas y recidiva de la inestabilidad.
En general, múltiples autores(31,36,37) coinciden en que un defecto glenoideo del 25% junto con los conceptos de on-track y off-track de las LHS definen los límites para el uso de una técnica de partes blandas o de tope óseo. Otros reconsideran bajar el límite del defecto glenoideo a un 20%. En general, cada vez se están aceptando o considerando como límite defectos glenoideos menores; algunos autores como Y. S. Jeon et al.(38) definen el límite en un 15-20% de defecto glenoideo anterior y, en esos casos, obtienen mejores resultados con la técnica de Latarjet que con procedimientos de Bankart de partes blandas (resultados mejores en cuanto a menos recidivas con el Latarjet: 6,5 frente a 22,5% con reparación de Bankart; p = 0,040)(38). Otro estudio, de J. S. Saha et al.(39), indica que la pérdida ósea "crítica" debe ser inferior al umbral del 20 al 25% que se cita a menudo; en su estudio, con una muestra de población militar con una actividad exigente, la pérdida ósea superior al 13,5% condujo a peores resultados(39). También el estudio de S. J. Shin et al.(40) concluye que el nivel crítico de pérdida ósea glenoidea anterior en el que deben considerarse las restauraciones óseas está más cerca del 15%(40).
Por tanto, no está definido un límite concreto de manera estandarizada y universal; en lo que sí parece haber concordancia según la bibliografía más actual es en que se deben tener en consideración los defectos óseos de glena comprendidos entre un 15 y un 25% y no solo a partir de un 25% como se afirmaba en publicaciones más antiguas. No existe en la bibliografía un protocolo concreto, sino que se recomienda individualizar cada caso con defectos óseos comprendidos en ese rango y estudiarlo de forma global junto con el resto de las lesiones y los factores de riesgo que presenten, sin subestimar lesiones óseas que superen el 15% de la glena.
En conclusión, según la mayor parte de la bibliografía actual consultada(38,39,40) y como recomendaciones generales para nuestro trabajo, en defectos óseos que superen un 20% de la glena, deben valorarse procedimientos que asocien aporte de hueso anterior, ya que se reducirá considerablemente el riesgo de recidiva. Y en defectos óseos comprendidos entre un 15 y un 20% es preferible individualizar cada caso, teniendo en cuenta de forma global todos los factores de riesgo de recidiva que presente, ya que estos pueden condicionar una actitud más agresiva con defectos menores.
Defectos óseos en la cabeza humeral
La LHS tiene una prevalencia de alrededor del 65% tras la primera luxación y de entre el 84 y el 93% tras luxaciones recurrentes(33,41).
Esta lesión produce inestabilidad en los movimientos de abducción combinada con rotación externa, ya que es en este momento cuando la zona posterolateral de la cabeza humeral entra en contacto con la glena. Si la lesión está contenida completamente dentro de la glena, no causará inestabilidad; sin embargo, si parte de la lesión no queda cubierta, puede engranarse con el borde anterior de la glena y producir una luxación. Esto se conoce como LHS enganchante (engaging Hill-Sachs lesion)(42).
Los conceptos de “lesión enganchante” y de “track glenoideo” o glenoid track (GT) son complementarios y consistentes entre sí, ya que ambos evalúan la presencia de defecto óseo humeral y su interacción con la glena durante el rango de movimiento. El GT es el área de la superficie articular posterior del húmero en contacto con la glena con el brazo en abducción y rotación externa máximas(31). Se ha establecido el GT a 90° de abducción como el 83% de la anchura de la superficie glenoidea(42). Para poder valorar si una LHS está dentro del GT y es on-track o está fuera y es off-track es importante conocer su disposición espacial con el hombro en abducción y la distancia existente entre el margen de la superficie articular (margen medial del GT) y el margen medial de la inserción del manguito rotador en la cabeza humeral.
La importancia de este concepto radica en su implicación clínica. La presencia de LHS off-track se asocia a mayor recurrencia tras la cirugía (33 a 75%) en comparación con la recurrencia de lesiones on-track (6 a 8%) cuando solo se trata mediante reparación de Bankart(43), y ha sido determinado como factor de riesgo independiente de recurrencia(44). En lesiones bipolares, al existir una lesión en la superficie glenoidea, se produce una disminución del GT, por lo que LHS que de forma aislada serían on-track, al combinarse con una lesión de la glena, pueden convertirse en off-track(33). La fórmula utilizada para calcular el GT del hombro afectado será calcular el 83% de la máxima distancia horizontal de la glena contralateral (GT normal) menos el defecto glenoideo (GT patológico = GT normal − d)(36). A continuación, sobre la visión posterior de la cabeza humeral calcularemos el defecto humeral (DH): diámetro de la LHS + puente óseo entre el margen lateral de la LHS y el margen medial del manguito rotador (DH = Hill-Sachs + puente óseo)(36).
Para establecer si la lesión es on-track u off-track, restaremos al GT el DH (GT − DH). De esta forma, si el DH es mayor que el GT, la lesión será off-track y la estabilización mediante una reparación de Bankart aislada correrá riesgo de fracasar (DH > GT → off-track). Por el contrario, si el DH es menor que el GT, la lesión será on-track y la estabilización mediante una reparación de Bankart aislada sería suficiente (DH < GT → on-track)(36).
El gesto asociado a las reparaciones de Bankart en casos de LHS off-track es el remplissage, técnica que se describirá más adelante.
Tratamiento conservador
El tratamiento conservador tras un primer episodio de luxación glenohumeral tiene como objetivo la cicatrización de estructuras lesionadas para restaurar la estabilidad y conseguir una movilidad articular completa y libre de dolor(45).
El tratamiento conservador está indicado en casos tras un primer episodio de luxación glenohumeral que no tengan factores de riesgo de recidiva. En presencia de estos factores, el tratamiento debe individualizarse y consensuarse según las particularidades de cada caso(46). El tratamiento conservador no estará indicado a priori en casos de múltiples luxaciones (2 o más), ni en casos en los que se diagnostique una inestabilidad establecida y sintomática(47).
El tratamiento consiste en inmovilizar de 1 a 3 semanas con un cabestrillo añadiendo tratamiento analgésico o antiinflamatorio(48) –aunque no existe evidencia de que inmovilizar más de 7-10 días disminuya de forma significativa la tasa de recurrencia(49)–, además de un programa fisioterápico estructurado por fases(50).
El abordaje de la rehabilitación de los pacientes tras un primer episodio de luxación glenohumeral se debe basar en las siguientes fases(51,52):
- Fase de protección. Su objetivo es la cicatrización capsulolabral. El paciente permanecerá inmovilizado con cabestrillo las primeras 1-3 semanas, retirándose únicamente para realizar los ejercicios de movilización pasiva de hombro, pendulares y de movilización activa de codo, muñeca y mano, además de ejercicios isométricos de deltoides y movilización escapular.
- Fase de recuperación activa. La finalidad de este periodo es la recuperación de la función del hombro. En esta fase se introducen los ejercicios de movilidad activa y pasiva de hombro, control neuromuscular escapular y, posteriormente, ejercicios de fuerza-resistencia según la tolerancia del individuo. Se recomienda fortalecer el manguito de los rotadores, que ayudará en la estabilidad, y restaurar el equilibrio o balance muscular del par infraespinoso-subescapular, así como ejercicios para la musculatura periescapular.
- Fase de recuperación funcional. La readaptación deportiva-laboral es la meta de esta fase, que se caracteriza por programas de recuperación individualizados. En este periodo se introduce el entrenamiento pliométrico.
Tratamiento quirúrgico de la inestabilidad glenohumeral sin defecto óseo
En el tratamiento de la inestabilidad de hombro se debe tener en cuenta la gran movilidad articular glenohumeral y la estabilidad de la misma. A la hora de indicar un tratamiento glenohumeral debemos conseguir un equilibrio entre la estabilización articular y la rigidez derivada de la reducción del rango de movimiento.
Ante una inestabilidad glenohumeral en la que no haya un defecto óseo significativo, la reparación capsulolabral, abierta o artroscópica, ha demostrado buenos resultados funcionales con baja tasa de recidiva(53,54,55). El progresivo adiestramiento de los cirujanos en técnicas artroscópicas ha permitido que esta técnica iguale a la técnica abierta en resultados funcionales postoperatorios y en la tasa de recidiva(56,57), minimizando las complicaciones debidas a la mayor agresión que supone la realización de una vía de abordaje quirúrgico(58).
Indicaciones(46)
Las principales indicaciones del tratamiento quirúrgico son:
- Inestabilidad glenohumeral (2 o más episodios de luxación) establecida y sintomática.
- Síntomas de inestabilidad glenohumeral sin llegar a luxación franca (episodios de subluxación ± aprensión ± dolor ± incomodidad) con presencia de lesión labral.
- Primer episodio de luxación glenohumeral con factores de alto riesgo de recurrencia (edad, deportes de contacto a nivel competitivo, defectos óseos significativos)(46,59).
De nuevo, estas indicaciones deben estar siempre supeditadas a los requerimientos y características de cada paciente, individualizándose siempre cada decisión terapéutica.
Técnica quirúrgica
Reparación capsulolabral artroscópica
La lesión de Bankart consiste en la desinserción de los ligamentos glenohumerales y el labrum en su porción anteroinferior; es la lesión más frecuente en los casos de inestabilidad anterior y además está presente tras un primer episodio de luxación en el 90% de las luxaciones traumáticas. La inestabilidad suele ser consecuencia de una no cicatrización de estas lesiones o una cicatrización en posición anómala, habitualmente medializadas sobre el cuello de la glena.
La reparación artroscópica de Bankart se considera la primera opción en el tratamiento de la inestabilidad traumática, unidireccional, anteroinferior e inferior del hombro. El tratamiento quirúrgico consistirá en liberar y movilizar el labrum, lo que permitirá reinsertarlo en su posición correcta. Dicha liberación y corrección de la posición labral resultará técnicamente más compleja en las lesiones de tipo ALPSA (anterior labroligamentous periosteal sleeve avulsion) y Perthes, pero resulta esencial para conseguir una reparación eficaz del labrum. De esta manera, con la reparación de Bankart se consigue fijar el labrum al borde de la glena y ascender la cápsula y los ligamentos en dirección proximal, dándoles tensión.
Descripción de la técnica
El procedimiento se realiza generalmente con el paciente bajo anestesia general y bloqueo del plexo braquial; es recomendable realizar una exploración bajo anestesia del hombro, ya que nos permite una exploración de la articulación glenohumeral con relajación muscular y confirmaremos clínicamente la inestabilidad, su tipo y grado.
La colocación del paciente puede ser en silla de playa o en decúbito lateral, a preferencia del cirujano. Se comienza con la introducción de un artroscopio de 30° a través de un portal posterior de visualización estándar. La exploración de la articulación glenohumeral de forma sistemática es de suma importancia para conseguir un diagnóstico certero de todas las lesiones, explorando posibles desprendimientos del labrum anterior, desgarros capsulares, lesiones superiores labrales y del bíceps, lesiones óseas que incluyen lesiones de Bankart óseo y LHS, patología del manguito rotador y la parte inferior del receso capsular para descartar una avulsión humeral del ligamento glenohumeral inferior.
Posteriormente, se establece un portal anteroinferior utilizando una técnica fuera dentro con una aguja espinal; el punto exacto del portal será aquel que nos permita alcanzar el labrum anteroinferior (posición de las 6 en huso horario), normalmente próximo al borde superior del subescapular y con una dirección de lateral a medial. Es recomendable la utilización de cánulas en todos los portales; en este portal, lo habitual es usar una cánula de 8 mm de diámetro, ya que será el portal de trabajo.
Y, por último, el portal anterosuperior accesorio, en el punto más lateral y superior del intervalo rotador y próximo a la corredera bicipital, de tal forma que permita trabajar a un lado y otro del bíceps. Este portal sirve para mejorar la visualización anterior del labrum y facilitar la recuperación de las suturas.
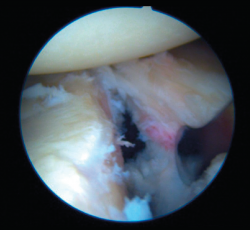
Una vez confirmada la lesión de Bankart, se despega y moviliza el complejo capsulobral del cuello glenoideo con raspadores y/o disectores artroscópicos hasta que sea satisfactorio y visualicemos fibras del subescapular (Figura 7). Antes de la colocación de los implantes es necesario realizar una decorticación del cuello anterior de la glenoides usando un sinoviotomo de 4 mm; tras este paso, se comienza la reparación comenzando siempre de inferior a superior.
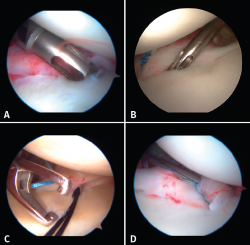
Los implantes deben colocarse a 45° de la superficie articular adyacentes al borde del cartílago anterior, teniendo cuidado de no medializarlos sobre el cuello de la glena (Figuras 8 A y B). Se empezará por el implante más inferior; dependiendo de la extensión de la lesión, precisará 3, 4 o 5 implantes, separados 3-5 mm entre ellos.
La reparación capsulolabral puede hacerse de diferentes maneras, ya que hay varios sistemas de paso de suturas: indirectos mediante un nitinol –suponen 2 pasos pero son menos lesivos para los tejidos– o directos con pinzas de paso directo –un solo paso pero más lesivo–.
Si usamos un sistema directo, consistirá en pasar una pinza penetrante-recuperahilos directa de anterior a posterior atravesando el tejido a suturar y recogiendo uno de los hilos del implante para después anudarlo sobre el poste, que será siempre el hilo que pasa por el tejido, e intentando mantener el nudo del hilo anterior al tejido reconstruido sin que roce con la superficie articular humeral. Este mismo paso puede realizarse con pinzas de paso indirecto, pasando un nitinol a través del tejido (Figura 8C), que permita enhebrar uno de los hilos del implante para después anudarlo (Figura 8D).
Si usamos implantes sin anudado (de tipo knotless) nos ahorraremos este paso del anudado, ya que son sistemas en los que el hilo va enhebrado y bloqueado dentro del implante. Estos implantes evitan el riesgo de aflojamiento del nudo y pérdida de tensión, o de que quede un nudo prominente que pueda movilizarse y rozar la superficie articular.
Presencia de lesiones asociadas
La presencia de deformidad plástica residual de la cápsula anteroinferior o hiperlaxitud de la cápsula subyacente se ha relacionado con el aumento de la tasa de recidivas debido a una insuficiencia del complejo capsuloligamentoso (haz anterior del ligamento glenohumeral inferior). En estos casos, estará indicado realizar una plicatura capsular, que consiste en incluir en el paso de sutura la cápsula inferior para intentar englobarla en la reparación. De esta manera, se consigue ascender la cápsula y los ligamentos inferiores en dirección proximal, consiguiendo mayor tensión de los mismos y obteniendo mayor estabilidad en nuestra reparación.
La lesión HAGL (humeral avulsión of the glenohumeral ligaments) consiste en la avulsión en el lado humeral del ligamento glenohumeral inferior. Es más frecuente el HAGL anterior (desinserción de ligamento glenohumeral inferior anterior) que el HAGL posterior. En algunos casos, puede asociar un fragmento óseo de la parte medial del cuello del húmero (bony HAGL). Estas lesiones pueden por sí mismas generar una inestabilidad glenohumeral sintomática sin la existencia de una lesión capsulolabral(60).
Son lesiones poco frecuentes (1-10%) y muy infradiagnosticadas. Se suelen diagnosticar artroscópicamente, pasando desapercibidas en la RM. Si pasan desapercibidas y no se tratan de manera adecuada, pueden ser causa de una luxación recidivante(61). El tratamiento de estas lesiones consiste en refijar la cápsula y los ligamentos glenohumerales a su inserción humeral anatómica mediante implantes. Se han descrito numerosas técnicas para reparar estas lesiones en función del número y el tipo de anclajes a utilizar, el orden a seguir en la reparación y el tipo de nudo a utilizar(62). De nuevo, el tipo de lesión y las características del paciente obligarán a una decisión individualizada sobre la técnica de reparación más conveniente en cada caso.
En caso de rotura completa del ligamento glenohumeral inferior o cápsula articular insuficiente se prefieren tratamientos con ligamentoplastias abiertas o incluso técnicas de tope óseo. Mikel Sánchez et al.(63) describieron una técnica asistida por artroscopia para la reconstrucción del ligamento glenohumeral inferior por medio de un refuerzo capsular artificial en 167 pacientes con resultados satisfactorios.
Las LHS asociadas al Bankart se encuentran en un porcentaje alto de casos (71-100%); debe distinguirse si la lesión es enganchante o no(33), o bien, si se ha utilizado la medición del GT para valorar en conjunto el déficit óseo humeral y glenoideo, determinar si es una lesión on-track u off-track.
Si es enganchante u off-track, el riesgo de recidiva aumenta considerablemente(33); en estos casos, el gesto quirúrgico a realizar debe convertir la LHS en on-track de nuevo o en no enganchante. La técnica de remplissage se ha utilizado con éxito para conseguir este fin(64) y consiste en fijar la cápsula posterior y parte del tendón infraespinoso (capsulotenodesis) al defecto óseo de la cabeza humeral. Connolly et al.(65) propusieron esta técnica como un procedimiento abierto hace 4 décadas, pero fue Wolf en 2004 quien describió por primera vez la técnica artroscópica como una modificación del procedimiento abierto. Muchos autores han informado de buenos resultados combinando la reparación artroscópica de Bankart con el remplissage. Wolf et al.(66) informaron de los resultados de seguimiento de hasta 10 años donde observaron que solo 2 de 45 pacientes (4,4%) experimentaron recurrencia. Boileau et al.(61) realizaron este procedimiento en 47 de 459 hombros y solo un hombro (2,1%) tuvo inestabilidad recurrente. Las revisiones sistemáticas recientes han descrito que la tasa de recurrencia general después de combinar ambas técnicas va de un 3,4 a un 5,4%, sin restricciones importantes del balance articular(67,68). Como efecto indeseado, la técnica puede provocar cierta disminución de la movilidad, especialmente de la rotación externa, pero disminuye considerablemente la recurrencia de inestabilidad(61).
Las lesiones del manguito rotador aumentan con la edad (80% en mayores de 60 años). Por ello, debemos sospecharlas siempre en pacientes mayores de 40 años o con clínica del manguito, en los que estaría indicado pedir una RM o una ecografía para diagnosticarlas y tratarlas.
Complicaciones
La complicación más frecuente es la recurrencia. La tasa de recidiva descrita por la mayoría de los estudios tras la reparación de Bankart está comprendida entre el 6 y el 12,5%(57,69), y dicha tasa de recurrencia es inversamente proporcional a la edad (tanto la edad a la que se realiza la cirugía como a la edad a la que comenzó la inestabilidad) y directamente proporcional al número de luxaciones previas y al grado de afectación de la anatomía del hombro tras sucesivas luxaciones (deformación plástica de la cápsula, afectación de la musculatura que rodea al hombro, etc.)(70). Ambos, la edad menor y el número de luxaciones previas a la cirugía, se consideran los factores de riesgo de recurrencia más relevantes tras la cirugía(71).
La rigidez es una complicación frecuente relacionada más con los abordajes abiertos y los primeros tratamientos artroscópicos con implantes no reabsorbibles; la pérdida del rango de movilidad más comúnmente descrita es la de la rotación externa. La incidencia global de rigidez tras Bankart artroscópico va de un 1,6(72) a un 5%(73). La mayoría de los pacientes con rigidez responden al tratamiento conservador, barajando la movilización bajo anestesia y/o la capsulotomía artroscópica si no hay mejoría tras 6 meses(74). En casos con pérdida severa aislada de la rotación externa, se ha propuesto realizar tratamiento artroscópico con liberación del intervalo rotador y de las adherencias entre el tendón del subescapular y el cuello de la glena(75).
Las complicaciones infecciosas que se han descrito fundamentalmente han sido infecciones superficiales de los portales artroscópicos; la tasa de infección profunda descrita es del 0,22%, siendo los patógenos más frecuentes los estafilococos (S. aereus y S. epidermidis). Cuando se confirma la infección, se recomienda realizar lavado articular de forma precoz y toma de cultivos, comenzando con antibioticoterapia lo antes posible(63).
Otra complicación es la condrolisis, que se caracteriza por la rápida destrucción del cartílago articular debido a la destrucción de los condrocitos y la disolución de la matriz del cartílago. Esta complicación se ha descrito en la capsulorrafia térmica. También se ha encontrado en un 50% de los casos en los que se ha realizado infiltración con bupivacaína (0,5%) introducida mediante catéter de bomba de dolor intraarticular a alto flujo en el postoperatorio(76,77).
Aunque muy infrecuentes, se han descrito lesiones nerviosas (0,3%)(78); el nervio más lesionado es el nervio axilar, que se extiende por delante del músculo subescapular y comienza a descansar en el borde inferolateral del tendón subescapular, lesionándose al realizar la reconstrucción capsulolabral en la zona anteroinferior (entre las posiciones 5 y 6 del huso horario). Una vez identificada la lesión nerviosa, se debe de esperar entre 3 y 6 meses, optando por la exploración quirúrgica en caso de no mejorar tras este periodo. También se han descrito lesiones nerviosas transitorias del plexo braquial y del nervio cubital, autolimitadas(74).
Conclusiones
La inestabilidad glenohumeral traumática es una entidad patológica especialmente frecuente en la población joven y físicamente activa. La historia clínica debe estar dirigida a identificar correctamente el problema y los factores de riesgo de recidiva tras el tratamiento. Las pruebas complementarias deben indicar dónde está el origen de la lesión y cuantificarla. Cuando no haya un defecto óseo significativo, es decir, un defecto óseo glenoideo inferior a un 20% o inferior a un 15% si acumula otros factores de riesgo, la reparación capsulolabral artroscópica es una técnica segura, reproducible y eficaz para tratar esta entidad.
Figuras
Figura 5. A y B: muestran 2 casos de pacientes con lesión de Hill-Sachs. A: se puede comparar cómo es más fácil visualizar el defecto con el hombro en rotación interna, especialmente si se trata de un defecto pequeño; B: se visualiza la misma lesión de Hill Sachs comparativamente en radiografía simple y resonancia magnética; C: tomografía axial computarizada (TAC) de una lesión de Hill-Sachs inversa; D: lesión de tipo ALPSA en resonancia magnética (RM) convencional y en artro-RM. La artro-RM es útil en caso de dudas diagnósticas, ya que proporciona una información más precisa sobre el tipo y las características de las lesiones capsulolabrales.
Información del artículo
Cita bibliográfica
Autores
Andrea Paniagua González
Unidad de Hombro y Codo. Hospital Fraternidad-Muprespa Habana. Madrid
Unidad de Hombro y Codo. Hospital Universitario Ramón y Cajal. Madrid
Lorena Trueba Sánchez
Hospital Mompía. Santander, Cantabria
Cirugía Ortopédica y Traumatología. Hospital Universitario de Burgos
Noelia Alonso García
Complejo Asistencial de Segovia
Alfonso Vaquero Picado
Servicio de Cirugía Ortopédica y Traumatología A, Hospital Universitario La Paz, Madrid, España
Jorge García Donaire
Hospital Cenyt. Estepona, Málaga
Maximiliano Sánchez Martos
Hospital Universitario Virgen de Valme. Sevilla
Javier Ruiz Diaz
Ibermutua. Oviedo
Hospital Ibermutua Asturias
Gonzalo Hernández Fernandez
Hospital Central de la Defensa Gómez Ulla. Madrid
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de interés.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Owens BD, Nelson BJ, Duffey ML, Mountcastle SB, Taylor DC, Cameron KL, et al. Pathoanatomy of first-time, traumatic, anterior glenohumeral subluxation events. J Bone Joint Surg Am. 2010;92(7):1605-11.
-
2Zacchilli MA, Owens BD. Epidemiology of shoulder dislocations presenting to emergency departments in the United States. J Bone Joint Surg Am. 2010;92(3):542-9.
-
3Rockwood CA. The shoulder. Philadelphia: Saunders/Elsevier; 2009.
-
4Olds M, Ellis R, Donaldson K, Parmar P, Kersten P. Risk factors which predispose first-time traumatic anterior shoulder dislocations to recurrent instability in adults: a systematic review and meta-analysis. Br J Sports Med. 2015;49(14):913-22.
-
5Hayes K, Callanan M, Walton J, Paxinos A, Murrell GA. Shoulder instability: management and rehabilitation. J Orthop Sports Phys Ther. 2002;32(10):497-509.
-
6Rowe CR. Prognosis in dislocations of the shoulder. J Bone Joint Surg Am. 1956;38-A(5):957-77.
-
7Robinson CM, Howes J, Murdoch H, Will E, Graham C. Functional outcome and risk of recurrent instability after primary traumatic anterior shoulder dislocation in young patients. J Bone Joint Surg Am. 2006;88(11):2326-36.
-
8Hovelius L, Olofsson A, Sandstrom B, Augustini BG, Krantz L, Fredin H, et al. Nonoperative treatment of primary anterior shoulder dislocation in patients forty years of age and younger. A prospective twenty-five-year follow-up. J Bone Joint Surg Am. 2008;90(5):945-52.
-
9Balg F, Boileau P. The instability severity index score. A simple pre-operative score to select patients for arthroscopic or open shoulder stabilisation. J Bone Joint Surg Br. 2007;89(11):1470-7.
-
10Griffith JF, Antonio GE, Yung PS, Wong EM, Yu AB, Ahuja AT, et al. Prevalence, pattern, and spectrum of glenoid bone loss in anterior shoulder dislocation: CT analysis of 218 patients. AJR Am J Roentgenol. 2008;190(5):1247-54.
-
11Dickens JF, Slaven SE, Cameron KL, Pickett AM, Posner M, Campbell SE, et al. Prospective Evaluation of Glenoid Bone Loss After First-time and Recurrent Anterior Glenohumeral Instability Events. Am J Sports Med. 2019;47(5):1082-9.
-
12Hovelius L, Augustini BG, Fredin H, Johansson O, Norlin R, Thorling J. Primary anterior dislocation of the shoulder in young patients. A ten-year prospective study. J Bone Joint Surg Am. 1996;78(11):1677-84.
-
13Farber AJ, Castillo R, Clough M, Bahk M, McFarland EG. Clinical assessment of three common tests for traumatic anterior shoulder instability. J Bone Joint Surg Am. 2006;88(7):1467-74.
-
14Bushnell BD, Creighton RA, Herring MM. The bony apprehension test for instability of the shoulder: a prospective pilot analysis. Arthroscopy. 2008;24(9):974-82.
-
15Lo IK, Nonweiler B, Woolfrey M, Litchfield R, Kirkley A. An evaluation of the apprehension, relocation, and surprise tests for anterior shoulder instability. Am J Sports Med. 2004;32(2):301-7.
-
16Hippensteel KJ, Brophy R, Smith MV, Wright RW. Comprehensive Review of Provocative and Instability Physical Examination Tests of the Shoulder. J Am Acad Orthop Surg. 2019;27(11):395-404.
-
17Eshoj H, Ingwersen KG, Larsen CM, Kjaer BH, Juul-Kristensen B. Intertester reliability of clinical shoulder instability and laxity tests in subjects with and without self-reported shoulder problems. BMJ Open. 2018;8(3):e018472.
-
18Beighton P, Horan F. Orthopaedic aspects of the Ehlers-Danlos syndrome. J Bone Joint Surg Br. 1969;51(3):444-53.
-
19Cain EL Jr, Ryan MK. Traumatic Instability: Treatment Options and Considerations for Recurrent Posttraumatic Instability. Sports Med Arthrosc Rev. 2018;26(3):102-12.
-
20Saliken DJ, Bornes TD, Bouliane MJ, Sheps DM, Beaupre LA. Imaging methods for quantifying glenoid and Hill-Sachs bone loss in traumatic instability of the shoulder: a scoping review. BMC Musculoskelet Disord. 2015;16:164.
-
21Pansard E, Klouche S, Billot N, Rousselin B, Kraus TM, Bauer T, et al. Reliability and validity assessment of a glenoid bone loss measurement using the Bernageau profile view in chronic anterior shoulder instability. J Shoulder Elbow Surg. 2013;22(9):1193-8.
-
22Sugaya H. Techniques to evaluate glenoid bone loss. Curr Rev Musculoskelet Med. 2014;7(1):1-5.
-
23Waldt S, Burkart A, Imhoff AB, Bruegel M, Rummeny EJ, Woertler K. Anterior shoulder instability: accuracy of MR arthrography in the classification of anteroinferior labroligamentous injuries. Radiology. 2005;237(2):578-83.
-
24Simank HG, Dauer G, Schneider S, Loew M. Incidence of rotator cuff tears in shoulder dislocations and results of therapy in older patients. Arch Orthop Trauma Surg. 2006;126(4):235-40.
-
25Garth WP Jr, Slappey CE, Ochs CW. Roentgenographic demonstration of instability of the shoulder: the apical oblique projection. A technical note. J Bone Joint Surg Am. 1984;66(9):1450-3.
-
26Griffith JF, Antonio GE, Tong CW, Ming CK. Anterior shoulder dislocation: quantification of glenoid bone loss with CT. AJR Am J Roentgenol. 2003;180(5):1423-30.
-
27Huijsmans PE, Haen PS, Kidd M, Dhert WJ, van der Hulst VP, Willems WJ. Quantification of a glenoid defect with three-dimensional computed tomography and magnetic resonance imaging: a cadaveric study. J Shoulder Elbow Surg. 2007;16(6):803-9.
-
28Omori Y, Yamamoto N, Koishi H, Futai K, Goto A, Sugamoto K, et al. Measurement of the Glenoid Track In Vivo as Investigated by 3-Dimensional Motion Analysis Using Open MRI. Am J Sports Med. 2014;42(6):1290-5.
-
29Burkhart SS, Debeer JF, Tehrany AM, Parten PM. Quantifying glenoid bone loss arthroscopically in shoulder instability. Arthroscopy. 2002;18(5):488-91.
-
30Jeske HC, Oberthaler M, Klingensmith M, Dallapozza C, Smekal V, Wambacher M, et al. Normal glenoid rim anatomy and the reliability of shoulder instability measurements based on intrasite correlation. Surg Radiol Anat. 2009;31(8):623-5.
-
31Itoi E. 'On-track' and 'off-track' shoulder lesions. EFORT Open Rev. 2017;2(8):343-51.
-
32Gerber C, Nyffeler RW. Classification of glenohumeral joint instability. Clin Orthop Relat Res. 2002(400):65-76.
-
33Burkhart SS, De Beer JF. Traumatic glenohumeral bone defects and their relationship to failure of arthroscopic Bankart repairs: significance of the inverted-pear glenoid and the humeral engaging Hill-Sachs lesion. Arthroscopy. 2000;16(7):677-94.
-
34Itoi E, Lee SB, Berglund LJ, Berge LL, An KN. The effect of a glenoid defect on anteroinferior stability of the shoulder after Bankart repair: a cadaveric study. J Bone Joint Surg Am. 2000;82(1):35-46.
-
35Yamamoto N, Muraki T, Sperling JW, Steinmann SP, Cofield RH, Itoi E, et al. Stabilizing mechanism in bone-grafting of a large glenoid defect. J Bone Joint Surg Am. 2010;92(11):2059-66.
-
36Di Giacomo G, Itoi E, Burkhart SS. Evolving concept of bipolar bone loss and the Hill-Sachs lesion: from "engaging/non-engaging" lesion to "on-track/off-track" lesion. Arthroscopy. 2014;30(1):90-8.
-
37Di Giacomo G, Piscitelli L, Pugliese M. The role of bone in glenohumeral stability. EFORT Open Rev. 2018;3(12):632-40.
-
38Jeon YS, Jeong HY, Lee DK, Rhee YG. Borderline Glenoid Bone Defect in Anterior Shoulder Instability: Latarjet Procedure Versus Bankart Repair. Am J Sports Med. 2018;46(9):2170-6.
-
39Shaha JS, Cook JB, Song DJ, Rowles DJ, Bottoni CR, Shaha SH, et al. Redefining "Critical" Bone Loss in Shoulder Instability: Functional Outcomes Worsen With "Subcritical" Bone Loss. Am J Sports Med. 2015;43(7):1719-25.
-
40Shin SJ, Koh YW, Bui C, Jeong WK, Akeda M, Cho NS, et al. What Is the Critical Value of Glenoid Bone Loss at Which Soft Tissue Bankart Repair Does Not Restore Glenohumeral Translation, Restricts Range of Motion, and Leads to Abnormal Humeral Head Position? Am J Sports Med. 2016;44(11):2784-91.
-
41Spatschil A, Landsiedl F, Anderl W, Imhoff A, Seiler H, Vassilev I, et al. Posttraumatic anterior-inferior instability of the shoulder: arthroscopic findings and clinical correlations. Arch Orthop Trauma Surg. 2006;126(4):217-22.
-
42Yamamoto N, Itoi E, Abe H, Minagawa H, Seki N, Shimada Y, et al. Contact between the glenoid and the humeral head in abduction, external rotation, and horizontal extension: a new concept of glenoid track. J Shoulder Elbow Surg. 2007;16(5):649-56.
-
43Shaha JS, Cook JB, Rowles DJ, Bottoni CR, Shaha SH, Tokish JM. Clinical Validation of the Glenoid Track Concept in Anterior Glenohumeral Instability. J Bone Joint Surg Am. 2016;98(22):1918-23.
-
44Lee SH, Lim KH, Kim JW. Risk Factors for Recurrence of Anterior-Inferior Instability of the Shoulder After Arthroscopic Bankart Repair in Patients Younger Than 30 Years. Arthroscopy. 2018;34(9):2530-6.
-
45Boffano M, Mortera S, Piana R. Management of the first episode of traumatic shoulder dislocation. EFORT Open Rev. 2017;2(2):35-40.
-
46Ávila Lafuente JL, Moros Marco S, García Pequerul JM. Controversies in the Management of the First Time Shoulder Dislocation. Open Orthop J. 2017;11:1001-10.
-
47Handoll HH, Hanchard NC, Goodchild L, Feary J. Conservative management following closed reduction of traumatic anterior dislocation of the shoulder. Cochrane Database Syst Rev. 2006(1):CD004962.
-
48De Carli A, Vadala AP, Lanzetti R, Lupariello D, Gaj E, Ottaviani G, et al. Early surgical treatment of first-time anterior glenohumeral dislocation in a young, active population is superior to conservative management at long-term follow-up. Int Orthop. 2019;43(12):2799-805.
-
49Paterson WH, Throckmorton TW, Koester M, Azar FM, Kuhn JE. Position and duration of immobilization after primary anterior shoulder dislocation: a systematic review and meta-analysis of the literature. J Bone Joint Surg Am. 2010;92(18):2924-33.
-
50Ruiz Ibán MA, Díaz Heredia J, García Navlet M, Serrano F, Santos Oliete M. Multidirectional Shoulder Instability: Treatment. Open Orthop J. 2017;11:812-25.
-
51Bateman M, Smith BE, Osborne SE, Wilkes SR. Physiotherapy treatment for atraumatic recurrent shoulder instability: early results of a specific exercise protocol using pathology-specific outcome measures. Shoulder Elbow. 2015;7(4):282-8.
-
52Wilk KE, Macrina LC. Nonoperative and postoperative rehabilitation for glenohumeral instability. Clin Sports Med. 2013;32(4):865-914.
-
53Adam M, Attia AK, Alhammoud A, Aldahamsheh O, Al Ateeq Al Dosari M, Ahmed G. Arthroscopic Bankart repair for the acute anterior shoulder dislocation: systematic review and meta-analysis. Int Orthop. 2018;42(10):2413-22.
-
54Mahure SA, Mollon B, Capogna BM, Zuckerman JD, Kwon YW, Rokito AS. Risk factors for recurrent instability or revision surgery following arthroscopic Bankart repair. Bone Joint J. 2018;100-B(3):324-30.
-
55Kennedy MI, Murphy C, Dornan GJ, Moatshe G, Chahla J, LaPrade RF, et al. Variability of Reporting Recurrence After Arthroscopic Bankart Repair: A Call for a Standardized Study Design. Orthop J Sports Med. 2019;7(5):2325967119846915.
-
56Hobby J, Griffin D, Dunbar M, Boileau P. Is arthroscopic surgery for stabilisation of chronic shoulder instability as effective as open surgery? A systematic review and meta-analysis of 62 studies including 3044 arthroscopic operations. J Bone Joint Surg Br. 2007;89(9):1188-96.
-
57Petrera M, Patella V, Patella S, Theodoropoulos J. A meta-analysis of open versus arthroscopic Bankart repair using suture anchors. Knee Surg Sports Traumatol Arthrosc. 2010 Dec;18(12):1742-7.
-
58Williams HLM, Evans JP, Furness ND, Smith CD. It's Not All About Redislocation: A Systematic Review of Complications After Anterior Shoulder Stabilization Surgery. Am J Sports Med. 2019;47(13):3277-83.
-
59Boone JL, Arciero RA. First-time anterior shoulder dislocations: has the standard changed? Br J Sports Med. 2010;44(5):355-60.
-
60Bui-Mansfield LT, Banks KP, Taylor DC. Humeral avulsion of the glenohumeral ligaments: the HAGL lesion. Am J Sports Med. 2007;35(11):1960-6.
-
61Boileau P, O'Shea K, Vargas P, Pinedo M, Old J, Zumstein M. Anatomical and functional results after arthroscopic Hill-Sachs remplissage. J Bone Joint Surg Am. 2012;94(7):618-26.
-
62Provencher MT, McCormick F, LeClere L, Sánchez G, Golijanin P, Anthony S, et al. Prospective Evaluation of Surgical Treatment of Humeral Avulsions of the Glenohumeral Ligament. Am J Sports Med. 2017;45(5):1134-40.
-
63Moen TC, Rudolph GH, Caswell K. Complications of shoulder arthroscopy. J Am Acad Orthop Surg. 2014, 22(7):410-9.
-
64Purchase RJ, Wolf EM, Hobgood ER, Pollock ME, Smalley CC. Hill-sachs "remplissage": an arthroscopic solution for the engaging hill-sachs lesion. Arthroscopy. 2008;24(6):723-6.
-
65Connolly J, Regen E, Evans OB. The management of the painful, stiff shoulder. Clin Orthop Relat Res. 1972;84:97-103.
-
66Wolf EM, Arianjam A. Hill-Sachs remplissage, an arthroscopic solution for the engaging Hill-Sachs lesion: 2- to 10-year follow-up and incidence of recurrence. J Shoulder Elbow Surg. 2014;23(6):814-20.
-
67Alkaduhimi H, Verweij LPE, Willigenburg NW, van Deurzen DFP, van den Bekerom MPJ. Remplissage With Bankart Repair in Anterior Shoulder Instability: A Systematic Review of the Clinical and Cadaveric Literature. Arthroscopy. 2019;35(4):1257-66.
-
68Camus D, Domos P, Berard E, Toulemonde J, Mansat P, Bonnevialle N. Isolated arthroscopic Bankart repair vs. Bankart repair with "remplissage" for anterior shoulder instability with engaging Hill-Sachs lesion: a meta-analysis. Orthop Traumatol Surg Res. 2018;104(6):803-9.
-
69Harris JD, Gupta AK, Mall NA, Abrams GD, McCormick FM, Cole BJ, et al. Long-term outcomes after Bankart shoulder stabilization. Arthroscopy. 2013;29(5):920-33.
-
70Olds MK, Ellis R, Parmar P, Kersten P. Who will redislocate his/her shoulder? Predicting recurrent instability following a first traumatic anterior shoulder dislocation. BMJ Open Sport Exerc Med. 2019;5(1):e000447.
-
71Wasserstein D, Dwyer T, Veillette C, Gandhi R, Chahal J, Mahomed N, et al. Predictors of dislocation and revision after shoulder stabilization in Ontario, Canada, from 2003 to 2008. Am J Sports Med. 2013;41(9):2034-40.
-
72Ahmed I, Ashton F, Robinson CM. Arthroscopic Bankart repair and capsular shift for recurrent anterior shoulder instability: functional outcomes and identification of risk factors for recurrence. J Bone Joint Surg Am. 2012;94(14):1308-15.
-
73Elmlund AO, Kartus J, Rostgard-Christensen L, Sernert N, Magnusson L, Ejerhed L. A 7-year prospective, randomized, clinical, and radiographic study after arthroscopic Bankart reconstruction using 2 different types of absorbable tack. Am J Sports Med. 2009;37(10):1930-7.
-
74Matsuki K, Sugaya H. Complications after arthroscopic labral repair for shoulder instability. Curr Rev Musculoskelet Med. 2015;8(1):53-8.
-
75Ando A, Sugaya H, Takahashi N, Kawai N, Hagiwara Y, Itoi E. Arthroscopic management of selective loss of external rotation after surgical stabilization of traumatic anterior glenohumeral instability: arthroscopic restoration of anterior transverse sliding procedure. Arthroscopy. 2012;28(6):749-53.
-
76Matsen FA 3rd, Papadonikolakis A. Published evidence demonstrating the causation of glenohumeral chondrolysis by postoperative infusion of local anesthetic via a pain pump. J Bone Joint Surg Am. 2013;95(12):1126-34.
-
77Scheffel PT, Clinton J, Lynch JR, Warme WJ, Bertelsen AL, Matsen FA 3rd. Glenohumeral chondrolysis: a systematic review of 100 cases from the English language literature. J Shoulder Elbow Surg. 2010;19(6):944-9.
-
78Owens BD, Harrast JJ, Hurwitz SR, Thompson TL, Wolf JM. Surgical trends in Bankart repair: an analysis of data from the American Board of Orthopaedic Surgery certification examination. Am J Sports Med. 2011;39(9):1865-9.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- <em>REACA</em>: escuela de autores
- La reconstrucción del ligamento patelofemoral medial es eficaz en el tratamiento de la inestabilidad patelofemoral lateral, incluso en presencia de displasia troclear. Una revisión de 18 casos
- Resultados de la encuesta sobre el uso del ecógrafo realizada a los socios de la Asociación Española de Artroscopia (AEA)
- Manejo de la inestabilidad glenohumeral anterior sin lesión ósea glenoidea significativa
- Rehabilitación tras reparación capsulolabral anterior de Bankart artroscópica: una guía para el artroscopista joven
- Diagnóstico y manejo de la lesión del ligamento cruzado anterior en pacientes esqueléticamente inmaduros. Una revisión narrativa
- Inestabilidad residual tras cirugía de reconstrucción del ligamento cruzado anterior. ¿Qué estamos pasando por alto?
- Inestabilidad posterolateral de rodilla tras fractura osteocondral que incluye la inserción femoral del tendón poplíteo. A propósito de un caso
- Porción larga del bíceps de tipo MESO: variante anatómica de la normalidad
- Normas de publicación (Abr. 2021)
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.