Injerto de cartílago en fresco. Indicaciones, técnica quirúrgica y evidencia científica
Fresh osteochondral graft. Indications, surgical technique and scientific evidence
Resumen:
Las lesiones condrales de la rodilla de espesor completo suponen un desafío para el cirujano ortopédico cuando se presentan en pacientes jóvenes y son sintomáticas. El aloinjerto osteocondral en fresco es un procedimiento válido para tratar grandes defectos osteocondrales de rodilla en pacientes jóvenes y activos, en los que la cirugía protésica no está indicada. Esta técnica quirúrgica ofrece la posibilidad de restaurar de manera inmediata la estructura histológica condral y ósea original sin añadir comorbilidad a la zona donante. Puede ser también utilizada en casos complejos de reconstrucción articular en el contexto de osteonecrosis, osteocondritis disecante, mala unión, artritis postraumática o en procedimientos de revisión. Los bancos de células y tejidos han mejorado la disponibilidad de este tipo de aloinjerto gracias a la optimización de las técnicas de procesado y de almacenamiento. Asimismo, la aplicación de protocolos estrictos de cribado de los donantes mediante pruebas serológicas aseguran un riesgo de transmisión de enfermedades mínimo. Para asegurar la supervivencia del injerto, es necesario realizar una adecuada selección del paciente, así como evaluar las condiciones de malalineación, estabilidad ligamentosa y déficit meniscal. El objetivo de este trabajo es revisar las indicaciones y los aspectos más destacados de la técnica quirúrgica, además de describir la tasa de supervivencia del aloinjerto osteocondral en fresco en distintas localizaciones de la rodilla.
Abstract:
Full-thickness chondral lesions of the knee are a challenge for orthopedic surgeons when manifesting with symptoms in young patients. Fresh osteochondral allografts are a valid option for treating large osteochondral defects of the knee in young and active individuals in which prosthetic surgery is not indicated. This surgical technique allows immediate restoration of the original bone and chondral histological structure without adding comorbidity to the donor zone. It can also be used in complex joint reconstruction cases in the context of osteonecrosis, osteochondritis dissecans, malunion, post-traumatic osteoarthritis, or in revision surgery. Cell and tissue banks have improved the availability of this type of allograft thanks to optimization of the processing and storage techniques. Likewise, the application of strict donor screening protocols based on serological tests ensures a minimum risk of disease transmission.
In order to ensure graft survival, adequate patient selection is required, with the evaluation of misalignment, ligament stability and meniscus deficit. The purpose of the present study was to review the indications and main aspects of the surgical technique, and to describe the fresh osteochondral allograft survival rate in different locations of the knee.
Antecedentes
Las lesiones del cartílago articular en la rodilla son frecuentes en personas jóvenes y activas (26 a 47 años)(1). La prevalencia de estas lesiones durante la evaluación artroscópica se sitúa en torno al 65%, de las cuales entre el 5 y el 20% son de alto grado(2,3,4,5,6). La mayoría de las veces la lesión del cartílago articular cursa con un dolor insidioso y derrame de la rodilla en relación con la actividad deportiva y conlleva una drástica afectación de la calidad de vida, no solo durante el deporte sino también en actividades de la vida diaria(7). Cuando la lesión condral afecta al espesor completo, puede ser necesario recurrir a técnicas de reparación condral hasta en un 11% de los casos(5).
En este tipo de pacientes, la artroplastia de sustitución ofrece resultados de satisfacción bajos y además tiene un elevado riesgo de cirugía de revisión por aflojamiento o desgaste(8,9). Es por ello que el objetivo de la cirugía debe ser restaurar la biología articular, aliviar el dolor, mejorar la funcionalidad y retrasar o eliminar la necesidad de la cirugía protésica.
En la actualidad, el uso de autoinjerto (mosaicoplastia) o aloinjerto en fresco ofrece la posibilidad de restaurar de manera inmediata la estructura histológica condral original. Sin embargo, el autoinjerto tiene el inconveniente de lesionar la zona sana donde se toma el injerto. Además, no posee la misma forma, densidad y espesor del tejido condral, ya que procede de zonas diferentes a la zona receptora.
El trasplante alogénico permite sustituir el cartílago articular y el hueso subcondral dañados por cartílago hialino maduro con condrocitos viables de la misma región anatómica junto con el hueso subcondral subyacente sano. También posibilita cubrir virtualmente todo tipo de defectos, restaurar superficies complejas y lesiones no contenidas(10,11,12,13,14,15,16,17,18,19). Asimismo, no produce morbilidad en la zona donante del paciente y provoca una mínima respuesta inmunológica en el receptor sin repercusión clínica(20). De este modo, el trasplante de aloinjerto osteocondral en fresco es una indicación válida para grandes defectos osteocondrales de rodilla(17,21). Esto es especialmente importante en pacientes jóvenes en los que han fallado las cirugías previas.
No obstante, el uso de aloinjertos osteocondrales en fresco plantea problemas desde el punto de vista logístico y médico. En nuestro medio, la obtención del injerto adecuado, tanto en morfología como en calidad del cartílago, es una de las mayores limitaciones de esta técnica quirúrgica. Otra es la programación de la cirugía; el periodo de viabilidad desde el momento de la obtención del donante está entre 2 y 4 semanas, dependiendo del método de procesamiento. Por otra parte, el tiempo de demora para disponer de los resultados de los controles de calidad (normalmente controles microbiológicos) del injerto es de 1 semana. Esto hace que el margen del que se dispone para llevar a cabo la cirugía sea de entre 1 y 3 semanas. A esta preocupación por la viabilidad celular del cartílago se añaden las referentes a la inmunogenicidad del injerto y la posibilidad de transmitir enfermedades infecciosas.
La presencia de condrocitos viables es esencial, puesto que son fundamentales para el mantenimiento de la matriz extracelular y para prevenir la degeneración del injerto con el paso del tiempo. De hecho, existe una correlación directa entre la viabilidad de los condrocitos y el éxito del trasplante osteocondral(19).
Los bancos de células y tejidos procesan y almacenan recursos terapéuticos para la reparación tisular, con el imperativo ético de poner a disposición de sus usuarios productos seguros, desde el punto de vista biológico, y clínicamente eficaces.
Fundamentalmente, el banco cuenta con 2 opciones de aloinjerto para su almacenamiento: congelación en fresco y criopreservación. La primera de las opciones es la más extendida en la conservación de tejidos en nuestro medio, pero produce la pérdida de vida celular, lo cual conlleva al fracaso de la conservación del tejido condral. Respecto a la criopreservación, en el tejido condral no se ha demostrado eficaz. La presencia de una matriz extracelular densa y consistente, y la falta de vascularización dificultan la penetración de las sustancias crioprotectoras. Como consecuencia, la viabilidad celular (salvo que se trate de fragmentos de apenas unos pocos mm3) que se consigue tras la descongelación es insuficiente para garantizar la eficacia clínica del aloinjerto.
Otra opción es la preservación en fresco. Precisamente las 2 características que dificultan una criopreservación satisfactoria (avascularidad y consistencia de la matriz), se presentan ahora como moduladoras o limitadoras frente a una eventual respuesta del sistema inmune del paciente receptor. De acuerdo con ello, se propone el almacenamiento en condiciones que permitan la disponibilidad del aloinjerto (con suficiente viabilidad celular), el tiempo suficiente para realizar los controles de calidad requeridos (fundamentalmente dirigidos a evitar el riesgo de transmisión de enfermedades), así como para programar la intervención quirúrgica. Es necesario que los bancos de tejidos realicen la validación del tiempo máximo de preservación en fresco para garantizar la viabilidad celular requerida para el éxito del implante.
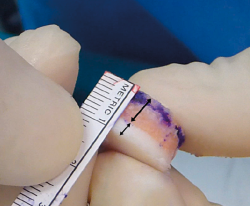
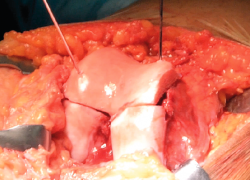
Al ser un injerto no vascularizado, los osteocitos del componente óseo del aloinjerto no sobreviven. En cambio, el tejido óseo permanece estructuralmente intacto y es mecánicamente resistente, de manera que actúa como soporte del cartílago hialino y de nexo de unión con el hueso del huésped. Con el tiempo, el hueso del huésped lo sustituirá mediante un fenómeno de creeping substitution(22,23). A la hora de utilizar aloinjertos, considerando que en las lesiones agudas la afectación del hueso subcondral suele ser escasa (salvo en caso de impactos de alta energía), es recomendable minimizar la fracción ósea del tejido (6-8 mm de espesor) (Figura 1). Así se disminuye el tiempo requerido para reemplazar el tejido óseo del donante por el del huésped y se consigue una incorporación completa del injerto óseo. En cualquier caso, puesto que los nutrientes llegan al cartílago articular tanto por difusión a través del fluido sinovial como desde el hueso esponjoso subyacente, hay que garantizar unas condiciones que faciliten la consolidación de la fracción ósea del injerto. En un modelo animal con babuinos Malinin y Ouellete(24) observaron el desarrollo de canales entre la capa más profunda del cartílago y el hueso subcondral, en autoinjertos, lo que sugiere que en la evolución clínica se generan vías para hacer llegar los nutrientes al injerto.
Desde el punto de vista inmunológico, no está claro si hay evidencia de una respuesta inmune que condicione la evolución del injerto. Los estudios realizados a este respecto han determinado la presencia de anticuerpos frente a colágeno(25), así como anticuerpos de clase I y de clase II(26), después del trasplante de tejido osteocondral criopreservado. Sin embargo, no hay datos que identifiquen inequívocamente los anticuerpos generados como específicos frente a antígenos HLA (human leukocyte antigen) del donante y también hay una necesidad de información sobre la respuesta al trasplante de tejido osteocondral fresco. Durante la cirugía, con el objetivo de reducir la presencia de estroma medular y, por tanto, su potencial carga antigénica, se realiza un exhaustivo lavado a presión del hueso(27).
Respecto al almacenamiento de tejido osteocondral viable, si bien la mayoría de los bancos que ofrecen este servicio utilizan una temperatura de 4 °C, se ha observado en modelo animal que se puede optimizar la viabilidad celular “cultivando” el tejido a 37 °C, ampliando además el tiempo efectivo de almacenamiento(28,29).
Para minimizar el riesgo de transmisión de enfermedades infecciosas lo máximo posible, además de la amplia formación que reciben los equipos de coordinación de trasplantes hospitalarios en España (responsables de la selección de los donantes), los bancos de tejidos siguen unos protocolos estrictos de cribado de los donantes mediante pruebas serológicas y procesamiento aséptico de las muestras. Además, la manipulación del tejido en el banco está regulada para minimizar el riesgo de contaminación medioambiental(30,31). Actualmente, gracias a la implementación de técnicas de enzimoinmunoanálisis (EIA) conjuntamente con el desarrollo de quimioluminoinmunoanálisis (MEIA y CMIA) por micropartículas y la detección de ácidos nucleicos (NAT), el riesgo de transmisión de enfermedades es extremadamente bajo.
De acuerdo con lo expuesto, los bancos deben trabajar en la implementación de protocolos dirigidos a optimizar su oferta asistencial: 1) desarrollando metodologías para ampliar el arsenal terapéutico, incorporando aloinjertos de tejido articular compuesto; 2) adecuando las condiciones de almacenamiento para una mejor preservación de la viabilidad celular; 3) adaptando la temperatura de incubación para permitir una preservación prolongada de la viabilidad celular manteniendo las propiedades de la matriz extracelular; 4) elaborando medios de cultivo específicos; y 5) incrementando la presión hidrostática. De este modo, se facilita la difusión de los nutrientes del medio de cultivo y, paralelamente, se pretende mimetizar el efecto biomecánico del movimiento, que también tiene un papel importante en la viabilidad y la funcionalidad celular(32).
Indicaciones y contraindicaciones
Indicaciones
- Pacientes jóvenes (menores de 50 años) que no son candidatos a sustitución protésica.
- Lesiones de grado III y IV localizadas, ya sean unipolares o bipolares.
- Manejo primario de lesiones condrales u osteocondrales mayores de 2 cm independientemente de que sean contenidas o no contenidas.
- Osteocondritis disecante (OCD).
- Osteonecrosis espontánea de rodilla.
- Grandes lesiones osteocondrales postraumáticas.
- Revisión de cirugías fallidas de reparación condral.
Contraindicaciones
- Índice de masa corporal (IMC) > 30 kg/m2.
- Cuadros degenerativos tricompartimentales.
- Enfermedades inflamatorias sistémicas, presencia de infección o antecedente de infección osteomielítica en la zona receptora del injerto, y neoplasia activa.
- Condiciones médicas que pudieran afectar a la incorporación del injerto, como la diabetes insulinodependiente o el tabaquismo.
Aspectos técnicos
Cuando se plantea un trasplante de aloinjerto osteocondral en fresco, lo primero que se debe hacer es elegir una pieza donante del tamaño, el lado y la forma similares a los del área afectada del receptor. Esto es especialmente importante en la articulación femoropatelar y en la meseta tibial. Para ello, podemos valernos de radiografías en proyecciones anteroposterior y lateral en carga y de Merchant(33). Más precisa es la tomografía computarizada preoperatoria, porque además es útil para determinar la afectación del hueso subcondral. Una vez obtenemos las medidas del injerto que se necesita, se remiten al responsable del banco de tejidos para localizar así al donante ideal. Asimismo, el banco de tejidos debe ofrecer información detallada sobre las dimensiones del aloinjerto (si fuera posible, realizando una tomografía computarizada del mismo) para facilitar la evaluación de su idoneidad (especialmente en casos de afectación de la rótula o la tróclea femoral).
Al igual que en otros procedimientos de reparación condral, es importante reconocer las condiciones de desalineamiento axial y coronal, ausencia meniscal o inestabilidad ligamentosa. Estos factores deben ser evaluados y tratados de forma adecuada. En la misma intervención, se puede realizar el trasplante de aloinjerto osteocondral en fresco con una reconstrucción ligamentosa, trasplante meniscal y/u osteotomías correctoras(34).
Las lesiones del menisco son una contraindicación relativa o al menos un factor a resolver de forma asociada, pues este desempeña un papel fundamental en la absorción y la distribución de cargas sobre la superficie articular. Por ello, se debe reparar las lesiones periféricas y, en los casos con deficiencias considerables, realizar un trasplante meniscal que mejore la supervivencia del aloinjerto osteocondral.
Se ha de valorar la malalineación por medio de radiografías en carga del miembro. Si el eje mecánico pasa por el compartimento afecto, se asociará una osteotomía correctiva para descargar y proteger el aloinjerto. Se debe ser especialmente riguroso en las osteotomías descompresivas, incluso las desviaciones de tan solo 2-3° pueden ser merecedoras de correcciones durante el mismo acto quirúrgico. Generalmente, se prefieren osteotomías de apertura cuando se realizan técnicas de aloinjerto en cilindros. Por el contrario, las osteotomías de cierre se reservan para aloinjertos en concha o masivos. Se recomienda, en la medida de lo posible, efectuar la osteotomía en el hueso contrario de la articulación a la lesión para minimizar los procedimientos quirúrgicos en el mismo hueso (osteotomía medial de cierre femoral distal y OCA de platillo lateral para lesiones osteocondrales de platillo externo asociadas a genu valgo marcado).
Cuando se efectúe un trasplante de aloinjerto osteocondral en fresco femoropatelar se deberá descartar el maltracking, ya que puede ser una causa subyacente de fracaso del aloinjerto. En estos casos, se pueden asociar técnicas sobre partes blandas, como la liberación o el alargamiento del retináculo lateral, la reconstrucción del ligamento femoropatelar medial, trocleoplastias o realineaciones óseas(35).
La inestabilidad rotacional y la traslacional pueden dañar el injerto debido a las fuerzas de cizallamiento que ejercen sobre este. En estos casos, se realizarán técnicas de reconstrucción/reparación ligamentosa.
Idealmente, la intervención quirúrgica debe ser realizada por 2 equipos quirúrgicos que trabajen simultáneamente. Uno se encargaría de la preparación del injerto y el otro de la artrotomía, la preparación de la zona receptora y el implante del injerto. Se administra la profilaxis antibiótica intravenosa según el protocolo habitual y se realiza una anestesia general o raquianestesia. Se posiciona al paciente en decúbito supino en la mesa quirúrgica con el manguito de isquemia en el muslo proximal.
Antes de la artrotomía, la artroscopia diagnóstica caracteriza mejor la lesión y asegura un correcto abordaje. Las opciones de acceso a la zona lesionada dependen de la zona afecta y de las preferencias del cirujano. La más habitual incisión recta sobre la línea media para después abordar la articulación a través de una artrotomía parapatelar medial o lateral, se puede alternar con una incisión parapatelar y artrotomía lateral si la lesión solo interesa a la tróclea o a la rótula. En casos de lesiones femorotibiales, lógicamente se debe adaptar a cada caso, siendo lo más habitual incisiones longitudinales anterolaterales o anteromediales, dependiendo del caso. Al tratar lesiones patelares, es aconsejable no retirar demasiada grasa de Hoffa para evitar la desvascularización de la rótula, como así también realizar una denervación rotuliana proximal, medial y lateral a dicho hueso.
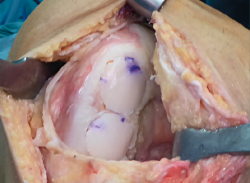
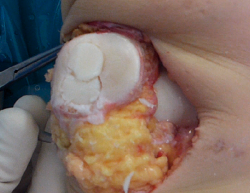
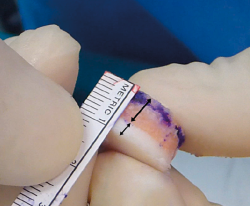
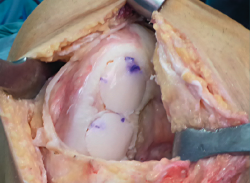
Las técnicas mediante aloinjertos en cilindros (dowel o plug en la literatura anglosajona) o en concha (shell) son las más empleadas. En defectos solitarios, bien delimitados y fácilmente accesibles como en el cóndilo femoral medial se utilizan aloinjertos en cilindro. El diámetro de este se puede adaptar de forma precisa al tamaño de la lesión, proporcionando una cobertura completa del área afecta y una integración estable con el hueso del huésped y las superficies cartilaginosas circundantes. En lesiones grandes o múltiples en las que un cilindro no consigue cubrir todo el defecto, en especial si la longitud de la lesión es mayor que la anchura, se puede optar por una configuración de “muñeco de nieve” (Figura 2) o “mastercard” (Figura 3) de los cilindros, aunque la misma ha reportado mayores tasas de revisión(36).
Cuando se trate de lesiones asimétricas (patela completa o lesiones amplias de la tróclea) o en localizaciones de difícil acceso, se utiliza la técnica en concha.
Aloinjerto en cilindros en el fémur
Tras exponer la lesión, se deben identificar las paredes del cartílago sano. Después, se determina el tamaño de la lesión por medio de las plantillas de medición que se encuentran disponibles en el instrumental de trasplante del aloinjerto.
Una vez determinado el tamaño, se posiciona una aguja de Kirschner en el centro de la lesión y perpendicular a su superficie. Mediante una fresa circular del tamaño elegido se profundiza unos 6-8 mm, sin sobrepasar los 10 mm. Si la profundidad de la lesión subcondral, tras desbridar hasta hueso sano, es mayor de 8-10 mm, se debe rellenar con injerto de hueso autólogo (cresta ilíaca o tibia proximal) hasta conseguir una profundidad ideal de 6-8 mm. Con el lecho receptor preparado, se mide la profundidad en las posiciones del reloj de las 12, las 3, las 6 y las 9.
En la mesa de preparación del injerto, se extrae con una trefina del mismo tamaño un cilindro del aloinjerto en fresco proporcionado por el banco de tejidos. El exceso de hueso subcondral se retira y se marca la posición de las 12 para una correcta orientación. Para eliminar los restos de médula del hueso subcondral se irriga con al menos 6 litros de solución fisiológica mediante lavado pulsátil. Este paso se realiza en cada una de las piezas antes de implantar el injerto en la zona receptora.
El cirujano responsable de preparar el aloinjerto es el encargado en transferirlo a la zona lesionada. Si el injerto cae al suelo, se recomienda un nuevo proceso de lavado de al menos 20 minutos y la inmersión en una solución de vancomicina de 1 g/100 mL, durante 10 minutos.
Se implanta el injerto a presión, de manera suave, con el pulgar o un impactador adecuado. Normalmente, no es necesaria la fijación, pero se pueden utilizar pines o tornillos biorreabsorbibles si esta es insuficiente. Para confirmar la estabilidad del injerto o zonas de pinzamiento se moviliza la rodilla en todo su rango de movilidad.
Aloinjerto en concha en el fémur
Tras identificar la lesión condilar se prepara la zona receptora. Debe tener una profundidad de 4-5 mm y una superficie plana. Es necesario retirar el tejido óseo necrótico o dañado.
Se esboza el injerto en una plantilla de papel, ligeramente sobredimensionado respecto al área del receptor. Se realiza el corte a mano alzada y se ajusta gradualmente con una pinza gubia hasta que coincida con el tamaño definitivo. Temporalmente se fija con agujas de Kirschner y se descartan las posibles zonas de pinzamiento a lo largo de todo el rango de movilidad. La fijación definitiva se realiza por medio de pines biorreabsorbibles o tornillos a compresión.
Aloinjerto de patela
La técnica en concha es la indicada en lesiones osteocondrales patelares extensas. La técnica quirúrgica es idéntica a la empleada en cirugía protésica cuando se va a colocar un implante rotuliano. Tras medir la superficie y el grosor patelares, se realiza un plano de corte paralelo al que pasa a través de los tendones rotuliano y cuadricipital, utilizando el instrumental de la prótesis de rodilla y una sierra oscilante. Para minimizar el riesgo de fractura, se debe mantener un espesor entre 12 y 15 mm. Sistemáticamente, se denerva la rótula con el electrocoagulador, con la idea teórica de disminuir la incidencia postoperatoria de dolor anterior de rodilla.
Se prepara el aloinjerto usando también el instrumental de la prótesis de rodilla; el espesor de este será el que una vez implantado consiga obtener un grosor de rótula igual que el original. Si el tamaño del injerto es un poco más grande, cosa que a veces ocurre, se recorta para ajustarlo al tamaño del receptor. Se marca en el implante la parte proximal y lateral, de manera que la posición del injerto sea la adecuada cuando se transfiera a la zona receptora.
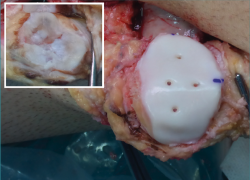
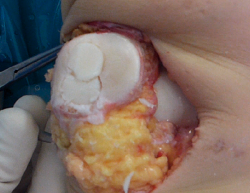
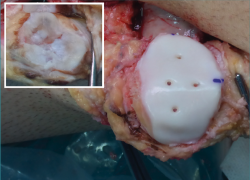
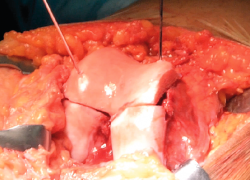
La fijación provisional se lleva a cabo mediante 2 agujas de Kirschner introducidas a través de la cortical anterior de la rótula y se comprueba el tracking y la congruencia articular. La fijación definitiva se realiza con 3 o 4 tornillos de compresión desde la cara dorsal de la rótula o preferentemente pines biorreabsorbibles desde la cara articular (Figura 4) que permitirán postoperatoriamente la evaluación del tejido osteocondral por resonancia magnética(23).
Aloinjerto de meseta tibial
Se suele indicar en secuelas de fracturas del platillo tibial medial o lateral.
Se corta con una sierra oscilante 1-2 cm de profundidad del platillo en función del tamaño del defecto. El corte debe ser perpendicular al eje de la tibia, manteniendo la pendiente posterior y conservando la alineación coronal y sagital. Se preservan la eminencia tibial y la raíz del menisco contralateral en el corte sagital. Se retira el menisco del compartimento afecto respetando el muro donde se suturará el aloinjerto meniscal.
Tras preparar en tamaño y forma el aloinjerto osteocondral tibial, se fija temporalmente mediante agujas de Kirschner y se valora la estabilidad durante todo el rango de movimiento. La fijación definitiva se consigue con 2 o 3 tornillos de esponjosa de 3,5 mm de diámetro y posteriormente se sutura el aloinjerto de menisco sobre el muro meniscal residual(37).
Aloinjerto de tróclea femoral
Tal como hemos comentado, en defectos pequeños se utiliza la técnica mediante 1 o 2 cilindros. Al igual que en las lesiones centrales de la rótula, la preparación del lecho receptor y la extracción de los cilindros de aloinjerto pueden verse dificultadas al no lograr una alineación perfecta de la plantilla de corte circular en las zonas trocleares centrales debido al doble contorno articular.
Cuando son lesiones más grandes, defectos bipolares o defectos que afectan prácticamente a la totalidad de la tróclea y especialmente en trócleas displásicas, se opta por el aloinjerto en concha. Es crucial elegir un aloinjerto de tróclea de tamaño, lado del receptor y forma adecuados. La resección de la tróclea del receptor se hará de manera similar al corte anterior del fémur distal que se realiza cuando se implanta una prótesis de rodilla o preferentemente utilizando 3 o 4 agujas de Kirschner que sirvan de guía orientadas 45° respecto al plano coronal, lo que permitirá avanzar hacia la zona intercondílea de forma más eficiente (Figura 5). Una vez implantado provisionalmente el injerto y comprobados el tracking y la congruencia articular, se fija con 2 tornillos mediales y 2 laterales, o con pines reabsorbibles.
Resultados. Revisión bibliográfica. Evidencia científica
Aunque no hay evidencia basada en ensayos controlados aleatorizados respecto al trasplante de aloinjerto osteocondral en fresco, se dispone de numerosos estudios a corto, medio y largo plazo, pues esta técnica se ha utilizado desde hace casi 50 años. Muchos de ellos con tasas de supervivencia altas y con resultados funcionales y de satisfacción buenos y/o excelentes. Y en otros recientes, con una recuperación de la actividad previa a su lesión cercana al 80%(38,39,40).
La serie retrospectiva de trasplantes de aloinjerto osteocondral en fresco de cóndilo femoral más grande publicada (129 rodillas) presenta una supervivencia del 82% a los 10 años, del 74% a los 15 años y del 66% a los 20 años(17). En ella, se determinaron como factores de riesgo del fracaso del injerto la edad mayor de 30 años y haber sido sometido a 2 o más cirugías previas. Estos resultados de supervivencia son similares a otras series publicadas con anterioridad(16,41).
Por otra parte, la serie con mayor seguimiento registrado(42), con una media de 21,8 años, obtuvo una supervivencia del 91% a los 10 años, del 84% a los 15 años, del 69% a los 20 años y se estimó que a los 25 sería del 59%. En ella, el 90% de los pacientes tenían menos de 40 años y un nivel alto de demanda de actividad física.
En cambio, se dispone de menos información publicada en lesiones osteocondrales del platillo tibial, porque las lesiones en esta localización, que, además, son susceptibles de tratar con esta técnica, son menos frecuentes. Shasha et al.(43), con un seguimiento medio de 12 años, obtuvieron una supervivencia del 80% a los 10 años y del 65% a los 15 años. Resultados similares a los de Gross et al.(16), donde, además, destaca la reconversión a prótesis de un tercio de los aloinjertos por fracaso de este aproximadamente a los 10 años.
La osteonecrosis espontánea de rodilla es una osteonecrosis focal del cóndilo femoral medial de la rodilla que puede progresar a artrosis severa de la articulación femorotibial medial. Es una entidad diferente de la osteonecrosis secundaria a alcoholismo, uso crónico de corticoides o enfermedades sistémicas. En los estadios iniciales responde, la mayoría de las veces, al tratamiento conservador. En cambio, las lesiones de estadios avanzados o defectos osteocondrales mayores del 40% del ancho condíleo tienen un pronóstico desfavorable y evolucionan hacia artrosis(44). El trasplante de aloinjerto osteocondral en fresco se ha utilizado en lesiones grandes y también tras cirugías fallidas(45). Tirico et al.(46) presentaron 7 pacientes con lesiones en estadio 2 y 3 del cóndilo medial femoral con un tamaño medio de la lesión de 4,6 cm2 y una mediana del porcentaje entre el tamaño de la lesión y la anchura del cóndilo del 56,8%. Tras 7 años de seguimiento, no hubo ningún fallo del injerto.
La OCD que no mejora con tratamiento conservador puede ser un problema de difícil abordaje clínico, sobre todo en esqueletos maduros y en grandes y/o inestables fragmentos osteocondrales. A pesar de que existen distintas opciones terapéuticas para tratar las lesiones condrales, es difícil compararlas debido a las diferencias entre poblaciones de pacientes. Se ha visto(47,48,49) que la utilización del trasplante de aloinjerto osteocondral en fresco en esta patología obtiene buenos resultados funcionales y tasas de supervivencia elevadas. La supervivencia a largo plazo (93% a los 10 años) y los resultados funcionales son excelentes a pesar de ser una técnica de salvamento y de tratar lesiones que representan el peor escenario posible (gran tamaño, estadios II y III, y fallo de cirugías previas)(50). Por ello, aunque no hay un consenso sobre cuál es el tratamiento más adecuado, el trasplante de aloinjerto osteocondral en fresco es una opción de tratamiento válida, con la ventaja añadida de restaurar tanto el defecto condral como óseo.
Las lesiones condrales bipolares de la articulación femorotibial, se asocien o no a afectación ósea, pueden ser consideradas una contraindicación relativa debido al éxito limitado de los resultados clínicos(51) y al considerable porcentaje de fracasos. Esto es más evidente si se compara con los trasplantes monopolares realizados en cóndilo femoral(52,53,54,55). Una de las causas de fracaso y en consecuencia de resultados más pobres puede ser la progresión de la enfermedad del cartílago(56,57).
Por otra parte, se ha demostrado la relación entre el tamaño del aloinjerto y el fracaso del trasplante en este tipo de lesiones(58). De esta manera, se puede suponer que grandes lesiones bipolares osteocondrales pueden indicar estadios avanzados de degeneración condral. Esto hace que se deba de ser más cauto cuando se indique el trasplante de aloinjerto osteocondral en fresco en grandes defectos osteocondrales bipolares. Sin embargo, los resultados clínicos, tanto subjetivos como objetivos, relativamente buenos de los pacientes con aloinjertos bipolares que sobreviven incitan al uso de este procedimiento cuando la edad y el nivel de actividad hacen inadecuada la artroplastia. De esta forma, aunque los resultados son inferiores a las lesiones monopolares, el trasplante de aloinjerto osteocondral en fresco se puede considerar como una opción de tratamiento biológico potencial para pacientes con lesiones bipolares del cartílago de la rodilla.
Las lesiones del cartílago femoropatelar plantean un problema de difícil manejo terapéutico y tal como refiere una revisión sistemática reciente (nivel IV de evidencia científica)(59): “no se puede establecer un procedimiento quirúrgico ideal para lesiones ≥ 4 cm2 en pacientes menores de 50 años”. En pacientes jóvenes se debe limitar la implantación de las prótesis femoropatelares por el riesgo de desgaste y aflojamiento. Si estos pacientes presentaran lesiones profundas y extensas, podría plantearse el empleo de aloinjertos osteocondrales masivos en fresco. Sin embargo, hay pocos trabajos publicados sobre el uso de aloinjertos osteocondrales masivos en fresco en la articulación femoropatelar y la mayoría son series clínicas(35,51,56,60,61).
Debido a la anatomía del surco troclear, el trasplante en dicha localización es técnicamente más exigente que en la articulación tibiofemoral. De hecho, la orientación del injerto en el plano coronal es más crítica que en defectos de tamaño similar en la articulación tibiofemoral(62). Esto puede explicar las tasas de revisiones del aloinjerto en la mayoría de estas series(35,51,56,60). Sin embargo, estudios más recientes muestran resultados muy consistentes a largo plazo que son equiparables a otros procedimientos de reparación condral y deberían alentar al uso del trasplante de aloinjerto para la articulación femoropatelar. Gracitelli et al.(35) presentaron una supervivencia del 78,1% a los 10 años y del 55,8% a los 15, mientras que en la serie de Cameron et al.(61) la supervivencia fue del 100% a los 5 años y del 91,7% a los 10 años para defectos aislados de tróclea.
Tal como hemos apuntado, las lesiones femorotibiales bipolares tienen resultados inferiores, con un incremento de la tasa de fracaso si se compara con defectos monopolares. En el caso de la articulación femoropatelar, no parece que sea así, ya que, al agrupar el número de fracasos de los aloinjertos monopolares en esta localización y el de los bipolares, los porcentajes de fracaso son similares(35,51,56,60). Todo esto otorga al trasplante de aloinjerto osteocondral en fresco un papel importante en defectos osteocondrales profundos, bipolares y/o procedimientos de revisión de la articulación femoropatelar.
Un punto clave para evitar el fracaso del aloinjerto es reconocer las posibles causas de desalineamiento axial, fallo meniscal o inestabilidad ligamentosa. Se ha descrito que la alineación de la rodilla y el estrechamiento del espacio articular mayor del 50% guardan relación con el fallo del aloinjerto(52). Asimismo, los injertos implantados en compartimentos sometidos a mayores fuerzas compresivas presentan histológicamente un retraso de la revascularización y del creeping substitution, junto a una pérdida de cartílago articular(22). Por ello, es clave evaluar la desalineación en las radiografías preoperatorias en carga con el fin de proteger los aloinjertos mediante una osteotomía de realineación(43,63), incluso ante pequeñas desviaciones angulares del orden de 2 o 3°. De hecho, una osteotomía concomitante al trasplante del aloinjerto ofrece mejores resultados frente a los casos en los que la osteotomía se realiza antes o después del trasplante(16). Se han observado resultados similares en trasplantes de aloinjerto osteocondral de platillo tibial que se asociaron a osteotomías varizantes de fémur distal(64). Por otra parte, aunque pueda existir un riesgo teórico que comprometa el aporte vascular al hueso que rodea el injerto y, por tanto, que afecte a su integración, no se dispone de datos que establezcan una relación clara que lo corrobore(65).
De la misma manera, si hay evidencia de subluxación o carga asimétrica de la faceta patelar lateral, inestabilidad femoropatelar o principio de artritis femoropatelar, debería combinarse el aloinjerto osteocondral fresco con un procedimiento de reconstrucción del ligamento patelofemoral medial o una realineación femoropatelar(56,62).
Conclusión
El trasplante de aloinjerto osteocondral en fresco es un procedimiento útil en grandes defectos osteocondrales de la rodilla en pacientes jóvenes y activos en los que se prevé que no van a responder bien a una sustitución protésica. Con las técnicas de procesamiento actuales se asegura una viabilidad alta de condrocitos combinada con un riesgo de transmisión de enfermedades despreciable. La selección del paciente, así como el estudio de las condiciones de malalineación, estabilidad ligamentosa y déficit meniscal, son primordiales para asegurar la supervivencia del injerto. Los aloinjertos sobre defectos femorales tienen excelentes resultados a medio y largo plazo, mientras que son factores que alteran el pronóstico las lesiones crónicas, bipolares, la afectación de la articulación femoropatelar y la mayor edad.
Figuras
Figura 4. Fijación definitiva de aloinjerto osteocondral en concha de rótula mediante pines biorreabsorbibles.
Información del artículo
Cita bibliográfica
Autores
Alejandro Roselló-Añón
Servicio de Cirugía Ortopédica y Traumatología. Hospital Arnau de Vilanova. Valencia
Vicente Mirabet Lis
Banco de Células y Tejidos. Centro de Transfusión de Valencia
Óscar Fariñas Barbera
Vall d'Hebron Institut de Recerca (VHIR). Barcelona
Banc de Sang i Teixits. Instituto de Investigación Biomédica Sant Pau. Barcelona
Departamento de Anatomía y Embriología Humana Prof. D. Ruano Gil. Facultad de Medicina. Universidad de Barcelona
Pablo Eduardo Gelber Ghertner
Departamento de Cirugía Ortopédica. Hospital de la Santa Creu i Sant Pau. Universitat Autonoma de Barcelona (UAB). Barcelona
ReSport Clinic, Barcelona
Unidad de Artroscopia y Rodilla. ICATME-Institut Universitari Dexeus.
Vicente Sanchís Alfonso
Servicio de Traumatología y Cirugía Ortopédica. Hospital Arnau de Vilanova. Valencia
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de intereses.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Flanigan DC, Harris JD, Trinh TQ, Siston RA, Brophy RH. Prevalence of chondral defects in athletes’ knees: a systematic review. Med Sci Sports Exerc. 2010;42(10):1795-801.
-
2Mankin HJ. The response of articular cartilage to mechanical injury. J Bone Joint Surg Am. 1982;64(3):460-6.
-
3Curl WW, Krome J, Gordon ES, Rushing J, Smith BP, Poehling GG. Cartilage injuries: a review of 31,516 knee arthroscopies. Arthroscopy. 1997;13(4):456-60.
-
4Hjelle K, Solheim E, Strand T, Muri R, Brittberg M. Articular cartilage defects in 1,000 knee arthroscopies. Arthroscopy. 2002;18(7):730-4.
-
5Arøen A, Løken S, Heir S, Alvik E, Ekeland A, Granlund OG, Engebretsen L. Articular cartilage lesions in 993 consecutive knee arthroscopies. Am J Sports Med. 2004 Jan-Feb;32(1):211-5.
-
6Widuchowski W, Widuchowski J, Trzaska T. Articular cartilage defects: study of 25,124 knee arthroscopies. Knee. 2007;14(3):177-82.
-
7Heir S, Nerhus TK, Røtterud JH, Løken S, Ekeland A, Engebretsen L, Arøen A. Focal cartilage defects in the knee impair quality of life as much as severe osteoarthritis: a comparison of knee injury and osteoarthritis outcome score in 4 patient categories scheduled for knee surgery. Am J Sports Med. 2010 Feb;38(2):231-7.
-
8Lonner JH, Hershman S, Mont M, Lotke PA. Total knee arthroplasty in patients 40 years of age and younger with osteoarthritis. Clin Orthop Relat Res. 2000;380:85-90.
-
9Bayliss LE, Culliford D, Monk AP, Glyn-Jones S, Prieto-Alhambra D, Judge A, et al. The effect of patient age at intervention on risk of implant revision after total replacement of the hip or knee: a population-based cohort study. Lancet. 2017 Apr 8;389(10077):1424-30.
-
10Assenmacher AT, Pareek A, Reardon PJ, Macalena JA, Stuart MJ, Krych AJ. Long-term outcomes after osteochondral allograft: a systematic review at long-term follow-up of 12.3 years. Arthroscopy. 2016;32(10):2160-8.
-
11Capeci CM, Turchiano M, Strauss EJ, Youm T. Osteochondral allografts: applications in treating articular cartilage defects in the knee. Bull Hosp Jt Dis (2013). 2013;71(1):60-7.
-
12Chahal J, Gross AE, Gross C, Mall N, Dwyer T, Chahal A, et al. Outcomes of osteochondral allograft transplantation in the knee. Arthroscopy. 2013;29(03):575-88.
-
13Chui K, Jeys L, Snow M. Knee salvage procedures: the indications, techniques and outcomes of large osteochondral allografts. World J Orthop. 2015;6(03):340-50.
-
14De Caro F, Bisicchia S, Amendola A, Ding L. Large fresh osteochondral allografts of the knee: a systematic clinical and basic science review of the literature. Arthroscopy. 2015;31(04):757-65.
-
15Görtz S, De Young AJ, Bugbee WD. Fresh osteochondral allografting for steroid-associated osteonecrosis of the femoral condyles. Clin Orthop Relat Res. 2010;468(05):1269-78.
-
16Gross AE, Shasha N, Aubin P. Long-term followup of the use of fresh osteochondral allografts for posttraumatic knee defects. Clin Orthop Relat Res. 2005;(435):79-87.
-
17Levy YD, Görtz S, Pulido PA, McCauley JC, Bugbee WD. Do fresh osteochondral allografts successfully treat femoral condyle lesions? Clin Orthop Relat Res. 2013;471(01):231-7.
-
18McCulloch PC, Kang RW, Sobhy MH, Hayden JK, Cole BJ. Prospective evaluation of prolonged fresh osteochondral allograft transplantation of the femoral condyle: minimum2-year followup. Am J Sports Med. 2007;35(03):411-20.
-
19Sherman SL, Garrity J, Bauer K, Cook J, Stannard J, Bugbee W. Fresh osteochondral allograft transplantation for the knee: current concepts. J Am Acad Orthop Surg. 2014;22(02):121-33.
-
20Hunt HE, Sadr K, Deyoung AJ, Gortz S, Bugbee WD. The role of immunologic response in fresh osteochondral allografting of the knee. Am J Sports Med. 2014;42(4):886-91.
-
21Williams RJ 3rd, Ranawat AS, Potter HG, Carter T, Warren RF. Fresh stored allografts for the treatment of osteochondral defects of the knee. J Bone Joint Surg Am. 2007;89(4):718-26.
-
22Oakeshott RD, Farine I, Pritzker KP, Langer F , Gross AE. A clinical and histologic analysis of failed fresh osteochondral allografts. Clin Orthop Relat Res. 1988;233:283-94.
-
23Gelber PE, Perelli S, Ibáñez M, Ramírez-Bermejo E, Fariñas O, Monllau JC, Sanchís-Alfonso V. Fresh Osteochondral Patellar Allograft Resurfacing. Arthrosc Tech. 2018;7(6):e617-e622.
-
24Malinin T, Ouellette EA. Articular cartilage nutrition is mediated by subchondral bone: a long-term autograft study in baboons. Osteoarthritis Cartilage. 2000;8(6):483-91.
-
25Bujia J, Alsalameh S, Naumann A, Wilmes E, Sittinger M, Burmester GR. Humoral immune response against minor collagens type IX and XI in patients with cartilage graft resorption after reconstructive surgery. Ann Rheum Dis. 1994;53:229-34.
-
26Friedlaender GE, Strong DM, Tomford WW, Mankin HJ. Long-term follow-up of patients with osteochondral allografts. A correlation between immunologic responses and clinical outcome. Orthop Clin North Am. 1999 Oct;30(4):583-8.
-
27Sun Y, Jiang W, Cory E, Caffrey JP, Hsu FH, Chen AC, et al. Pulsed lavage cleansing of osteochondral grafts depends on lavage duration, flow intensity, and graft storage condition. PLoS One. 2017;12(5):e0176934.
-
28Pallante AL, Bae WC, Chen AC, Görtz S, Bugbee WD, Sah RL. Chondrocyte viability is higher after prolonged storage at 37 degrees C than at 4 degrees C for osteochondral grafts. Am J Sports Med. 2009;37(Suppl 1):24S-32S.
-
29Garrity JT, Stoker AM, Sims HJ, Cook JL. Improved osteochondral allograft preservation using serum-free media at body temperature. Am J Sports Med. 2012 Nov;40(11):2542-8.
-
30Caselli-Fernández LM, Terkola R. Clean room environment, personnel, quality assurance and their monitoring. Eur J Hosp Pharm. 2006;12:29-34.
-
31Real Decreto-Ley 9/2014, por el que se establecen las normas de calidad y seguridad para la donación, la obtención, la evaluación, el procesamiento, la preservación, el almacenamiento y la distribución de células y tejidos humanos, y se aprueban las normas de coordinación y funcionamiento para su uso en humanos. BOE n.° 163: 52716-63. Año 2014.
-
32Reinold MM, Wilk KE, Macrina LC, Dugas JR, Cain EL. Current concepts in the rehabilitation following articular cartilage repair procedures in the knee. J Orthop Sports Phys Ther. 2006;36:774-94.
-
33Pisanu G, Cottino U, Rosso F, Blonna D, Marmotti AG, Bertolo C, et al. Large Osteochondral Allografts of the Knee: Surgical Technique and Indications. Joints. 2018 Mar 13;6(1):42-53.
-
34Alford JW, Cole BJ. Cartilage restoration, Part 1: Basic science, historical perspective, patient evaluation, and treatment options. Am J Sports Med. 2005;33:295-306.
-
35Gracitelli GC, Meric G, Pulido PA, Görtz S, De Young AJ, Bugbee WD. Fresh osteochondral allograft transplantation for isolated patellar cartilage injury. Am J Sports Med. 2015;43(04):879-84.
-
36Familiari F, Cinque ME, Chahla J, Godin JA, Olesen ML, Moatshe G, LaPrade RF. Clinical Outcomes and Failure Rates of Osteochondral Allograft Transplantation in the Knee: A Systematic Review. Am J Sports Med. 2018 Dec;46(14):3541-9.
-
37Gelber PE, Erquicia J, Ramírez E, Fariñas O, Monllau JC. Fresh osteochondral and meniscus allografting for posttraumatic tibial plateau defects. Arthrosc Tech. 2018;7:e661-e667.
-
38Krych AJ, Pareek A, King AH, Johnson NR, Stuart MJ, Williams RJ III. Return to sport after the surgical management of articular cartilage lesions in the knee: a meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2017;25(10):3186-96.
-
39Nielsen ES, McCauley JC, Pulido PA, Bugbee WD. Return to sport and recreational activity after osteochondral allograft transplantation in the knee. Am J Sports Med. 2017;45(07): 1608-14.
-
40McCarthy MA, Meyer MA, Weber AE, Levy DM, Tilton AK, Yanke AB, Cole BJ. Can Competitive Athletes Return to High-Level Play After Osteochondral Allograft Transplantation of the Knee? Arthroscopy. 2017 Sep;33(9):1712-7.
-
41Aubin PP, Cheah HK, Davis AM, Gross AE. Long-term followup of fresh femoral osteochondral allografts for posttraumatic knee defects. Clin Orthop Relat Res. 2001;(391 Suppl):S318-S327.
-
42Raz G, Safir OA, Backstein DJ, Lee PT, Gross AE. Distal Femoral Fresh Osteochondral Allografts: Follow-up at a Mean of Twenty-two Years. J Bone Joint Surg Am. 2014 Jul 2;96(13):1101-7.
-
43Shasha N, Krywulak S, Backstein D, Pressman A, Gross AE. Long-term follow-up of fresh tibial osteochondral allografts for failed tibial plateau fractures. J Bone Joint Surg Am. 2003;85-A(suppl 2):33-9.
-
44Aglietti P, Insall JN, Buzzi R, Deschamps G. Idiopathic osteonecrosis of the knee: aetiology, prognosis and treatment. J Bone Joint Surg Br. 1983;65(5):588-97.
-
45Bugbee W, Cavallo M, Giannini S. Osteochondral allograft transplantation in the knee. J Knee Surg. 2012;25(2):109-16.
-
46Tírico LEP, Early SA, McCauley JC, Bugbee WD. Fresh Osteochondral Allograft Transplantation for Spontaneous Osteonecrosis of the Knee: A Case Series. Orthop J Sports Med. 2017 Oct 3;5(10):2325967117730540.
-
47Garrett JC. Fresh osteochondral allografts for treatment of articular defects in osteochondrtitis dissecans of the lateral femoral condyle in adults. Clin Orthop Relat Res. 1994;(303):33-7.
-
48Emmerson BC, Gortz S, Jamali AA, Chung C, Amiel D, Bugbee WD. Fresh osteochondral allografting in the treatment of osteochondritis dissecans of the femoral condyle. Am J Sports Med. 2007;35(6):907-14.
-
49Lyon R, Nissen C, Liu XC, Curtin B. Can fresh osteochondral allografts restore function in juveniles with osteochondritis dissecans of the knee? Clin Orthop Relat Res. 2013;471(4):1166-73.
-
50Sadr KN, Pulido PA, McCauley JC, Bugbee WD. Osteochondral Allograft Transplantation in Patients With Osteochondritis Dissecans of the Knee. Am J Sports Med. 2016 Nov;44(11):2870-5.
-
51Chu CR, Convery FR, Akeson WH, Meyers M, Amiel D. Articular cartilage transplantation: clinical results in the knee. Clin Orthop Relat Res. 1999;360:159-68.
-
52Ghazavi MT, Pritzker KP, Davis AM, Gross AE. Fresh osteochondral allografts for post-traumatic osteochondral defects of the knee. J Bone Joint Surg Br. 1997 Nov;79(6):1008-13.
-
53Convery F, Akeson W, Meyers M. The operative technique of fresh osteochondral allografting of the knee. Opin Tech Orthop. 1997;7:340-4.
-
54Bugbee WD, Convery FR. Osteochondral allograft transplantation. Clin Sports Med. 1999 Jan;18(1):67-75.
-
55Bugbee WD. Fresh osteochondral allografts. J Knee Surg. 2002;15(3):191-5.
-
56Jamali AA, Emmerson BC, Chung C, Convery FR, Bugbee WD. Fresh osteochondral allografts: results in the patellofemoral joint. Clin Orthop Relat Res. 2005;437:176-85.
-
57Horton MT, Pulido PA, McCauley JC, Bugbee WD. Revision osteochondral allograft transplantations: do they work? Am J Sports Med. 2013 Nov;41(11):2507-11.
-
58Meric G, Gracitelli GC, Görtz S, De Young AJ, Bugbee WD. Fresh osteochondral allograft transplantation for bipolar reciprocal osteochondral lesions of the knee. Am J Sports Med. 2015 Mar;43(3):709-14.
-
59Noyes FR, Barber-Westin SD. Advanced patellofemoral cartilage lesions in patients younger than 50 years of age: is there an ideal operative option? Arthroscopy. 2013;29:1423-36.
-
60Torga Spak R, Teitge RA. Fresh osteochondral allografts for patellofemoral arthritis: long-term followup. Clin Orthop Relat Res. 2006;444:193-200.
-
61Cameron JI, Pulido PA, McCauley JC, Bugbee WD. Osteochondral allograft transplantation of the femoral trochlea. Am J Sports Med. 2016;44(03):633-8.
-
62Lattermann C, Kremser V, Altintas B. Use of Fresh Osteochondral Allografts in the Patellofemoral Joint. J Knee Surg. 2018;31(03):227-30.
-
63Gross AE, Aubin P, Cheah HK, Davis AM, Ghazavi MT. A fresh osteochondral allograft alternative. J Arthroplasty. 2002 Jun;17(4 Suppl 1):50-3.
-
64Drexler M, Gross A, Dwyer T, Safir O, Backstein D, Chaudhry H, et al. Distal femoral varus osteotomy combined with tibial plateau fresh osteochondral allograft for post-traumatic osteoarthritis of the knee. Knee Surg Sports TraumatolArthrosc. 2015;23(5):1317-23.
-
65Hsu AC, Tirico LEP, Lin AG, Pulido PA, Bugbee WD. Osteochondral Allograft Transplantation and Opening Wedge Tibial Osteotomy: Clinical Results of a Combined Single Procedure.Cartilage. 2018 Jul;9(3):248-254. doi: 10.1177/1947603517710307. Epub 2017 May 22.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Actualización en el tratamiento de las úlceras condrales de la rodilla
- Comparación de la inyección intraarticular de plasma rico en plaquetas (PRGF®) y ácido hialurónico (Hyalone®) en el tratamiento de las lesiones condrales: estudio clínico prospectivo aleatorizado
- Microfracturas o estimulación de la médula ósea (BMS): la evolución de la técnica
- Injerto de cartílago en fresco. Indicaciones, técnica quirúrgica y evidencia científica
- Condrogénesis inducida por matrices (AMIC)
- Instant CEMTRO Cell (ICC), implante de condrocitos autólogos de alta densidad
- Regenerar el cartílago articular: perspectivas y futuro
- Cirugía de implante de condrocitos autólogos en rodilla
- Úlceras condrales de espesor completo en rótula y cóndilo femoral de rodilla
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.