Tratamiento de las lesiones osteocondrales del astrágalo mediante artroscopia anterior del tobillo
Managing osteochondral lesions of the talus with anterior ankle arthroscopy
Resumen:
Las lesiones osteocondrales del astrágalo (osteochondral lesions of the talus –OLT–) se asocian con frecuencia a traumatismos del tobillo y pueden provocar síntomas y discapacidad importantes. Los pacientes suelen presentar dolor profundo en el tobillo entre 6 y 12 meses después de la lesión inicial. Las OLT pueden visualizarse mediante técnicas de imagen como la tomografía computarizada (TC) y la resonancia magnética (RM). Existe un acuerdo general acerca de que el tratamiento no quirúrgico debe ser el tratamiento inicial. Si el tratamiento no quirúrgico no conduce a una mejoría clínica suficiente, existen diversas opciones de tratamiento quirúrgico, tanto mediante artroscopia como mediante técnicas abiertas. La elección del tratamiento depende de las características tanto del paciente como de la lesión. Dada su naturaleza menos invasiva y sus tiempos de recuperación más cortos, las técnicas artroscópicas suelen considerarse como primera opción quirúrgica. Este artículo describe la etiología y el diagnóstico de las OLT y resume las opciones de tratamiento artroscópico disponibles más utilizadas, como la estimulación de la médula ósea, la perforación retrógrada, la fijación y las técnicas de implantación de cartílago.
Abstract:
Osteochondral lesions of the talus (OLT) are commonly associated with ankle trauma and can lead to significant symptoms and disability. Patients typically present with deep ankle pain 6-12 months following the initial injury. OLTs can be visualized through imaging techniques such as computed tomography (CT) scans and magnetic resonance imaging (MRI). There is general agreement that non-surgical treatment should be the initial treatment. If non-surgical management does not lead to sufficient clinical improvement, various surgical treatment options are available, both through arthroscopy as well as open techniques. The choice of treatment depends on both patient and lesion characteristics. Given their less invasive nature and shorter recovery times, arthroscopic techniques may usually be considered as a first surgical option. This article describes the etiology and diagnosis of OLTs and summarizes the available evidence on the most commonly used arthroscopic treatment options, such as bone marrow stimulation (BMS), retrograde drilling, fixation and cartilage implantation techniques.
Introducción
Una lesión osteocondral del astrágalo (osteochondral lesion of the talus –OLT–) se define como una lesión del hueso subastragalino y del cartílago articular suprayacente. Estas lesiones suelen desarrollarse tras un traumatismo en el tobillo(1,2,3). Se ha demostrado que las OLT se producen en más del 65% de los esguinces crónicos de tobillo y hasta en el 75% de las fracturas de tobillo(2,3). Actualmente, se desconoce la etiología de las OLT. Sin embargo, existe la hipótesis de que, durante un traumatismo, el astrágalo impacta contra la meseta tibial creando microfisuras en el cartílago y en la placa ósea subcondral(1,4,5,6). Se teoriza que, durante la carga de peso, un aumento de la presión en la articulación puede provocar la infiltración de líquido sinovial a través de estas microfracturas, lo que induce osteonecrosis y, por lo tanto, provoca la expansión de la lesión y la formación de una OLT(4).
Los pacientes suelen presentarse entre 6 y 12 meses después de un traumatismo de tobillo con dolor profundo en el tobillo, provocado durante la realización de actividades en las que se soporta peso o con posterioridad. Otros síntomas de presentación pueden ser sensación de bloqueo o chasquido, hinchazón o rigidez del tobillo(4,7). La exploración física y la anamnesis minuciosas son esenciales para un diagnóstico adecuado y para la toma de decisiones sobre el tratamiento. La palpación forzada de la cúpula talar durante la flexión plantar puede provocar la sensación de dolor profundo reconocible en el tobillo, si la lesión está situada en una posición lo suficientemente anterior como para poder palparla(4,7).
Cuando hay sospecha clínica de una OLT, se pueden realizar más pruebas de imagen. Las radiografías pueden ser útiles para evaluar la alineación del tobillo, pero tienen un escaso valor diagnóstico en las OLT(8). La confirmación radiológica y la evaluación de las OLT deben realizarse mediante tomografía computarizada (TC) y/o resonancia magnética nuclear (RMN), que tienen una alta sensibilidad y especificidad diagnósticas(8,9). La RMN puede ser útil para evaluar el cartílago del tobillo, detectar edema de médula ósea o diagnosticar lesiones concomitantes de partes blandas del tobillo. Sin embargo, se prefiere la TC para evaluar la morfología ósea y el tamaño de las OLT, y para evaluar la capa ósea subcondral, ya que la RMN puede sobrestimar el tamaño de la lesión debido al edema óseo(9,10). Además, la TC es una herramienta valiosa para la evaluación de la capa ósea subcondral, que desempeña un papel importante en las OLT(7). La TC también es útil en la planificación preoperatoria, por ejemplo, para valorar la viabilidad de alcanzar la OLT artroscópicamente(11). La TC por emisión monofotónica (SPECT) combina la evaluación del tamaño y la morfología de la lesión mediante TC con la obtención de imágenes funcionales de la actividad de la lesión(12,13). Así pues, la SPECT puede tener un valor añadido en la toma de decisiones terapéuticas en casos complejos con patologías coexistentes, para identificar la causa principal de los síntomas cuando las pruebas de imagen estándar y la evaluación clínica no proporcionan un diagnóstico adecuado(9).
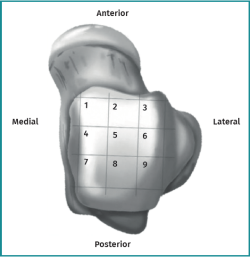
Las lesiones pueden caracterizarse por su localización, morfología y tamaño. La localización puede describirse utilizando un esquema anatómico del astrágalo de 9 cuadrículas, como el descrito por Raikin et al., que se muestra en la Figura 1(14). La morfología de una OLT puede describirse como crateriforme, quística o fragmentaria (Figura 2)(4,15,16). El tamaño de la lesión debe indicarse en el plano anteroposterior, en el plano medial-lateral y en profundidad, lo que permite calcular la superficie y el volumen de la lesión(4). Sin embargo, no hay consenso sobre la morfología de las OLT y, aunque existen sistemas de clasificación radiológica de las OLT, carecen de validación y utilizan una terminología incongruente. Además, los métodos de medición del tamaño de las lesiones varían, lo que contribuye aún más a la incongruencia en la caracterización de las lesiones en la literatura(15).
El tratamiento de la OLT debe comenzar con un periodo inicial de 3-6 meses de tratamiento no quirúrgico, a menos que sea factible la fijación de un fragmento desplazado agudo (es decir, una fractura osteocondral intraarticular aguda)(17). El tratamiento no quirúrgico puede incluir fisioterapia centrada en la amplitud de movimiento, la fuerza, el equilibrio y la propiocepción, o tratamientos como la inmovilización con yeso, ajustes del calzado con plantillas ortopédicas, pérdida de peso, tratamiento psicológico, modificaciones en la actividad laboral e inyecciones de ácido hialurónico o corticoides(4). El tratamiento no quirúrgico tiene éxito en aproximadamente el 45% de los pacientes(18).
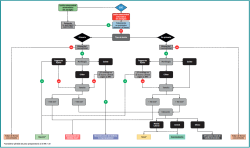
Si los pacientes siguen presentando síntomas tras el periodo de tratamiento no quirúrgico, puede considerarse la intervención quirúrgica. El tratamiento quirúrgico adecuado debe decidirse mediante una toma de decisiones compartida y un enfoque personalizado, incorporando las características del paciente (como la edad, el índice de masa corporal –IMC–, el nivel de actividad preoperatorio y las preferencias del paciente), los factores de la lesión (primaria o no primaria –no primaria significa que no se ha realizado un tratamiento quirúrgico previo de la OLT–, el tamaño de la lesión –área y volumen– y la morfología) y la patología concomitante del pie y el tobillo (por ejemplo, la alineación del retropié, la estabilidad del tobillo y las lesiones concomitantes)(4). Estos factores se incorporan a un paradigma de tratamiento basado en algoritmos multinivel. Existen diferentes paradigmas(4,19); uno de ellos puede apreciarse en la Figura 3.
Las técnicas quirúrgicas artroscópicas pueden ser una opción adecuada para tratar lesiones osteocondrales primarias pequeñas (< 15 mm) del astrágalo, aunque los procedimientos artroscópicos también pueden tener éxito en lesiones no primarias(20,21). Las técnicas artroscópicas conllevan incisiones cutáneas más pequeñas, no requieren una osteotomía y, por lo tanto, suelen tener un tiempo de recuperación más corto en comparación con las técnicas quirúrgicas abiertas para las OLT. Dado su carácter menos invasivo, las técnicas artroscópicas suelen considerarse habitualmente como primera opción quirúrgica. Sin embargo, cuando las técnicas quirúrgicas artroscópicas no son factibles, por ejemplo, en el caso de lesiones de mayor tamaño (> 15 mm), cuando una cirugía artroscópica previa ha fracasado y no es conveniente repetir el procedimiento, o cuando es difícil acceder a la lesión a través de los portales artroscópicos, puede considerarse la posibilidad de utilizar técnicas quirúrgicas abiertas(4). En la siguiente sección se analizarán diferentes tipos de técnicas quirúrgicas artroscópicas para el tratamiento de las OLT.
Técnicas quirúrgicas
Estimulación de la médula ósea
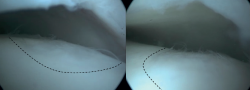
La estimulación de la médula ósea (EMO) por artroscopia es el tratamiento más frecuentemente utilizado para la lesión osteocondral primaria del astrágalo(22). Es posible utilizar la EMO en lesiones relativamente pequeñas (< 15 mm), no quísticas y no fijables(20,23). La EMO por artroscopia comienza con el desbridamiento y curetaje del cartílago defectuoso y del hueso subcondral(24). Posteriormente, se perfora el hueso esclerótico a la altura de la base del defecto, a menudo con una aguja de Kirschner o un punzón para microfractura(25). Los orificios deben realizarse a una profundidad que provoque la hemorragia del hueso subcondral o la presencia de gotas de grasa(23) (Figura 4). Esta técnica interrumpe los vasos sanguíneos intraóseos, lo que provoca la hemorragia del hueso subcondral y la formación de un coágulo de fibrina. La liberación de células sanguíneas mesenquimales favorece la vascularización, lo que induce la formación de fibrocartílago(26). Cuando se trata de una lesión cartilaginosa aislada (es decir, sin otras lesiones óseas o articulares) con una capa ósea subcondral macroscópicamente intacta, solo puede realizarse un desbridamiento(27).
La tasa de éxito de la EMO para lesiones primarias es del 82%, con una tasa de complicaciones del 4% y una tasa de reintervención del 7%(22,28,29). La tasa de éxito informada para las lesiones secundarias es inferior, del 69-75%(21). La progresión de la artrosis tras la EMO ha sido motivo de preocupación debido al deterioro más rápido del fibrocartílago en contraposición con el cartílago hialino. Aunque solo el 18% de los pacientes se sometieron a una cirugía de revisión a los 10 años de seguimiento(30), tras un seguimiento medio de 13 años, se observó una progresión de la artrosis en el 28% de los pacientes tras la EMO(31). Por lo tanto, se han descrito diversas terapias complementarias destinadas a mejorar la calidad del cartílago y la reparación del hueso subcondral. Estas terapias complementarias pueden ser productos sanguíneos autólogos como el plasma rico en plaquetas (PRP) o el concentrado de aspirado de médula ósea (bone marrow aspirate concentrate –BMAC–), que se administran al final del procedimiento de EMO(17,32,33). Sin embargo, no hay pruebas suficientes que respalden un efecto positivo de estos complementos y aún no se han demostrado los efectos positivos previstos de estas terapias adicionales(34).
Por lo que respecta al protocolo postoperatorio después de la EMO, las investigaciones demuestran que el levantamiento precoz de peso proporciona resultados similares o mejores después de la EMO en comparación con el levantamiento tardío de peso(35,36). Por lo tanto, se aconseja el levantamiento precoz de peso tras la artroscopia, lo que incluye vendaje y muletas durante los 2 primeros días del postoperatorio, tras lo cual se recomienda aumentar el levantamiento de peso y reducir el uso de muletas en 2 semanas, según se tolere(24).
Perforación retrógrada
La perforación retrógrada es una técnica no transarticular, que utiliza la fluoroscopia para la visualización del astrágalo, lo que permite desbridar y perforar el quiste subcartilaginoso. La perforación retrógrada puede considerarse una intervención quirúrgica para las OLT quísticas con una capa de cartílago articular intacta(22). La perforación retrógrada permite penetrar en la zona esclerótica necrótica para estimular la médula ósea sin dañar la superficie intacta del cartílago(37). Al igual que la EMO, la perforación retrógrada provoca la interrupción de los vasos sanguíneos intraóseos y, por tanto, favorece el relleno óseo subarticular del quiste. Tras exponer el astrágalo utilizando los portales anteromedial y anterolateral, se colocará una aguja de Kirschner bajo control fluoroscópico, transtalar desde el cuello astragalino opuesto hacia la zona subcondral esclerótica(37).
Como procedimiento adicional, el quiste desbridado puede rellenarse con hueso esponjoso, sobre todo en el caso de lesiones de gran tamaño, ya que la insuficiencia de células madre en el hueso subcondral en estos casos conlleva una menor probabilidad de regeneración adecuada del cartílago y el hueso subcondral dañados(22,38). En las OLT primarias, la perforación retrógrada tiene una tasa de éxito de entre el 68 y el 100% y una tasa de complicaciones del 5%(22,29).
El protocolo postoperatorio tras la perforación retrógrada suele consistir en 6 semanas de carga parcial de peso, lo que permite una amplitud de movimiento completa de inmediato. A las 6 semanas ya se puede soportar todo el peso.
Técnicas de fijación
Las técnicas de fijación se aplican principalmente a las OLT con morfología fragmentaria. Hubo consenso en que, para que estas técnicas fueran técnicamente viables, el fragmento de la lesión debía tener un diámetro de al menos 10 mm y una profundidad de 3 mm(39). Sin embargo, también se ha descrito una fijación satisfactoria de lesiones más pequeñas en estudios en los que se han utilizado clavos óseos corticales(40).
En las lesiones fragmentarias agudas desplazadas, la fijación debe considerarse como tratamiento inicial(4). Esto debe realizarse lo antes posible para maximizar el potencial de cicatrización y evitar mayores daños intraarticulares(39). En el caso de las lesiones crónicas, la fijación puede aplicarse cuando el tratamiento no quirúrgico no tiene éxito. Dado que las técnicas de fijación pueden proporcionar una cicatrización ósea subcondral superior(41), además de preservar el cartílago hialino suprayacente, deberían considerarse como la opción de tratamiento quirúrgico primario cuando sea factible.
Se han descrito varias técnicas de fijación que utilizan diferentes materiales, como agujas de Kirschner, tornillos metálicos, tornillos bioabsorbibles, clavijas óseas y/o pegamento de fibrina(42,43,44,45). Las técnicas de fijación pueden realizarse artroscópicamente cuando sea técnicamente posible. La naturaleza menos invasiva de la fijación artroscópica es ventajosa en teoría. El factor más decisivo para la posibilidad de fijación artroscópica es la localización/accesibilidad de la lesión. Para conseguir una fijación adecuada y estable, el fragmento debe fijarse perpendicularmente a la cúpula del astrágalo. Por lo tanto, la lesión debe estar situada en posición relativamente anterior en la cúpula talar para que la fijación artroscópica sea factible(11). Si la fijación artroscópica no es técnicamente posible, la fijación también puede realizarse como técnica abierta.
Una técnica quirúrgica de fijación específica es el procedimiento elevar, perforar, rellenar y fijar (lift, drill, fill and fix –LDFF–)(45). En esta técnica, se visualiza la lesión osteocondral y se utiliza un cuchillo de castor para crear un colgajo. A continuación, se levanta el colgajo para permitir el desbridamiento y la microfracturación del hueso subcondral. En el lecho del colgajo puede colocarse hueso esponjoso, normalmente extraído de la metáfisis distal de la tibia. Por último, el colgajo osteocondral se vuelve a colocar y se fija mediante tornillos de compresión bioabsorbibles, dardos condrales o clavijas óseas.
Las técnicas de fijación han demostrado éxito clínico y radiológico en 8 de cada 10 pacientes y el éxito también se ha mantenido a largo plazo (Figuras 5 y 6). Dado que estas técnicas preservan el cartílago hialino y proporcionan una cicatrización superior del hueso subcondral, resultan ventajosas frente a otras opciones de tratamiento quirúrgico de las OLT, cuando son factibles(39,41).
Implantación de cartílago
Las técnicas de implantación de cartílago, como la implantación de condrocitos autólogos (autologous chondrocyte implantation –ACI–) y la ACI inducida por matriz (matrix-induced autologous chondrocyte implantation –MACI–), tienen como objetivo regenerar el cartílago de tipo hialino mediante la implantación de condrocitos obtenidos y cultivados en la lesión osteocondral(46,47,48). Estas técnicas suelen constar de 2 pasos. En el primer paso, los condrocitos se extraen de una zona del astrágalo que no soporta carga o de los márgenes de la lesión durante un procedimiento artroscópico. Posteriormente, estos condrocitos se cultivan in vitro. La segunda fase consiste en reimplantar los condrocitos cultivados en la lesión extirpada.
Para la ACI, los condrocitos cultivados se implantan en un segundo procedimiento que suele tener lugar 3 semanas después del paso 1(47). Durante este segundo procedimiento, se realiza una osteotomía medial o lateral para acceder a la lesión, tras lo cual se lleva a cabo el desbridamiento de la lesión para prepararla para la implantación. Tras la implantación, los condrocitos implantados se cubren con un colgajo periostal de la tibia distal(49). Se utiliza adhesivo de fibrina para sellar la unión del colgajo con el cartílago articular(49).
En la técnica MACI, los condrocitos se cultivan y se incorporan en una matriz biodegradable, para evitar la morbilidad asociada al colgajo periostal y al lugar de extracción(46,48). El segundo paso suele realizarse entre 8 y 12 semanas después de la extracción de los condrocitos. Se accede mediante una osteotomía medial o lateral y, tras el desbridamiento de la lesión, se mide el tamaño de la lesión utilizando una plantilla metálica. A continuación, el injerto MACI se recorta siguiendo la plantilla y se coloca en la lesión con la cara que contiene las células orientada hacia el defecto. A continuación, se utiliza adhesivo de fibrina para fijar el injerto(50).
Estas técnicas han mostrado resultados prometedores en la rodilla, con una regeneración tisular superior a la de la EMO(51). Esto aún no se ha demostrado en el caso de la OLT. Sin embargo, estas técnicas presentan algunas desventajas: requieren un procedimiento quirúrgico adicional y el laboratorio con los recursos necesarios para realizar estas técnicas puede ser bastante costoso.
La condrogénesis autóloga inducida por matriz (autologous matrix-induced chondrogenesis –AMIC–) es una terapia de nueva generación basada en andamiaje que combina una matriz de colágeno con la técnica de microfracturas y no requiere un procedimiento de 2 pasos(52). La membrana AMIC es una matriz bicapa de colágeno de tipo I/III que estabiliza el supercoágulo que se forma sobre la lesión tras la microfractura. Esto evita la pérdida de células por filtración al espacio articular y limita la tensión mecánica en la zona de regeneración, lo cual favorece la diferenciación condrogénica y mejora la deposición de proteoglicanos, lo que conduce a la formación de cartílago hialino. Durante el procedimiento AMIC, se desbrida la lesión osteocondral y se estimula el hueso subcondral mediante la EMO, tras lo cual se corta la membrana AMIC en el tamaño exacto del defecto antes de introducirla y fijarla con adhesivo de fibrina(52).
Las técnicas de implantación de cartílago tienen una tasa de éxito del 70-92% y una tasa de complicaciones del 5%(18,29). El tratamiento postoperatorio suele consistir en no soportar peso durante 6 semanas. Se suele permitir el soporte completo de peso después de 7-9 semanas(47,50).
Conclusión
Este artículo ofrece una visión general de la etiología y el diagnóstico de las OLT, y resume la bibliografía actual sobre las opciones de tratamiento artroscópico. El tratamiento no quirúrgico debe ser el enfoque inicial para las OLT. Si fracasa el tratamiento no quirúrgico, las técnicas de fijación, como el procedimiento LDFF, cuando son técnicamente viables, pueden considerarse como la opción de tratamiento quirúrgico inicial. En ausencia de un fragmento fijable, es posible que el tratamiento artroscópico con técnicas de EMO o de implantación de cartílago sean eficaces. Si el tratamiento artroscópico fracasa o no es técnicamente viable, las técnicas quirúrgicas abiertas siguen siendo una alternativa para tratar las OLT.
Figuras
Figura 2. Tipos de morfologías de las lesiones osteocondrales del astrágalo observados en tomografía computarizada en vista coronal y sagital. A: crateriforme; B: quística; C: fragmentaria.
Figura 3. Diagrama de flujo para el tratamiento quirúrgico de las lesiones osteocondrales del astrágalo, versión modificada del diagrama de flujo de Rikken et al.(4), con permiso de los autores.
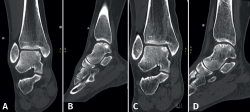
Figura 5. Tomografía computarizada preoperatoria (A y B) y postoperatoria al año (C y D) de un paciente tras la fijación.
Información del artículo
Cita bibliográfica
Autores
Juliëtte HM Pijnacker
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Jason AH Steman
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Julian J Hollander
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Jari Dahmen
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Quinten GH Rikken
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Kaj S Emanuel
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Sjoerd AS Stufkens
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Gino MMJ Kerkhoffs
Departamento de Cirugía Ortopédica y Medicina Deportiva. Amsterdam University Medical Center (UMC). Sede AMC. Universidad de Ámsterdam. Países Bajos
Ciencias del Movimiento de Ámsterdam. Programas de Deporte y Salud Musculoesquelética. Ámsterdam. Países Bajos
Centro Académico de Medicina Deportiva Basada en la Evidencia (ACES). Amsterdam UMC. Ámsterdam. Países Bajos
Colaboración de Ámsterdam para la Salud y la Seguridad en el Deporte (ACHSS). Centro de Investigación del Comité Olímpico Internacional (COI). Amsterdam UMC. Ámsterdam. Países Bajos
Responsabilidades éticas
Conflictos de intereses. El autor Prof. Dr. G.M.M.J. Kerkhoffs declara los siguientes conflictos de intereses: consultor Arthrex, Nápoles.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Blom RP, Mol D, van Ruijven LJ, et al. A Single Axial Impact Load Causes Articular Damage That Is Not Visible with Micro-Computed Tomography: An Ex Vivo Study on Caprine Tibiotalar Joints. Cartilage. 2021;13(2_suppl):1490s-1500s.
-
2Hintermann B, Boss A, Schafer D. Arthroscopic findings in patients with chronic ankle instability. Am J Sports Med. 2002;30(3):402-9.
-
3Hintermann B, Regazzoni P, Lampert C, et al. Arthroscopic findings in acute fractures of the ankle. J Bone Joint Surg Br. 2000;82(3):345-51.
-
4Rikken QGH, Kerkhoffs G. Osteochondral Lesions of the Talus: An Individualized Treatment Paradigm from the Amsterdam Perspective. Foot Ankle Clin. 2021;26(1):121-36.
-
5Kerkhoffs G, Karlsson J. Osteochondral lesions of the talus. Knee Surg Sports Traumatol Arthrosc. 2019;27(9):2719-20.
-
6Dahmen J, Karlsson J, Stufkens SAS, Kerkhoffs G. The ankle cartilage cascade: incremental cartilage damage in the ankle joint. Knee Surg Sports Traumatol Arthrosc. 2021;29(11):3503-7.
-
7Reilingh M, van Bergen C, Dijk vN. Diagnosis and treatment of osteochondral defects of the ankle. South African Orthopaedic J. 2009;8:44-50.
-
8Verhagen RA, Maas M, Dijkgraaf MG, et al. Prospective study on diagnostic strategies in osteochondral lesions of the talus. Is MRI superior to helical CT? J Bone Joint Surg Br. 2005;87(1):41-6.
-
9Van Bergen CJ, Gerards RM, Opdam KT, et al. Diagnosing, planning and evaluating osteochondral ankle defects with imaging modalities. World J Orthop. 2015;6(11):944-53.
-
10Yasui Y, Hannon CP, Fraser EJ, et al. Lesion Size Measured on MRI Does Not Accurately Reflect Arthroscopic Measurement in Talar Osteochondral Lesions. Orthop J Sports Med. 2019;7(2):2325967118825261.
-
11Van Bergen CJ, Tuijthof GJ, Maas M, et al. Arthroscopic accessibility of the talus quantified by computed tomography simulation. Am J Sports Med. 2012;40(10):2318-24.
-
12Meftah M, Katchis SD, Scharf SC, et al. SPECT/CT in the management of osteochondral lesions of the talus. Foot Ankle Int. 2011;32(3):233-8.
-
13Leumann A, Valderrabano V, Plaass C, et al. A novel imaging method for osteochondral lesions of the talus--comparison of SPECT-CT with MRI. Am J Sports Med. 2011;39(5):1095-101.
-
14Raikin SM, Elias I, Zoga AC, et al. Osteochondral lesions of the talus: localization and morphologic data from 424 patients using a novel anatomical grid scheme. Foot Ankle Int. 2007;28(2):154-61.
-
15Van Diepen PR, Smithuis FF, Hollander JJ, et al. Reporting of Morphology, Location, and Size in the Treatment of Osteochondral Lesions of the Talus in 11,785 Patients: A Systematic Review and Meta-Analysis. Cartilage. 2024:19476035241229026.
-
16Rikken QGH, Wolsink LME, Dahmen J, et al. 15% of Talar Osteochondral Lesions Are Present Bilaterally While Only 1 in 3 Bilateral Lesions Are Bilaterally Symptomatic. J Bone Joint Surg Am. 2022;104(18):1605-13.
-
17Dombrowski ME, Yasui Y, Murawski CD, et al. Conservative Management and Biological Treatment Strategies: Proceedings of the International Consensus Meeting on Cartilage Repair of the Ankle. Foot Ankle Int. 2018;39(1):9s-15s.
-
18Zengerink M, Struijs PA, Tol JL, van Dijk CN. Treatment of osteochondral lesions of the talus: a systematic review. Knee Surg Sports Traumatol Arthrosc. 2010;18(2):238-46.
-
19Savage-Elliott I, Ross KA, Smyth NA, et al. Osteochondral lesions of the talus: a current concepts review and evidence-based treatment paradigm. Foot Ankle Spec. 2014;7(5):414-22.
-
20Ramponi L, Yasui Y, Murawski CD, et al. Lesion Size Is a Predictor of Clinical Outcomes After Bone Marrow Stimulation for Osteochondral Lesions of the Talus: A Systematic Review. Am J Sports Med. 2017;45(7):1698-705.
-
21Lambers KTA, Dahmen J, Reilingh ML, et al. No superior surgical treatment for secondary osteochondral defects of the talus. Knee Surg Sports Traumatol Arthrosc. 2018;26(7):2158-70.
-
22Dahmen J, Lambers KTA, Reilingh ML, et al. No superior treatment for primary osteochondral defects of the talus. Knee Surg Sports Traumatol Arthrosc. 2018;26(7):2142-57.
-
23Hannon CP, Bayer S, Murawski CD, et al. Debridement, Curettage, and Bone Marrow Stimulation: Proceedings of the International Consensus Meeting on Cartilage Repair of the Ankle. Foot Ankle Int. 2018;39(1):16s-22s.
-
24D'Hooghe P, Murawski CD, Boakye LAT, et al. Rehabilitation and Return to Sports: Proceedings of the International Consensus Meeting on Cartilage Repair of the Ankle. Foot Ankle Int. 2018;39(1_suppl):61s-67s.
-
25Murawski CD, Foo LF, Kennedy JG. A Review of Arthroscopic Bone Marrow Stimulation Techniques of the Talus: The Good, the Bad, and the Causes for Concern. Cartilage. 2010;1(2):137-44.
-
26O'Driscoll SW. The healing and regeneration of articular cartilage. J Bone Joint Surg Am. 1998;80(12):1795-812.
-
27Shimozono Y, Coale M, Yasui Y, et al. Subchondral Bone Degradation After Microfracture for Osteochondral Lesions of the Talus: An MRI Analysis. Am J Sports Med. 2018;46(3):642-8.
-
28Toale J, Shimozono Y, Mulvin C, et al. Midterm Outcomes of Bone Marrow Stimulation for Primary Osteochondral Lesions of the Talus: A Systematic Review. Orthop J Sports Med. 2019;7(10):2325967119879127.
-
29Hollander JJ, Dahmen J, Emanuel KS, et al. The Frequency and Severity of Complications in Surgical Treatment of Osteochondral Lesions of the Talus: A Systematic Review and Meta-Analysis of 6,962 Lesions. Cartilage. 2023;14(2):180-97.
-
30Rikken QGH, Aalders MB, Dahmen J, et al. Ten-Year Survival Rate of 82% in 262 Cases of Arthroscopic Bone Marrow Stimulation for Osteochondral Lesions of the Talus. J Bone Joint Surg Am. 2024;106(14):1268-76.
-
31Rikken QGH, Dahmen J, Stufkens SAS, Kerkhoffs G. Satisfactory long-term clinical outcomes after bone marrow stimulation of osteochondral lesions of the talus. Knee Surg Sports Traumatol Arthrosc. 2021;29(11):3525-33.
-
32Guney A, Akar M, Karaman I, et al. Clinical outcomes of platelet rich plasma (PRP) as an adjunct to microfracture surgery in osteochondral lesions of the talus. Knee Surg Sports Traumatol Arthrosc. 2015;23(8):2384-9.
-
33Murphy EP, Fenelon C, McGoldrick NP, Kearns SR. Bone Marrow Aspirate Concentrate and Microfracture Technique for Talar Osteochondral Lesions of the Ankle. Arthrosc Tech. 2018;7(4):e391-e396.
-
34Klein C, Dahmen J, Emanuel KS, et al. Limited evidence in support of bone marrow aspirate concentrate as an additive to the bone marrow stimulation for osteochondral lesions of the talus: a systematic review and meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2023;31(12):6088-103.
-
35Deal JB Jr., Patzkowski JC, Groth AT, et al. Early vs Delayed Weightbearing After Microfracture of Osteochondral Lesions of the Talus: A Prospective Randomized Trial. Foot Ankle Orthop. 2019;4(2):2473011419838832.
-
36Song M, Li S, Yang S, et al. Is Early or Delayed Weightbearing the Better Choice After Microfracture for Osteochondral Lesions of the Talus? A Meta-analysis and Systematic Review. J Foot Ankle Surg. 2021;60(6):1232-40.
-
37Anders S, Lechler P, Rackl W, et al. Fluoroscopy-guided retrograde core drilling and cancellous bone grafting in osteochondral defects of the talus. Int Orthop. 2012;36(8):1635-40.
-
38Takao M, Innami K, Komatsu F, Matsushita T. Retrograde cancellous bone plug transplantation for the treatment of advanced osteochondral lesions with large subchondral lesions of the ankle. Am J Sports Med. 2010;38(8):1653-60.
-
39Reilingh ML, Murawski CD, DiGiovanni CW, et al. Fixation Techniques: Proceedings of the International Consensus Meeting on Cartilage Repair of the Ankle. Foot Ankle Int. 2018;39(1_suppl):23s-27s.
-
40Park CH, Song KS, Kim JR, Lee SW. Retrospective evaluation of outcomes of bone peg fixation for osteochondral lesion of the talus. Bone Joint J. 2020;102-b(10):1349-53.
-
41Reilingh ML, Lambers KTA, Dahmen J, et al. The subchondral bone healing after fixation of an osteochondral talar defect is superior in comparison with microfracture. Knee Surg Sports Traumatol Arthrosc. 2018;26(7):2177-82.
-
42Kumai T, Takakura Y, Kitada C, et al. Fixation of osteochondral lesions of the talus using cortical bone pegs. J Bone Joint Surg Br. 2002;84(3):369-74.
-
43Fuchs M, Vosshenrich R, Dumont C, Sturmer KM. Refixation of osteochondral fragments using absorbable implants. First results of a retrospective study. [German]. Chirurg. 2003;74(6):554-61.
-
44Kaplonyi G, Zimmerman I, Frenyo AD, et al. The use of fibrin adhesive in the repair of chondral and osteochondral injuries. Injury. 1988;19(4):267-72.
-
45Lambers KTA, Dahmen J, Reilingh ML, et al. Arthroscopic lift, drill, fill and fix (LDFF) is an effective treatment option for primary talar osteochondral defects. Knee Surg Sports Traumatol Arthrosc. 2020;28(1):141-7.
-
46Lenz CG, Tan S, Carey AL, et al. Matrix-Induced Autologous Chondrocyte Implantation (MACI) Grafting for Osteochondral Lesions of the Talus. Foot Ankle Int. 2020;41(9):1099-105.
-
47Baums MH, Heidrich G, Schultz W, et al. Autologous chondrocyte transplantation for treating cartilage defects of the talus. J Bone Joint Surg Am. 2006;88(2):303-8.
-
48Cherubino P, Grassi FA, Bulgheroni P, Ronga M. Autologous chondrocyte implantation using a bilayer collagen membrane: a preliminary report. J Orthop Surg (Hong Kong). 2003;11(1):10-5.
-
49Baums MH, Heidrich G, Schultz W, et al. The surgical technique of autologous chondrocyte transplantation of the talus with use of a periosteal graft. Surgical technique. J Bone Joint Surg Am. 2007;89 Suppl 2 Pt.2:170-82.
-
50Schneider TE, Karaikudi S. Matrix-induced Autologous Chondrocyte Implantation (MACI) grafting for osteochondral lesions of the talus. Foot Ankle Int. 2009;30(9):810-4.
-
51Saris DB, Vanlauwe J, Victor J, et al. Characterized chondrocyte implantation results in better structural repair when treating symptomatic cartilage defects of the knee in a randomized controlled trial versus microfracture. Am J Sports Med. 2008;36(2):235-46.
-
52Gottschalk O, Altenberger S, Baumbach S, et al. Functional Medium-Term Results After Autologous Matrix-Induced Chondrogenesis for Osteochondral Lesions of the Talus: A 5-Year Prospective Cohort Study. J Foot Ankle Surg. 2017;56(5):930-6.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- La artroscopia anterior de tobillo en todo su esplendor
- La artroscopia de pie y tobillo, una realidad consolidada y en expansión
- Historia y conceptos actuales de la artroscopia de tobillo
- Estado actual del pinzamiento anterior de tobillo
- Tratamiento artroscópico de la inestabilidad lateral crónica de tobillo
- Tratamiento de las lesiones osteocondrales del astrágalo mediante artroscopia anterior del tobillo
- Papel de la artroscopia en las lesiones de la sindesmosis
- Papel de la artroscopia en el tratamiento de las fracturas de tobillo
- Artrodesis artroscópica anterior de tobillo
- El uso de la artroscopia con aguja en el tobillo
- La letra pi en el tobillo
Más en PUBMED
Más en Google Scholar


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.