Fisiopatología, diagnóstico y tratamiento de la tendinopatía aquílea
Pathophysiology, diagnosis and treatment of Achilles tendinopathy
Resumen:
El tendón de Aquiles es el tendón más grande, grueso y fuerte del cuerpo. Por ello, queremos resaltar la importancia de su patología inflamatoria, degenerativa y traumática, que representa un reto diagnóstico y terapéutico. A este respecto, cabe destacar la evolución de la ecografía como método diagnóstico comparable a la resonancia magnética (RM) en muchos aspectos. A tal efecto, la ecografía se ha integrado en los procesos terapéuticos invasivos no quirúrgicos, así como en cirugías endoscópicas, ya que les presta un soporte útil aumentando el campo de visión. En cuanto al tratamiento, sigue siendo de elección el conservador, que asocia medidas físicas y ortopédicas. El fracaso del mismo puede complementarse con terapias invasivas no quirúrgicas como la electrolisis percutánea intratisular, así como la infiltración de diferentes sustancias. El tratamiento quirúrgico solo está indicado ante la ausencia de resultados beneficiosos de los anteriores y con el único objetivo de restablecer la función del tendón. En esta línea, se han desarrollado técnicas poco invasivas con resultados similares o incluso mejores que los obtenidos con cirugía abierta, con una menor morbilidad y tiempo quirúrgico.
Abstract:
The Achilles tendon is the largest, thickest and strongest tendon in the body. It is thus advisable to underscore the importance of the inflammatory, degenerative and traumatic disorders of this tendon, which constitute a diagnostic and therapeutic challenge. In this regard, mention must be made of the evolution of ultrasound as a diagnostic method comparable in many aspects to magnetic resonance imaging (MRI). Ultrasound has become incorporated to nonsurgical invasive therapeutic processes, as well as to endoscopic surgery, since it offers useful support, magnifying the field of vision. With regard to treatment, conservative management remains the preferred option, combining physical and orthopedic measures. In the event of failure of such treatment, nonsurgical invasive procedures may be used, such as intratissue percutaneous electrolysis, as well as the infiltration of different substances. Surgery is only indicated when the above measures fail to yield benefits, and with the sole purpose of restoring tendon function. In this regard, scantly invasive techniques have been developed offering outcomes similar to or even better than those obtained by open surgery, and with less morbidity and shorter operating times.
Introducción
El tendón de Aquiles es el tendón más potente del organismo, soportando fuerzas de tracción de hasta 10 veces el peso corporal(1). Debido a la importancia de este tendón, cabe destacar sus mecanismos de evolución fisiopatológicos, que ayuden a comprender su gran diversidad clínica desde el punto de vista inflamatorio, degenerativo y traumático(2,3,4,5). En el plano diagnóstico, el desarrollo de la ecografía la ha convertido en una herramienta importante, equiparable a la resonancia magnética (RM) en muchos aspectos(2). Además, juega un papel destacable al asistir con imagen procesos invasivos no quirúrgicos y junto a cirugías endoscópicas, para aumentar el campo de visión de estas técnicas quirúrgicas(6,7). Al abordar el tratamiento de las tendinopatías, debe ser considerado el conservador como la estrategia de primera línea, siendo las terapias físicas las que actualmente tienen una especial relevancia(8,9). Estas medidas se pueden asociar con terapias invasivas dentro del ámbito no quirúrgico, como son la electrolisis percutánea intratisular (EPI)(10,11) o la infiltración de diferentes sustancias que actualmente se encuentran disponibles(12,13,14,15). En cuanto al tratamiento quirúrgico, el objetivo sería restaurar la función previa del tendón. Se destaca el desarrollo en los últimos años de las técnicas mínimamente invasivas y endoscópicas, por ser procedimientos efectivos con una menor morbilidad, tiempo quirúrgico y número de complicaciones(16,17,18,19,20,21,22,23).
Los objetivos de esta revisión son: explicar la evolución natural de las tendinopatías, destacando el papel diagnóstico de la ecografía y la RM, en las que describiremos los hallazgos en las imágenes que definen cada patología. Por último, analizaremos los principios del tratamiento, haciendo un recorrido desde los más conservadores hasta los más invasivos.
Fisiopatología y evolución natural de la tendinopatía aquílea
El tendón de Aquiles es el tendón más grande, grueso y fuerte del organismo. Su longitud es de 15 cm, su anchura de 12-15 mm y su espesor de 5-6 mm. Está sujeto a cargas tensiles de hasta 10 veces el peso corporal(1).
La patología del tendón de Aquiles se puede clasificar en 2 grandes entidades(2,5): tendinopatías y roturas tendinosas.
. Tendinopatías. Dentro de esta entidad se puede distinguir entre:
– Peritendinitis: es una inflamación del paratendón, en la que se produce una proliferación de fibroblastos e hipervascularización. Puede ser aguda (< 2 semanas), subaguda (de 2 a 6 semanas) o crónica (> 6 semanas). Cuando es crónica, se puede asociar a fenómenos degenerativos.
– Tendinosis: es una degeneración del tendón. Se produce por microtraumas de repetición(3), envejecimiento o la mezcla de ambos. Se altera el metabolismo de los tenocitos, que producen un colágeno menos resistente (tipo 3) y una matriz alterada, aumenta el catabolismo (apoptosis precoz) y se produce una respuesta reparadora excesiva, que conlleva una neoangiogénesis, neoinervación (dolor) y cicatrización de mala calidad, dando cambios degenerativos. Puede evolucionar hacia roturas intersticiales, roturas parciales o roturas completas agudas.
A su vez, por su localización, podemos clasificar las tendinopatías en:
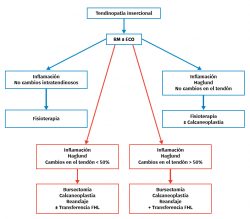
– Tendinopatía insercional(24): alteración patológica tendinosa en su zona de inserción. Se asocia frecuentemente a bursitis retroaquílea. En este contexto, la deformidad de Haglund no necesariamente se asocia a este cuadro, ni mucho menos es la causa(25).
– Tendinopatía no insercional(26): los mecanismos patológicos tienen lugar en el cuerpo del tendón que, al ser una zona mal vascularizada, predispone al desarrollo de cambios degenerativos. Suele asociarse con microrroturas cuando están presentes mecanismos por sobreuso. La presencia de este tipo de patología es menos frecuente en la unión miotendinosa, que se relaciona más con fenómenos de desgarro muscular.
Existen una serie de factores de riesgo que intervienen en el desarrollo de la patología del tendón de Aquiles. Entre ellos, se destacan:
– Intrínsecos: anatomía que predispone a una situación biomecánica de incapacidad para absorber fuerzas y una fisiología que afecta a la resistencia tisular del tendón(27). Entre ellos, destacan: excesivo varo/valgo del retropié o el antepié, hiperpronación subtalar, pie cavo, dismetría, atrofias o deficiencias musculotendinosas, desequilibrios musculares, sobrepeso y obesidad, edad avanzada y enfermedades reumáticas que cursen con artropatías inflamatorias o tendinosis.
– Extrínsecos(28): entre ellos, el sobreuso, deporte en exceso, errores de entrenamiento (duración, intensidad), carrera o salto sobre superficies no adecuadas(29), calzado inadecuado y fármacos como fluoroquinolonas y corticoides (sistémicos o infiltrados localmente).
. Roturas tendinosas: son más frecuentes en varones (5:1), con edades comprendidas entre los 30 y los 50 años, y en deportistas no profesionales. Su incidencia va en aumento en relación con la práctica de deporte en edades más avanzadas. Suele ser consecuencia de traumatismo indirecto, dándose la combinación de tensión mecánica más degeneración intratendinosa, a partir de dorsiflexión brusca de tobillo partiendo de una flexión plantar activa con la rodilla en extensión o en flexión plantar forzada partiendo de posición neutra(4).
Las roturas pueden ser parciales, completas e intrasustancia. De todas ellas, las completas son las más frecuentes. Se asocian generalmente a fenómenos degenerativos en el tendón, por lo que los factores de riesgo suelen ser similares a las descritos anteriormente para las tendinopatías(28).
Diagnóstico por imagen
Ecografía
La ecografía permite el estudio del tendón en toda su longitud, visualizándose un patrón fibrilar en el eje longitudinal y una estructura ovalada hiperecogénica en el eje transversal(6,30).
Se emplea una sonda lineal de alta frecuencia (10-18 MHz). Conviene comenzar la exploración en el eje transversal proximal a la unión miotendinosa en dirección distal. Posteriormente, se valora el tendón en el eje longitudinal girando la sonda 90°(30).
En la descripción ecográfica del tendón de Aquiles normal, se observa cómo la inserción distal en calcáneo se produce por medio de una interfase fibrocartilaginosa hipoecogénica de 2 cm. Así mismo, el paratendón (no siempre visible) aparece más frecuentemente como una banda hiperecogénica en la región posterior y más hipoecogénica en la región lateral y medial(30). Se distingue la grasa de Kager como un triángulo invertido hipoecogénico por delante del tendón de Aquiles(6). En el estudio de las bursas, la retrocalcánea puede contener líquido de manera fisiológica aunque en cuantía no mayor de 3 mm y la retroaquílea no es visible en condiciones normales(5).
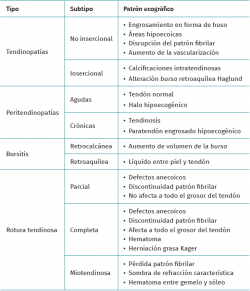
En cuanto a los hallazgos patológicos de la ecografía (Tabla 1), en la tendinopatía aquílea no insercional (2-6 cm de la inserción del calcáneo) (Figura 1), se aprecia un engrosamiento del área del tendón en forma de huso; áreas hipoecoicas y disrupción del patrón fibrilar que pueden corresponder a degeneración o rotura parcial(24,28). También es posible que presente un aumento de la vascularización en la porción ventral peritendinosa(5,6,30).
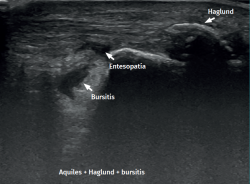
Sin embargo, en las formas crónicas de tendinopatía aquílea insercional o entesopatía (presente en los 2 cm distales del tendón), se pueden observar calcificaciones intratendinosas a modo de entesofitos de tracción o en la inserción como espolones. A menudo se asocian con alteraciones en la bursa retroaquílea(5,31) (Figura 2).
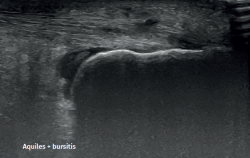
En la peritendinitis aislada, la ecografía muestra un tendón normal rodeado de líquido en forma de halo hipoecogénico. En las crónicas, se aprecia un paratendón engrosado hipoecogénico que suele asociar fenómenos de tendinosis(32).
Las bursitis retrocalcáneas muestran un aumento de volumen de la bursa y se pueden asociar a deformidad de Haglund(25). En las bursitis retroaquílea o calcánea superficial se puede apreciar líquido entre la piel y el tendón de Aquiles(5).
En el estudio de las roturas del tendón de Aquiles, las parciales se aprecian en la ecografía como defectos anecoicos con discontinuidad del patrón fibrilar en el eje longitudinal del tendón que no afecta a todo el grosor tendinoso(33). En cuanto a las roturas completas, estos defectos anecoicos van a estar presentes en todo el grosor del tendón. En el caso de las roturas agudas, se puede valorar el hematoma y la herniación de la grasa de Kager. Sin embargo, en las crónicas, la base del diagnóstico se hará por RM, como se describirá posteriormente. Las roturas en la unión miotendinosa se caracterizan por presentar una pérdida del patrón fibrilar, con una sombra de refracción característica que delimita los segmentos rotos y retraídos, así como el hematoma interfascial localizado entre el gemelo y el sóleo(33).
Resonancia magnética
A pesar de la evolución en este terreno de la ecografía, la RM sigue siendo un método útil para el diagnóstico de las alteraciones del tendón de Aquiles, ya que permite identificar y cuantificar la degeneración, la infiltración grasa, las lesiones intratendinosas y es especialmente útil para identificar roturas parciales y completas de carácter crónico.
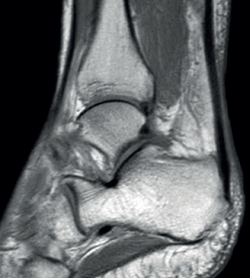
El tendón de Aquiles normal se observa hipointenso tanto en secuencias T1 como en T2(33) (Figura 3). En el plano sagital sus bordes son paralelos y en el axial presenta en su tramo distal un borde cóncavo anterior hacia el calcáneo en la mayor parte de su trayecto. Mantiene un grosor similar en su recorrido y presenta una cantidad mínima de líquido a nivel retrocalcáneo (el líquido rodeando al tendón es patológico)(34).
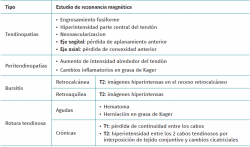
En relación con los patrones patológicos del tendón de Aquiles (Tabla 2), las tendinosis, en RM presentan una pérdida de la forma normal del tendón con engrosamiento fusiforme. Se puede observar una pérdida del aplanamiento anterior en secuencias sagitales y convexidad en la cara anterior del tendón en secuencias axiales. También se aprecian zonas de hiperintensidad de la parte central del tendón tanto en secuencias potenciadas en T1 como en T2, con neovascularización tendinosa(34). Hay que tener presente que se pueden hallar signos de tendinosis aquílea en personas asintomáticas(35).
Las paratendinopatías muestran un aumento de intensidad tanto en la secuencia T1 como en la secuencia T2 alrededor del tendón, pudiendo asociar cambios inflamatorios en la grasa de Kager o “kageítis”(34).
Las bursitis retrocalcáneas muestran imágenes hiperintensas en secuencias T2 en el receso retrocalcáneo(5) y en la bursitis retroaquílea o bursitis calcánea superficiales, la inflamación de la bursa se traduce en imágenes hiperintensas en la secuencia T2(5).
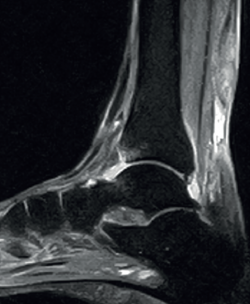
Por último, en las roturas agudas del tendón de Aquiles, la RM muestra el hematoma y también herniación de la grasa de Kager, signos similares a los hallados en la ecografía (Figura 4). En las crónicas, el estudio mediante RM es más adecuado para su diagnóstico. En la secuencia T1, se aprecia pérdida de la continuidad entre los cabos y, en la secuencia T2, se aprecia hiperintensidad entre los 2 cabos tendinosos por interposición de tejido conjuntivo y cambios cicatriciales(36).
Tratamiento no quirúrgico
Las distintas modalidades clínicas en las que se puede presentar la tendinopatía aquílea obligan a adecuar el tratamiento a cada caso, identificando el problema y adoptando las medidas oportunas para conseguir su curación y un retorno óptimo a la actividad física(37).
El tratamiento conservador debe ser considerado la estrategia de primera línea. El primer paso debería ser la identificación y la corrección de alteraciones en la movilidad, en la pisada y desalineaciones o dismetrías(27).
La inmovilización con férulas, de forma prolongada, ha demostrado tener efectos negativos sobre el tejido tendinoso(37). La inmovilización intermitente con férulas asociada a un programa de terapia física tampoco ha conseguido demostrar superioridad respecto a la terapia física aislada(38,39).
Las ortesis plantares pueden ser beneficiosas porque reducen el estrés mecánico al corregir desalineaciones(40), aumentan la movilidad del retropié(41) y descargan el tendón de Aquiles(42). Sin embargo, un metaanálisis de ensayos clínicos aleatorizados no encontró ningún beneficio en el empleo de ortesis asociadas a programas de terapia física o comparadas de forma aislada con placebo, por lo que no se recomienda su uso en esta patología(43).
Dentro de las terapias físicas, las basadas en el ejercicio han adquirido especial relevancia desde hace más de tres décadas. Los ejercicios excéntricos se han considerado la base del tratamiento de la mayoría de las tendinopatías del miembro inferior, especialmente a raíz de la publicación del protocolo de Alfredson(44), consistente en un programa de entrenamiento basado en ejercicios de alta frecuencia y baja intensidad realizados sobre una superficie inclinada. Su efectividad en la mejora del dolor y de la función, así como en la estructura tendinosa, está ampliamente contrastada, tanto para tendinopatías insercionales como no insercionales(8). Aunque hay estudios que describen mejores resultados que los entrenamientos basados en ejercicios concéntricos de forma aislada(45), actualmente no esta tan clara la diferencia entre los distintos tipos de contracción en el tratamiento de las tendinopatías del Aquiles(46). Sin embargo, la introducción de programas de trabajo que combinan diferentes ejercicios aplicados en intensidades variables, como el heavy, slow resistance training, han demostrado resultados comparables al entrenamiento excéntrico único, por lo que actualmente se recomienda con frecuencia la combinación de ejercicios concéntricos y excéntricos(9).
En los últimos años se ha extendido el uso de las ondas de choque como tratamiento de las tendinopatías. Existen varios mecanismos por los cuales pueden producir efectos beneficiosos en el tendón patológico, tales como la inhibición de los receptores aferentes nociceptivos y el aumento de la proliferación celular local(47). Su uso en tendinopatías aquíleas insercionales parece ser más efectivo que el entrenamiento con excéntricos aislados a medio plazo, mientras que en tendinopatías no insercionales tienen resultados comparables y, en cualquier caso, superiores a no realizar ningún tratamiento(48), por lo que constituyen una alternativa válida en el tratamiento de esta entidad.
Tratamientos invasivos no quirúrgicos
Como hemos mencionado, en la literatura se han descrito numerosos algoritmos terapéuticos para el tratamiento de la tendinopatía aquílea, desde el rehabilitador hasta el quirúrgico. El tratamiento con técnicas invasivas mediante punción ocupa un lugar intermedio entre ambos. Su uso combinado con técnicas de imagen como la ecografía aumenta la efectividad con respecto a la punción a ciegas y disminuye el riesgo de complicaciones asociadas a la punción accidental no diana o por el efecto del material empleado en estructuras no deseadas.
Las infiltraciones con corticoides han demostrado reducir el dolor, la inflamación a corto plazo y mejorar las imágenes ecográficas del tendón, probablemente por su acción vasoconstrictora(49). Sin embargo, se han descrito efectos adversos importantes que incluyen la debilidad y la rotura del tendón(12). Johansen et al.(50) realizaron una revisión sistemática con seguimiento durante 10 años en pacientes tratados con inyecciones ecoguiadas con corticoides y suplementadas con rehabilitación controlada. Observaron que 1 o 2 inyecciones de corticoides son efectivas y seguras en el tratamiento del dolor aquíleo, sin signos de deterioro del tendón a largo plazo, tanto en tendinopatías insercionales como no insercionales. Dada la heterogeneidad de los resultados, su uso hoy en día es controvertido, ya que cualquier beneficio producido por los corticosteroides parece ser superado por las posibles complicaciones potenciales(51).
El uso de plasma rico en plaquetas (PRP) se ha convertido en otra alternativa terapéutica. La evidencia científica actual no apoya de forma clara su uso en tendinopatía aquílea(52), ya que actualmente la mayoría de los estudios no establecen una mejoría clínica estadísticamente significativa. Yi-Jun Zhang(13) et al. han realizado un metaanálisis comparando el tratamiento de infiltraciones con PRP y con placebo (suero salino fisiológico –SSF–), ambos combinados con ejercicios excéntricos. Evaluaron la mejoría en la escala VISA-A, cambios en el grosor del tendón y en la actividad en la ecografía Doppler, sin encontrarse resultados estadísticamente significativos en ninguno de los parámetros estudiados.
La proloterapia(53) consiste en la inyección en la zona lesionada de una sustancia irritante (la más utilizada es la dextrosa hiperosmolar), que desencadena una respuesta inflamatoria local y estimula la reparación tisular. Además, disminuye la neovascularización que se produce en las tendinopatías no insercionales. Una reciente revisión sistemática(14) concluye que la proloterapia tiene resultados superiores o al menos comparables al tratamiento con ejercicios excéntrico, siendo una alternativa a considerar en el tratamiento de la patología no insercional.
El polidocanol(54) utilizado como terapia esclerosante (obliteración de la vascularización aberrante del tendón afecto), inyectado bajo control con ecografía Doppler sobre los vasos anormales en la cara ventral del tendón de Aquiles, ha demostrado resultados clínicos satisfactorios en escalas funcionales y de dolor. Un ensayo clínico aleatorizado(15), que compara el tratamiento con polidocanol y placebo y evalúa los resultados tras 6 meses de seguimiento, indica que se trata de un tratamiento seguro, pero ineficaz a medio plazo.
La EPI es la aplicación de corriente galvánica a través de una aguja conectada a un cátodo, con el fin de promover una respuesta inflamatoria y reparativa del tendón afecto. Este tratamiento produce además liberación de H2, que es un potente inhibidor de radicales libres y promueve el efecto analgésico(10). Ronzio(11) et al. realizaron un ensayo clínico comparando el tratamiento rehabilitador con este mismo tratamiento, pero asociado a EPI en pacientes con tendinopatía aquílea. Los resultados fueron significativos en cuanto a la disminución del dolor, el aumento del rango articular y la disminución de la rigidez matutina a favor del segundo grupo.
En la misma línea, se está preconizando la hidrodisección percutánea para la liberación de las adherencias formadas entre el tendón aquíleo y la grasa de Kager. Lulu He et al.(55) trataron a 3 pacientes mediante una técnica simple de hidrodisección de manera ambulatoria, liberando estas estructuras y restaurando la movilidad del tendón.
Tratamiento quirúrgico
El objetivo de la cirugía es restaurar la función previa del tendón. Este tipo de tratamientos suele estar indicado una vez agotado el tratamiento conservador. Se destaca el desarrollo en los últimos años de las técnicas mínimamente invasivas y endoscópicas, por ser procedimientos efectivos con menor morbilidad, tiempo quirúrgico y número de complicaciones(16).
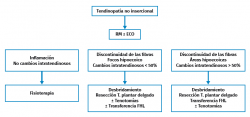
Entre las opciones de tratamiento quirúrgico de la tendinopatía no insercional del tendón de Aquiles destacamos (Figura 5)(56) el desbridamiento a cielo abierto de los nódulos y las adherencias, con o sin resección del paratendón(17). Cuando el desbridamiento del tendón es mayor del 50% se recomienda la aumentación con flexor hallucis longus (FHL). La literatura describe un 36-77% de buenos resultados(5,57), pero con un 19 a un 40% de complicaciones como: infecciones, necrosis cutánea, dehiscencia de la herida, cicatriz hipertrófica y/o dolorosa(18).
También podemos realizar este tipo de cirugías con técnicas endoscópicas. Descritas por Van Dijk(58,59), permiten la resección del paratendón y el desbridamiento del tendón, con una tasa de buenos resultados que oscilan entre el 67 y el 97%. Estas técnicas permiten eliminar la neovascularización y la inervación aberrante con una menor agresión de los tejidos blandos, un menor número de complicaciones (8,6-19%)(18) y una incorporación más rápida a las actividades deportivas(19,20). A este respecto, al realizar una incisión más pequeña, obtenemos una menor cantidad de tejido cicatricial y una disminución del dolor postoperatorio(18,21).
Se pueden asociar a las técnicas anteriores tenotomías longitudinales, siguiendo la dirección de las fibras del tendón de Aquiles, para promover la neovascularización y la reparación del tendón(18).
Con la transposición del FHL (Figura 6) el objetivo es conseguir una mejoría del dolor, sin pérdida de fuerza en la flexión plantar del hallux(22,60). Se describe en la literatura entre un 73 y un 90% de satisfacción en los pacientes intervenidos con esta técnica(22).
Van Sterkenburg y Van Dijk(59) describen la importancia del tendón plantar delgado en la tendinopatía de la porción media del tendón de Aquiles. En condiciones normales, el tendón plantar delgado se mueve libremente. Sin embargo, en el curso de la tendinopatía del tendón de Aquiles, se producen adherencias entre estas 2 estructuras. De hecho, hay autores que demuestran cambios histológicos similares a los que presenta el tendón de Aquiles(22,59). Por tanto, se recomienda la resección del tendón plantar delgado durante el tratamiento, ya que ayuda a aliviar los síntomas. En esta línea, se ha descrito la liberación percutánea del delgado plantar con EPI(10), con resultados prometedores sobre la liberación abierta, ya que disminuye el riesgo de complicación de la herida y permite una rehabilitación precoz.
Duthon et al. en 2011(61) asocian el alargamiento del gastrocnemio medial con una reducción de la carga sobre el tendón patológico, permitiendo la cicatrización y el alivio de los síntomas. Mejora los resultados de la tenolisis endoscópica y no afecta al sistema aquíleo-calcáneo-plantar en deportistas(62).
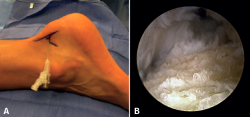
En el curso de la tendinopatía insercional, el 25% de los pacientes precisan tratamiento quirúrgico (Figura 7). La resección de la bursitis retrocalcánea y de la tuberosidad posterior del calcáneo o calcaneoplastia es una técnica que podemos realizar a cielo abierto o por vía endoscópica mediante un portal lateral de visión y un portal medial de trabajo. La indicación de esta técnica es retirar la bursa inflamada provocada por la fricción entre el calcáneo y el tendón de Aquiles aun en ausencia de tendinopatía(23) (Figuras 8A y B). Ante la existencia de tendinopatía, se puede llevar a cabo un desbridamiento con posterior reinserción del tendón de Aquiles, asociando o no la transposición del FHL(60). El riesgo de desinserción del tendón es bajo cuando el desbridamiento es menor del 50%; si fuera superior al 50%, se recomienda el reanclaje o la aumentación(63). Aunque se describen resultados excelentes en el 84,8% de los pacientes, con un bajo índice de complicaciones (10-15%), en el 25% de los casos no pudieron regresar a su nivel de actividad deportiva(17).
La transposición del FHL se suele asociar a pacientes con afectación importante del tendón de Aquiles, con altos requerimientos físicos, un índice de masa corporal elevado, en mayores de 50 años, con diabetes mellitus (DM), hipertensión arterial (HTA) y/o tratamiento crónico con corticoides. Así, Kenneth et al.(64) llevan a cabo un estudio de nivel I en pacientes mayores de 50 años con técnica a cielo abierto, obteniendo una mejora significativa de la fuerza en la flexión plantar, sin pérdida de fuerza en el hallux. Vega y Vila(16), en un estudio en roturas crónicas de tendón de Aquiles, realizan la transferencia de FHL asistida por endoscopia y sin resección del tejido cicatricial del tendón, proporcionando excelentes resultados con las ventajas de usar un procedimiento mínimamente invasivo. Sin embargo, es una técnica que requiere un nivel de experiencia elevado. La hipótesis que barajan los autores anteriores es que la vascularización del vientre muscular del FHL aumenta la perfusión del tendón de Aquiles dañado y el tejido del tendón cicatricial se reemplaza por un tendón sano o cercano a uno sano. Este fenómeno también se observa en las RM postoperatorias.
Finalmente, destacar la osteotomía de Zadek, consistente en una osteotomía de cierre con cuña dorsal, a la que se puede asociar la resección de la bursitis retrocalcánea y la exéresis de la tuberosidad posterosuperior del calcáneo. Esta técnica está reservada para casos seleccionados, sobre todo en aquellos con un ángulo de inclinación del calcáneo elevado (> 20°)(65) y en tendinopatías calcificantes insercionales(66). Aunque se describe un 96% de buenos resultados, este tratamiento ensancha el talón, precisa material de osteosíntesis con descarga postoperatoria y presenta mayor variabilidad en los resultados que la calcaneoplastia(23). Los estudios publicados sobre este procedimiento son limitados y es necesaria una investigación adicional.
Hay que insistir en el papel de la ecografía en la cirugía del tendón de Aquiles. El soporte de imagen, mediante esta técnica, durante las cirugías endoscópicas nos permite un mayor control de la cirugía, pues logramos una visión más completa si la comparamos con la obtenida exclusivamente con la cirugía endoscópica. De este modo, las lesiones yatrogénicas de las estructuras adyacentes o de la propia donde se está efectuando el proceso quirúrgico tienden a minimizarse(7). Igualmente y a tiempo real, nos permite una valoración diagnóstica del tendón de Aquiles que facilita una cirugía más precisa.
Conclusiones
La tendinopatía aquílea es una entidad de carácter multifactorial y con distintas expresiones clínicas, lo que dificulta el proceso diagnóstico y sobre todo el terapéutico.
El desarrollo de la ecografía la ha convertido en un elemento para el diagnóstico equiparable a la RM. Además, la capacidad de realizar estudios dinámicos con ecografía ha permitido su aplicación en tratamientos invasivos mediante punción y en la cirugía del tendón de Aquiles.
A pesar de la evolución de la ecografía, la RM sigue siendo un método útil para el diagnóstico de la patología del tendón de Aquiles, siendo especialmente eficaz en el proceso de identificación de las roturas parciales y completas, sobre todo de carácter crónico.
No obstante, conviene destacar que la primera opción terapéutica es la conservadora, indicando la cirugía en aquellos casos que no respondan a este tipo de tratamientos.
En esta línea, se destaca dentro del campo quirúrgico el desarrollo de las técnicas mínimamente invasivas y endoscópicas, con el objetivo de conseguir procedimientos efectivos, con menor morbilidad y con una recuperación funcional mas rápida.
Tablas
Tabla 2. Hallazgos en resonancia magnética de los distintos patrones patológicas del tendón de Aquiles
Figuras
Figura 3. Resonancia magnética de tobillo potenciada en T1. Corte sagital que muestra un tendón normal.
Figura 4. Corte sagital de resonancia magnética con rotura subaguda no insercional del tendón de Aquiles. Se muestra área de hiperintensidad entre los 2 cabos.
Figura 6. Transposición del flexor hallucis longus (FHL). Fijación en calcáneo con tornillo de biotenodesis.
Información del artículo
Cita bibliográfica
Autores
Néstor Antonio Zurita Uroz
Hospital IMED Elche. Alicante
Arthrosport. Zaragoza
Servicios Médicos. Real Federación Española de Natación
Servicio de Cirugía Ortopédica y Traumatología. Hospital IMED Elche. Alicante
Andrea Paniagua González
Unidad de Hombro y Codo. Hospital Fraternidad-Muprespa Habana. Madrid
Unidad de Hombro y Codo. Hospital Universitario Ramón y Cajal. Madrid
Ignacio Fernández Kelly
Hospital Monográfico Asepeyo Coslada. Madrid
Pablo Carnero Martín de Soto
Arthrosport Zaragoza
Instituto Malagueño de Traumatología del Deporte (IMATDE). Málaga
Hospital Regional de Málaga
Dolores Pilar Garrido Pozo
Unidad de Miembro Inferior. Hospital Fraternidad-Muprespa Habana. Madrid
Deborah González-García
Complejo Hospitalario Quirón Juan Bravo. Madrid
Unidad de Pie y Tobillo. Hospital Universitario de Guadalajara
Hospital ASEPEYO. Coslada. Madrid
Responsabilidades éticas
Conflicto de interés. El autor Néstor A. Zurita Uroz es compliance de Zimmer Biomet.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1O'Brien M. The anatomy of the Achilles tendon. Foot Ankle Clin. 2005 Jun;10(2):225-38.
-
2Soma CA, Mandelbaum BR. Achilles tendon disorders. Clin Sports Med. 1994;13(4):811-23.
-
3Silbernagel KG, Thomeé R, Thomeé P, Karlsson J. Eccentric overload training for patients with chronic Achilles tendon pain--a randomised controlled study with reliability testing of the evaluation methods. Scand J Med Sci Sports. 2001 Aug;11(4):197-206.
-
4Devereaux MD, Lachmann SM. Athletes attending a sports injury clinic--a review. Br J Sports Med. 1983;17(4):137-42.
-
5Van Dijk CN, van Sterkenburg MN, Wiegerinck JI, Karlsson J, Maffulli N. Terminology for Achilles tendon related disorders. Knee Surg Sports Traumatol Arthrosc. 2011 May;19(5):835-41.
-
6Jimenez Díaz. Ecografía musculoesquelética. 1.ª Edición. Marban; 2017. pp. 288-93.
-
7Smith J, Alfredson H, Masci L, Sellon JL, Woods CD. Sonographically Guided Plantaris Tendon Release: A Cadaveric Validation Study. PM R. 2019 Jan;11(1):56-63.
-
8Beyer R, Kongsgaard M, Hougs Kjær B, Øhlenschlæger T, Kjær M, Magnusson SP. Heavy Slow Resistance Versus Eccentric Training as Treatment for Achilles Tendinopathy: A Randomized Controlled Trial. Am J Sports Med. 2015 Jul;43(7):1704-11.
-
9Malliaras P, Barton CJ, Reeves ND, Langberg H. Achilles and patellar tendinopathy loading programmes: a systematic review comparing clinical outcomes and identifying potential mechanisms for effectiveness. Sports Med. 2013 Apr;43(4):267-86.
-
10Mattiussi G, Moreno C. Percutaneous electrochemical debridement of the Plantaris tendon: a novel option in the treatment of midportion Achilles tendinopathy. J Am Podiatr Med Assoc. 2018;108(5):437-41.
-
11Ronzio OA, Da Silva E, Soares MDR, Froes P. Effects of percutaneous microelectrolysis (MEP®) on pain, rom and morning stiffness in patients with Achilles tendinopathy. Eur J Physiother. 2017;19:62-3.
-
12Kearney RS, Parsons N, Metcalfe D, Costa ML. Injection therapies for Achilles tendinopathy. Cochrane Database Syst Rev. 2015 May 26;(5):CD010960.
-
13Zhang YJ, Xu SZ, Gu PC, et al. Is platelet-rich plasma injection effective for chronic Achilles tendinopathy? A meta-analysis. Clin Orthop Relat Res. 2018;476(8):1633-41.
-
14Sanderson LM, Bryant A. Effectiveness and safety of prolotherapy injections for management of lower limb tendinopathy and fasciopathy: a systematic review. J Foot and Ankle Res. 2015;8(1):57.
-
15Ebbesen BH, Molgaard CM, Olesen JL, Gregersen HE, Simonsen O. No beneficial effect of polidocanol treatment in Achilles tendinopathy: a randomized controlled trial. Knee Surg Sport Traumatol Arthrosc. 2018;26(7):2038-44.
-
16Vega J, Vilá J, Batista J, Malagelada F, Dalmau-Pastor M. Endoscopic Flexor Hallucis Longus Transfer for Chronic Noninsertional Achilles Tendon Rupture. Foot Ankle Int. 2018;39(12):1464-72.
-
17Leppilahti J, Karpakka J, Gorra A, Puranen J, Orava S. Surgical treatment of overuse injuries to the Achilles tendon. Clin J Sport Med. 1994;4:100-7.
-
18Chraim M, Alrabai HM, Krenn S, Bock P, Trnka HJ. Short-Term Results of Endoscopic Percutaneous Longitudinal Tenotomy for Noninsertional Achilles Tendinopathy and the Presentation of a Simplified Operative Method. Foot Ankle Spec. 2019 Feb;12(1):73-8.
-
19Maquirriain J. Surgical treatment of chronic Achilles tendinopathy: long-term results of the endoscopic technique. J Foot Ankle Surg. 2013;52:451-5.
-
20Maquirriain J, Ayerza M, Costa-Paz M, Muscolo DL. Endoscopic surgery in chronic Achilles tendinopathies: a preliminary report. Arthroscopy. 2002;18:298-303.
-
21Cerrato R, Switaj P . Using Arthroscopic Techniques for Achilles Pathology. Foot Ankle Clin North Am. 2017;22:781-99.
-
22Opdam KTM, Baltes TPA, Zwiers R, Wiegerinck JI, van Dijk CN. Endoscopic Treatment of Mid-Portion Achilles Tendinopathy: A Retrospective Case Series of Patient Satisfaction and Functional Outcome at a 2- to 8-Year Follow-up. Arthroscopy. 2018 Jan;34(1):264-9.
-
23Scholten PE, van Dijk CN. Endoscopic calcaneoplasty. Foot Ankle Clin. 2006 Jun;11(2):439-46.
-
24Maganaris CN, Narici MV, Almekinders LC, Maffulli N. Biomechanics and pathophysiology of overuse tendon injuries: ideas on insertional tendinopathy. Sports Med. 2004;34(14):1005-17.
-
25Kang S, Thordarson DB, Charlton TP. Insertional Achilles Tendinitis and Haglund’s Deformity. Foot Ankle Int. 2012 Jun;33(6):487-91.
-
26Pearce CJ, Tan A. Non-insertional Achilles tendinopathy. EFFORT Open Rev. 2017;1(11):383-90.
-
27Clement DB, Taunton JE, Smart GW. Achilles tendinitis and peritendinitis: etiology and treatment. Am J Sports Med. 1984;12(3):179-84.
-
28Kujala UM, Sarna S, Kaprio J. Cumulative incidence of Achilles tendon rupture and tendinopathy in male former elite athletes. Clin J Sport Med. 2005;15(3):133-5.
-
29Kvist M. Achilles tendon injuries in athletes. Sports Med. 1994;18(3):173-201.
-
30Iriarte I, Balius R, Cerezal L, Pedret C. Experto universitario en ecografía musculoesquelética. Universidad Francisco de Vitoria. Editorial Panamericana. Curso 2018-2019.
-
31Caudell GM. Insertional Achilles Tendinopathy. Clin Podiatr Med Surg. 2017;34:195-205.
-
32Stecco A, Busoni F, Stecco C, et al. Comparative ultrasonographic evaluation of the Achilles paratenon in symptomatic and asymptomatic subjects: an imaging study. Surg Radiol Anat. 2015 Apr;37(3):281-5.
-
33Cobos-Huerga C, Vega ML, Anguita G, Martín A. Lesiones del tendón de Aquiles. Diagnóstico por imagen. Rev Int Cienc Podol. 2011;5(2):35-45.
-
34Bäcker HC, Wong TT, Vosseller JT. MRI Assessment of Degeneration of the Tendon in Achilles Tendon Ruptures. Foot Ankle Int. 2019 Aug;40(8):895-9.
-
35Maffulli N, Via AG, Oliva F. Chronic Achilles Tendon Rupture. Open Orthop J. 2017 Jul 31;11:660-9.
-
36Paavola M, Kannus P, Paakkala T, Pasanen M, Järvinen M. Long-term prognosis of patients with Achilles tendinopathy. An observational 8-year follow-up study. Am J Sports Med. 2000 Sep-Oct;28(5):634-42.
-
37Loitz BJ, Zernicke RF, Vailas AC, Kody MH, Meals RA. Effects of short-term immobilization versus continuous passive motion on the biomechanical and biochemical properties of the rabbit tendon. Clin Orthop Relat Res. 1989 Jul;(244):265-71.
-
38Knobloch K, Schreibmueller L, Longo UG, Vogt PM. Eccentric exercises for the management of tendinopathy of the main body of the Achilles tendon with or without the AirHeel Brace. A randomized controlled trial. A: effects on pain and microcirculation. Disabil Rehabil. 2008;30(20-22):1685-91.
-
39Petersen W, Welp R, Rosenbaum D. Chronic Achilles tendinopathy: a prospective randomized study comparing the therapeutic effect of eccentric training, the AirHeel brace, and a combination of both. Am J Sports Med. 2007 Oct;35(10):1659-67.
-
40Maffulli N, Kader D. Tendinopathy of tendo achillis. J Bone Joint Surg Br. 2002 Jan;84(1):1-8.
-
41Donoghue OA, Harrison AJ, Coffey N, Hayes K. Functional data analysis of running kinematics in chronic Achilles tendon injury. Med Sci Sports Exerc. 2008 Jul;40(7):1323-35.
-
42Hertel J, Sloss BR, Earl JE. Effect of foot orthotics on quadriceps and gluteus medius electromyographic activity during selected exercises. Arch Phys Med Rehabil. 2005 Jan;86(1):26-30.
-
43Wilson F, Walshe M, O'Dwyer T, Bennett K, Mockler D, Bleakley C. Exercise, orthoses and splinting for treating Achilles tendinopathy: a systematic review with meta-analysis. Br J Sports Med. 2018 Dec;52(24):1564-74.
-
44Alfredson H, Pietilä T, Jonsson P, Lorentzon R. Heavy-load eccentric calf muscle training for the treatment of chronic Achilles tendinosis. Am J Sports Med. 1998 May-Jun;26(3):360-6.
-
45Mafi N, Lorentzon R, Alfredson H. Superior short-term results with eccentric calf muscle training compared to concentric training in a randomized prospective multicenter study on patients with chronic Achilles tendinosis. Knee Surg Sports Traumatol Arthrosc. 2001;9(1):42-7.
-
46Head H, Mallows A, Debenham J, Travers MJ, Allen L. The efficacy of loading programmes for improving patient-reported outcomes in chronic midportion Achilles tendinopathy: a systematic review. Musculoskeletal Care. 2019 Dec;17(4):283-99.
-
47Vitali M, Naim Rodriguez N, Pironti P, et al. ESWT and nutraceutical supplementation (Tendisulfur Forte) vs ESWT-only in the treatment of lateral epicondylitis, Achilles tendinopathy, and rotator cuff tendinopathy: a comparative study. J Drug Assess. 2019 May 3;8(1):77-86.
-
48Korakakis V, Whiteley R, Tzavara A, Malliaropoulos N. The effectiveness of extracorporeal shockwave therapy in common lower limb conditions: a systematic review including quantification of patient-rated pain reduction. Br J Sports Med. 2018 Mar;52(6):387-407.
-
49Suzuki T, Nakamura Y, Moriya T, Sasano H. Effects of steroid hormones on vascular functions. Microsc Res Tech. 2003;60:76-84.
-
50Johannsen F, Jensen S, Wetke E. 10-year follow-up after standardized treatment for Achilles tendinopathy. BMJ Open Sport Exerc Med. 2018;4(1).
-
51Coombes BK, Bisset L, Vicenzino B. Efficacy and safety of corticosteroid injections and other injections for management of tendinopathy: a systematic review of randomized controlled trials. Lancet. 2010;376(9754):1751-67.
-
52Poggio D, Álvarez C, García R. Evidencia de los nuevos tratamientos de la cirugía del pie y el tobillo. Monografía SEMCPT. 2017;9:3-12.
-
53Chan O, Havard B, Morton S, et al. Outcomes of prolotherapy por intratendinous Achilles tears: a case series. Muscles Ligaments Tendons J. 2017;7(1):78-87.
-
54Roche AJ, Calder JDF. Achilles tendinopathy: a review of the current concepts of treatment. Bone Joint J. 2013;95B:1299-307.
-
55He L, Genin J, Delzell P. Ultrasound diagnosis and percutaneous treatment of Achilles tendon tethering: a case series. Skeletal Radiol. 2016;45(9):1293-8.
-
56Reddy SS, Pedowitz DI, Parekh SG, Omar IM, Wapner KL. Surgical treatment for chronic disease and disorders of the Achilles tendon. J Am Acad Orthop Surg. 2009 Jan;17(1):3-14.
-
57Maffulli N, Binfield PM, Moore D, King JB. Surgical decompression of chronic central core lesions of the Achilles tendon. Am J Sports Med. 1999;27:747-52.
-
58Zwiers R, Wiegerinck JI, Van Dijk CN. Treatment of midportion Achilles tendinopathy: an evidence‑based overview. Knee Surg Sports Traumatol Arthrosc. 2016 Jul;24(7):2103-11.
-
59Van Sterkenburg MN, Kerkhoffs GM, van Dijk CN. Good outcome after stripping the plantaris tendon in patients with chronic mid-portion Achilles tendinopathy. Knee Surg Sports Traumatol Arthrosc. 2011;19:1362-6.
-
60Staggers JR, Smith K, de C Netto C, Naranje S, Prasad K, Shah A. Reconstruction for chronic Achilles tendinopathy: comparison of flexor hallucis longus (FHL) transfer versus V-Y advancement. Int Orthop. 2018 Apr;42(4):829-34.
-
61Duthon VB, Lubbeke A, Duc SR, Stern R, Assal M. Noninsertional Achilles tendinopathy treated with gastrocnemius lengthening. Foot Ankle Int. 2011;32:375-9.
-
62Kiewiet NJ, Holthusen SM, Bohay DR, Anderson JG. Gastrocnemius recession for chronic noninsertional Achilles tendinopathy. Foot Ankle Int. 2013;34:481-5.
-
63Shakked RJ, Raikin SM. Insertional Tendinopathy of the Achilles Debridement, Primary Repair, and When to Augment. Foot Ankle Clin North Am. 2017;22:761-80.
-
64Kenneth J, Cohen BE, Davis WH, Anderson RB, Jones CP. Surgical Treatment of Insertional Achilles Tendinopathy With or Without Flexor Hallucis Longus Tendon Transfer: A Prospective, Randomized Study. Foot Ankle Int. 2015;36(9):998-1005.
-
65López-Capdevila L, Santamaría Fumas A, Domínguez Sevilla A, et al. Osteotomía calcánea con cuña de sustracción dorsal como tratamiento quirúrgico en la tendinopatía insercional de Aquiles. Rev Esp Cir Ortop Traumatol. 2020;64(1):22-7.
-
66Mafulli N, Gougoulias N, D’Addona A, Oliva F, Maffulli GD. Modified Zadek Osteotomy without excision of the intratendinous calcific deposit is effective for the surgical treatment of calcific insertional Achilles tendinopathy. Surgeon. 2020 Oct 22:S1479-666X(20)30143-8.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- La lesión de tendón, del eterno olvidado a una patología de moda
- Fisiología y mecanobiología del tejido tendinoso y muscular
- Tendinopatía rotuliana: diagnóstico ecográfico y por resonancia magnética. Alternativas de tratamiento conservador y quirúrgico
- Fisiopatología, diagnóstico y tratamiento de la tendinopatía aquílea
- Tendinopatía del supraespinoso: diagnóstico ecográfico y por resonancia magnética. Alternativas de tratamiento conservador y quirúrgico
- Resultados de reparación artroscópica de tendón glúteo medio en pacientes afectos de síndrome de dolor trocantérico. Serie de casos
- Actualización en el diagnóstico y el tratamiento de las lesiones musculares del cuádriceps
- Manejo de las lesiones musculares del tríceps sural en deportistas adultos jóvenes y de mediana edad: revisión narrativa de la literatura
- Tendinopatía insercional del tendón de Aquiles. Tratamiento de principio a fin
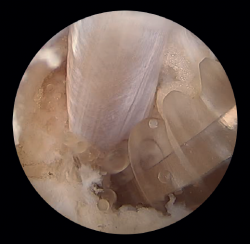
- Cíclope invertido
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.