Analgesia perioperatoria en cirugía artroscópica de rodilla
Perioperative analgesia in arthroscopic surgery of the knee
Resumen:
Un adecuado control del dolor perioperatorio es clave no solo para brindar al paciente un máximo bienestar tras el procedimiento, sino por la implicación que tiene este en el grado de satisfacción que se obtiene al final del proceso quirúrgico.
Debido a la variedad de opciones analgésicas y ante la falta de consenso sobre la técnica ideal para el control del dolor tras realizar una artroscopia de rodilla, se plantea una revisión de la literatura. El objetivo es evaluar las diferentes herramientas que existen en la actualidad en función de la evidencia.
Para optimizar los resultados y lograr un precoz control de la extremidad, se sugiere al paciente trabajar su masa muscular cuadricipital, a la vez que se recomienda la utilización de antiinflamatorios no esteroideos (AINE) inhibidores de la COX-2 durante el preoperatorio.
Para el momento quirúrgico, junto con las diferentes alternativas anestésicas, se recomienda la realización de bloqueos nerviosos periféricos. Entre los bloqueos recomendados se encuentran el del canal del aductor y del nervio femoral. La realización de infiltraciones anestésicas locales ha demostrado su beneficio no solo por el acceso a los compartimentos laterales y anterior de la rodilla, sino por la posibilidad de acceder a la cápsula articular posterior. A su vez, la utilización del ácido tranexámico mediante infiltración intraarticular o intravenoso permite disminuir los episodios de hemartrosis y, por lo tanto, el dolor postoperatorio.
Con el objetivo de disminuir el requerimiento de opioides intravenosos en el postoperatorio, el uso de protocolos de analgesia multimodal ha ido ganando terreno. Es así que, junto a los bloqueos nerviosos periféricos, la administración de AINE, los sistemas de analgesia controlada por el paciente, la utilización de agentes como el zolpidem y la crioterapia forman parte del esquema recomendado para un correcto control del dolor tras una artroscopia de rodilla.
Abstract:
Adequate perioperative pain control is essential not only to ensure maximum patient well-being after the procedure, but also in view of the influence it has upon patient satisfaction at the end of the surgical process.
Due to the variety of analgesic options and the lack of consensus regarding which technique is best suited for pain control after knee arthroscopy, we decided to conduct a literature review on the subject. The aim was to assess the different tools available, based on the existing evidence.
In order to optimise the outcomes and secure early control of the extremity, it is advisable for the patient to work his or her quadriceps muscle mass, together with the administration of COX-2 inhibiting non-steroidal anti-inflammatory drugs (NSAIDs) during the preoperative period.
At the time of surgery, and in addition to the different anaesthetic alternatives, the use of peripheral nerve blocks is advised. The recommended block procedures include adductor canal block and femoral nerve block. Local anaesthetic infiltrations have demonstrated benefit not only in terms of access to the lateral and anterior compartments of the knee, but also in allowing access to the posterior joint capsule. In turn, the use of tranexamic acid as an intraarticular infiltration or via the intravenous route is able to reduce episodes of haemarthrosis and therefore of postoperative pain.
The use of multimodal analgesia protocols has gained acceptance with the purpose of reducing the need for intravenous opioids in the postoperative period. Accordingly, these protocols, together with peripheral nerve blocks, the administration of NSAIDs, patient-controlled analgesia systems, the use of drugs such as zolpidem, and cryotherapy, currently form part of the recommended strategy for correct pain control following knee arthroscopy.
Introducción
El dolor no controlado es la complicación más frecuente tras una cirugía artroscópica de rodilla. La ausencia de un manejo óptimo del dolor puede causar un aumento de la morbilidad postoperatoria, una disminución de la satisfacción del paciente y tener una influencia negativa en el resultado final del procedimiento. Por lo tanto, el control del dolor postoperatorio es de suma importancia para los cirujanos ortopédicos(1).
Un mal manejo del dolor postoperatorio puede retrasar el alta del paciente, lo que resulta en una estancia hospitalaria prolongada y un mayor uso de los recursos sanitarios(2).
En la actualidad se dispone de varias técnicas para tratar el dolor que sigue a una cirugía artroscópica de rodilla; las más utilizadas incluyen el uso de opioides, agentes antiinflamatorios no esteroideos (AINE) y anestésicos como la lidocaína o la bupivacaína. Las estrategias menos utilizadas incluyen ketamina, ácido tranexámico (TXA), sedantes, gabapentinoides y corticosteroides(3).
Si bien históricamente los opiáceos y los opioides fueron el gold standard en el control del dolor postoperatorio, las complicaciones asociadas con el uso prolongado de narcóticos han cambiado el paradigma del manejo del dolor en la práctica ortopédica(4,5). El éxito de los regímenes multimodales ha sido bien documentado en la literatura en función de la cirugía protésica, dando como resultado puntuaciones de dolor más bajas en el postoperatorio inmediato e incluso hasta 1 año después del procedimiento(6,7).
El objetivo de esta revisión narrativa es resumir la información más relevante de la literatura actual sobre los distintos agentes involucrados en el manejo perioperatorio del dolor en la cirugía artroscópica de rodilla y establecer así recomendaciones claras, basadas en la evidencia, sobre las diferentes opciones disponibles.
Principios fisiológicos del dolor agudo
Los procedimientos quirúrgicos producen un aluvión de señales aferentes dolorosas, generando una respuesta inflamatoria secundaria, que contribuye sustancialmente al dolor postoperatorio. Estas señales tienen la capacidad de iniciar cambios prolongados, tanto en el sistema nervioso central como periférico, que conducirán a la amplificación y prolongación del dolor postoperatorio(8). Como resultado del proceso inflamatorio en el sitio quirúrgico podemos observar una sensibilización periférica, caracterizada por una reducción en el umbral nociceptivo de las terminales aferentes(9).
Valoración del dolor
La escala visual analógica (EVA), la escala numérica (EN) y la escala de clasificación verbal (ECV) están entre las comúnmente utilizadas para valorar la intensidad del dolor en contextos clínico-quirúrgicos y de investigación. Diferentes estudios han valorado la utilidad de cada una de las anteriores, encontrando sutiles diferencias entre ellas. Es necesario destacar que la EN es, de todas las anteriores, la que muestra mayor sensibilidad, siendo capaz de detectar diferencias entre sexo e intensidad del dolor(10).
Manejo del dolor preoperatorio
Definir objetivos y establecer expectativas
Una parte importante del control del dolor postoperatorio comienza mucho antes de la cirugía. Un estudio prospectivo mostró que los pacientes a quienes se mostraron vídeos que describían el tratamiento antes de la operación a las 6 semanas tenían significativamente menos dolor que aquellos a los que no se les mostraron(11). El reconocimiento preoperatorio y el tratamiento de la ansiedad y la depresión son importantes porque está bien establecido que estas condiciones pueden amplificar la percepción del dolor(12).
Analgesia preventiva
La analgesia preventiva comienza antes de la cirugía, con el objetivo de prevenir la sensibilización del sistema nervioso central y periférico secundaria a la incisión quirúrgica y la manipulación del tejido. La prevención de esta sensibilización puede mejorar el dolor postoperatorio del paciente y reducir el riesgo de desarrollo de dolor neuropático crónico(8). Los analgésicos preventivos deben ser relativamente fáciles de administrar, proporcionar un inicio rápido y tener un perfil de efectos adversos que no interfiera con el procedimiento quirúrgico planificado. Por lo general, los AINE, los inhibidores de la ciclooxigenasa-2 (COX-2) y el paracetamol se usan para este propósito y se administran en el área de espera preoperatoria 1 a 2 horas antes de comenzar el procedimiento quirúrgico(13).
Inhibidores de ciclooxigenasa-2
Trabajan a nivel periférico para prevenir la producción de prostaglandinas. Tienen un perfil de efectos adversos favorable, con riesgo reducido de úlceras gástricas y disfunción plaquetaria mínima en comparación con los AINE tradicionales, que son inhibidores inespecíficos de COX-1 y COX-2. Aunque se ha implicado a los inhibidores de la COX-2 en el aumento del riesgo de eventos cardiovasculares adversos, no se ha demostrado que dosis de celecoxib de hasta 400 mg al día aumenten este riesgo(14,15).
Paracetamol
Se cree que actúa a través de varias vías mediadas centralmente, incluso como agonista del receptor de cannabinoides, como inhibidor de la isoenzima COX-2 y como agonista del canal catiónico potencial del receptor transitorio, subfamilia V, miembro 1, un antinociceptor central(16).
Terapia física
La fuerza muscular preoperatoria es un factor importante que puede influir en los resultados postoperatorios. A los 1, 2 y 3 meses después de la reconstrucción del ligamento cruzado anterior (LCA), los pacientes con una fuerza preoperatoria > 90% al comparar la extremidad lesionada con la contralateral tenían una fuerza significativamente mejor que los pacientes con una fuerza preoperatoria < 75%. Evidencia de nivel 1 ha demostrado que la rehabilitación preoperatoria puede facilitar la recuperación postoperatoria(17).
Manejo del dolor intraoperatorio
Anestesia general y raquídea
La anestesia general se asocia con una reducción de la tensión de oxígeno tisular perioperatoria(18), así como náuseas, vómitos y delirio postoperatorios, que se evitan mediante el uso de anestesia raquídea(19). Sin embargo, la administración de anestesia raquídea requiere habilidad técnica en el procedimiento y, aunque generalmente es muy exitosa, se asocia con una tasa de fallo de aproximadamente un 4%, lo que requiere la conversión a una anestesia general(20). Se ha informado que la tasa de complicaciones de la anestesia raquídea es extremadamente baja (0,03%). Los efectos adversos más comunes incluyen hipotensión postoperatoria y retención urinaria(21).
Infiltración anestésica local (LIA)
La analgesia mediante infiltración local en forma de inyecciones intraarticulares (i.a.) o periarticulares (p.a.) proporciona otro medio para el control eficaz del dolor. Se ha demostrado que el uso de infiltraciones de anestésico local tiene un efecto significativo sobre la reducción en el nivel de dolor y el consumo de opioides después de la reconstrucción del LCA(22) y un efecto no significativamente diferente del de un bloqueo del nervio femoral (BNF) en varios estudios(23,24,25). Además, se demostró que la infiltración i.a. afecta menos a la fuerza del cuádriceps que el BNF(26).
Existen distintas combinaciones de medicación, pero la más utilizada habitualmente es lidocaína, bupivacaína, ketorolaco y morfina(22).
La LIA p.a. e i.a. es efectiva para reducir el dolor postoperatorio después de la cirugía de reconstrucción del LCA y puede desempeñar un papel vital en los regímenes multimodales de control del dolor. En un ensayo clínico aleatorizado (ECA) llevado a cabo por Koh et al., se aleatorizaron 100 pacientes en 5 grupos: 1) grupo de control sin inyección; 2) grupo de ropivacaína i.a.; 3) cóctel de fármacos multimodal (CFM) i.a.; 4) inyección p.a. de CFM; y 5) inyección i.a. + p.a. de CFM. Se distribuyeron 5 inyecciones p.a. en el periostio alrededor de las áreas de extracción tendinosa, incisión, retículo del tendón rotuliano, almohadilla grasa infrapatelar y en el periostio y la fascia alrededor del túnel tibial. Observaron una reducción significativa del dolor en la primera noche postoperatoria en el grupo p.a. CFM y el i.a. + p.a. CFM, en comparación con las otras 3 cohortes (p < 0,001). Este estudio sugirió que las inyecciones p.a. pueden ser más beneficiosas que las inyecciones i.a. para el control del dolor perioperatorio(27).
Manguito de isquemia
Se ha investigado el papel del manguito de isquemia en el desarrollo de dolor postoperatorio. Las variables principales en estas investigaciones son la duración de su utilización y la presión del torniquete(28). La isquemia conduce a hipoxia tisular y acidosis, proporcional a la duración(29). Los tiempos de torniquete superiores a 2 horas pueden resultar en un síndrome postorniquete con edema, rigidez, palidez, debilidad y entumecimiento subjetivo, que generalmente se resuelve en 1 semana. También se pueden observar complicaciones menores, como debilidad del cuádriceps, que probablemente sea multifactorial(30).
Ácido tranexámico
El TXA se ha mostrado prometedor para reducir la intensidad del dolor y la incidencia de hemartrosis en el periodo postoperatorio temprano después de una artroscopia de rodilla. El TXA, un derivado antifibrinolítico sintético de la lisina, inhibe competitivamente la fibrinólisis y estabiliza la formación de coágulos(31). Aunque en la práctica actual existen varios regímenes de dosificación para el TXA intravenoso (i.v.), estudios recientes han informado que los efectos hemostáticos y analgésicos deseados se logran usando dosis de 10 y 15 mg/kg(32,33). Se ha demostrado que tanto la administración i.a. como i.v. disminuyen significativamente el dolor y el volumen de derrame de la articulación de la rodilla sin aumentar el riesgo de eventos tromboembólicos. Además, la administración i.a. e i.v. son comparables en términos de eficacia, con puntuaciones similares en la EVA a las semanas 1.ª y 2.ª postoperatorias(34).
Manejo del dolor postoperatorio
Analgesia multimodal
Con la disminución de la utilización de opioides, asociada a un cambio en el paradigma del tratamiento del dolor hacia un enfoque multimodal, se han desarrollado y probado múltiples combinaciones y regímenes de agentes analgésicos.
La analgesia multimodal se refiere a la combinación de varios tipos de medicamentos y vías de administración, incluido el bloqueo de nervios periféricos (BNP), la inyección p.a., la analgesia controlada por el paciente (PCA) y medicamentos por vía oral, opioides y no opioides. El objetivo de la analgesia multimodal es proporcionar un control superior del dolor postoperatorio mediante la modulación simultánea de varias vías de dolor y minimizar los efectos adversos no deseados del consumo excesivo de opioides(35).
Un estudio multicéntrico reciente comparó diferentes enfoques en el manejo del dolor después de la reconstrucción del LCA en términos de dolor subjetivo medido a través de la EVA, el consumo de opioides, tasas de alta tardía y complicaciones. Los procedimientos analgésicos incluidos fueron BNF continuo y de dosis única, y analgesia con técnica LIA p.a. o i.a. Además, también se comparó el uso de AINE y corticosteroides i.v. Los pacientes que recibieron AINE tenían menos probabilidades de tener un retraso en el alta y el uso de dexametasona se asoció con una disminución del consumo de opioides y menos efectos secundarios de los agentes de bloqueo nervioso(35).
Opiáceos y opioides
Los opiáceos y sus análogos sintéticos, los opioides, se encontraban entre las modalidades de control del dolor más populares utilizadas en el periodo postoperatorio agudo para una gran variedad de procedimientos ortopédicos.
Como analgésicos, los opioides inhiben la conducción de las señales de dolor a través de la activación de estos receptores mediante varios métodos de administración.
Si bien los opioides se empleaban anteriormente con mayor frecuencia como principal medida de control del dolor después de una cirugía artroscópica de rodilla, como puede ser una reconstrucción del LCA, la posibilidad de generar adicción o abuso, su adicción asociada, los síntomas de abstinencia al suspenderlos después de un uso prolongado y otros efectos secundarios desagradables, como la disminución de la motilidad intestinal, han cambiado el paradigma del manejo del dolor en los últimos años a un enfoque más multimodal(36).
No obstante, los medicamentos opiáceos todavía se emplean con frecuencia como una medida para tratar el dolor irruptivo dentro de la primera semana después de la cirugía de reconstrucción del LCA, especialmente cuando el dolor del paciente no se maneja con éxito por medios alternativos. Los opioides que se recetan con más frecuencia incluyen tramadol y, con menos frecuencia, morfina(37).
Varios estudios han explorado los factores de riesgo involucrados en el uso prolongado de opioides después de la cirugía de LCA, entre los que destaca un metaanálisis realizado en 9.474 militares estadounidenses que tomaban medicamentos opioides después de la reconstrucción del LCA. Este reveló que el 28% de la población del estudio continuó tomando opioides durante más de 90 días e identificó que la cantidad y la frecuencia de prescripciones pre- y perioperatorias era el factor de riesgo más importante en el uso postoperatorio prolongado de opioides(38).
Dado el riesgo de dependencia del paciente, el paradigma actual del manejo del dolor se ha desplazado en los últimos años hacia un mayor enfoque en los regímenes multimodales.
Bloqueos nerviosos periféricos
La cirugía artroscópica de rodilla se realiza con mayor frecuencia en el entorno ambulatorio. Como tal, proporcionar un control adecuado del dolor para el alta oportuna y la satisfacción del paciente es fundamental para optimizar la atención y reducir costos innecesarios asociados con un retraso del alta o reingreso del paciente(39). Los BNP se implementan cada vez más como control del dolor perioperatorio. Los beneficios de los BNP incluyen una disminución del consumo de opioides intra- y postoperatorio, un mejor control del dolor postoperatorio y una disminución de la fatiga y las náuseas que se asocian con otras formas orales de control del dolor. Los efectos secundarios de los BNP son raros, pero incluyen un pequeño riesgo de lesión nerviosa y debilidad muscular prolongada(40).
Los bloqueos nerviosos más utilizados son los bloqueos femorales, del canal aductor y ciático(41).
Bloqueo del nervio femoral
Excluyendo la cápsula posterior, la articulación de la rodilla está inervada por el nervio femoral, lo que lleva a muchos cirujanos a adoptar BNF para la analgesia postoperatoria(42).
Este bloqueo se dirige al nervio femoral en el canal femoral y depende de la difusión del anestésico local para bloquear los nervios femorales, femoral lateral cutáneo y obturador. Tradicionalmente, se ha realizado mediante estimulación nerviosa, pero ahora se utiliza cada vez más la ecografía para reducir la tasa de bloqueo fallido y punción arterial o intraneural inadvertida. Este es un bloqueo mixto (sensitivo y motor), por lo que produce entumecimiento de las caras anterior, lateral y medial del muslo, lo que causa una debilidad profunda del cuádriceps. Cuando se realiza este bloqueo, el paciente se coloca en decúbito supino y se utiliza ecografía para identificar el nervio en la confluencia de los músculos ilíaco y psoas. La ecografía también se utiliza para visualizar el anestésico local inyectado debajo y alrededor del nervio femoral(43).
En un ECA de pacientes sometidos a reconstrucciones del LCA bajo anestesia espinal con o sin BNF, los pacientes que habían recibido bloqueo reportaron valores de dolor más bajos, que solo fueron significativos a las 6 horas (p = 0,007). Sin embargo, después del alta hospitalaria, se observó que los pacientes que tenían un BNF presentaron mayor dolor, a medida que disminuía el efecto de bloqueo(44).
Al comparar el BNF con otros modos de analgesia, los estudios no han encontrado pruebas de su superioridad. En una revisión sistemática del uso del bloqueo femoral en la reconstrucción del LCA, Mall y Wright no encontraron evidencia de que proporcione un beneficio adicional sobre la analgesia multimodal(45).
Varios estudios han sugerido que los BNF pueden afectar la fuerza y la función de la rodilla durante un periodo prolongado más allá del postoperatorio inmediato(46,47,48). La prevalencia de déficits neurológicos transitorios o incluso permanentes se estima en un 1,94%(49).
Bloqueo del canal aductor
Se dirige principalmente a los nervios sensitivos en el canal aductor mientras reduce el grado de debilidad del cuádriceps. Incluye el nervio safeno, las ramas articulares del nervio obturador, el nervio retinacular medial y el nervio del vasto interno, que es el único nervio motor involucrado.
Esta técnica da como resultado un bloqueo sensitivo de la cara anteromedial de la rodilla, a nivel del polo superior de la rótula y la parte medial de la pierna, con una pérdida mínima de la fuerza del cuádriceps. El bloqueo se realiza colocando al paciente en decúbito supino, con el ecógrafo aplicado en la cara medial del muslo a nivel medio-distal, 2 a 3 cm proximal al hiato del aductor. La arteria y la vena femoral se localizan profundamente al músculo sartorio, con el nervio safeno lateral a ellas a este nivel, y se inyecta anestésico local alrededor del nervio(50).
En un ECA, Abdallah et al. resumieron que el bloqueo del canal aductor es una modalidad analgésica superior al BNF en pacientes sometidos a reconstrucción del LCA, ya que proporciona una analgesia postoperatoria eficaz al tiempo que produce menos debilidad del cuádriceps(51).
Infusión continua en bloqueos nerviosos
Se pueden aplicar catéteres para proporcionar un bloqueo continuo del nervio femoral, inyección i.a. o infiltración de la herida. Se ha demostrado que el uso de estos catéteres proporciona un alivio eficaz del dolor después de la reconstrucción del LCA y una rehabilitación física temprana mejorada(52,53).
En contraposición con lo hallado en los estudios mencionados anteriormente, diferentes trabajos concluyen que esta técnica no ofrece ninguna ventaja clínica, lo que se suma a una considerable tasa de complicaciones, que alcanza el 13%(54).
Antiinflamatorios no esteroideos e inhibidores selectivos de la COX-2
Los fármacos AINE se utilizan habitualmente como analgésicos en ortopedia y regularmente en protocolos de manejo del dolor postoperatorio multimodal para cirugía del LCA(55).
Numerosos estudios han investigado su eficacia como analgésico postoperatorio y lo han demostrado como un método de tratamiento eficaz y seguro(56,57).
En un ECA triple ciego, Mardani-Kivi et al. encontraron que el uso de celecoxib como analgesia preventiva después de la reconstrucción del LCA redujo la intensidad del dolor y el consumo de opioides en el grupo de celecoxib a las 6 y 24 h después de la cirugía (p < 0,0001)(58). Además, los AINE son asociados con menos efectos secundarios como náuseas y vómitos, y una mejor tolerancia entre los pacientes en comparación con otros analgésicos postoperatorios(59,60).
Estudios anteriores han sugerido que el uso de AINE puede tener efectos adversos sobre la recuperación y la curación después de procedimientos ortopédicos(61,62). Sin embargo, otros estudios no han observado efectos negativos con el uso de AINE e inhibidores selectivos de la COX-2 sobre la cicatrización de tejidos blandos y tendones(63). Los estudios que investigaron el uso de AINE en la reparación del LCA, hombro/labrum y menisco tampoco encontraron diferencias en la tasa de curación relacionada con el uso de AINE en el postoperatorio(63,64).
Ketamina
La ketamina es un fármaco derivado de la fenciclidina y presenta una acción antagonista sobre los receptores de N-metil-D-aspartato (NMDA)(65).
En un estudio prospectivo aleatorizado, Zhu et al. evaluaron el efecto analgésico de mezclar ketamina con ropivacaína en bloqueos del nervio ciático y femoral combinados guiados por ecografía (BNCF)(66). Los resultados en la escala del dolor fueron significativamente más bajos para el grupo RNK (ropivacaína + ketamina perineural) en comparación con el grupo RIK (ropivacaína + ketamina i.v.) y el grupo R (ropivacaína aislada) a las 20 y 24 horas postoperatorias (p = 0,001). Además, el grupo RNK mostró un tiempo más prolongado hasta requerir la primera dosis de analgésico (p = 0,014) en comparación con los otros 2 grupos, lo que sugiere que la ketamina perineural mejora el efecto antinociceptivo del BNCF(66).
Sedantes y corticoides
Aunque se emplean con menos frecuencia en la práctica clínica, los sedantes, la gabapentina y los corticosteroides se han explorado como medios alternativos para el manejo del dolor en la artroscopia de rodilla. Los sedantes descritos en el tratamiento del dolor postoperatorio después de la reconstrucción del LCA son típicamente de la clase no benzodiacepínica, incluidos agentes como el zolpidem(67).
Se ha demostrado que los pacientes que reciben 10 mg de zolpidem todas las noches durante la primera semana postoperatoria tienen una reducción del 28% en el consumo de opioides(68).
La gabapentina y la pregabalina se han utilizado como agentes anticonvulsivos y analgésicos, especialmente en casos en los que se cree que el dolor es de origen neuropático(69,70).
La gabapentina administrada preoperatoriamente se ha estudiado como agente potencial en el tratamiento del dolor multimodal. Se han realizado ECA con el uso de 150 mg de pregabalina pre- y postoperatoria, y se ha demostrado una reducción del dolor subjetivo medido por la escala EVA y el consumo postoperatorio de opioides(71). Sin embargo, estos resultados están en conflicto con otro ECA sobre el uso de pregabalina pre- y postoperatoria en las reconstrucciones del LCA, que indicó que el fármaco no era mejor que el placebo con respecto a la reducción del dolor postoperatorio y el consumo de opioides(72).
Dado el riesgo de inmunosupresión y otros efectos secundarios, el papel de los corticosteroides en el control del dolor es relativamente limitado en la cirugía artroscópica de rodilla. Se ha demostrado que el uso de AINE junto con 8 mg de dexametasona i.v. postoperatoriamente después de la reconstrucción del LCA es superior para reducir el dolor que los AINE solos(73). Además, agregar de 1 a 4 mg de dexametasona a la solución de bupivacaína cuando se realiza un bloqueo del nervio safeno subsartorial aumenta potencialmente la duración del bloqueo hasta en 13 horas(73).
Analgesia controlada por el paciente
La PCA es una opción para el manejo del dolor postoperatorio en la artroscopia de rodilla, ya que proporciona un alivio del dolor simple, rápido y adecuado. Se puede administrar a través de diferentes vías y requiere de un alto grado de colaboración por parte del paciente. El dispositivo se programa según el analgésico utilizado, las características físicas y el dolor basal de los pacientes. Los pacientes pueden administrar una pequeña cantidad de analgésico presionando el botón cuando más lo necesitan. Por lo general, los opioides que se usan en PCA son morfina, fentanilo y tramadol(74).
A pesar de que esta técnica se asocia con algunos efectos adversos como náuseas, vómitos, depresión respiratoria y retención urinaria, estos son menos graves que los provocados por el tratamiento convencional con opioides. Por lo tanto, se considera que la PCA es segura y eficaz para tratar el dolor postoperatorio de moderado a intenso(75).
Crioterapia
El efecto de la crioterapia postoperatoria se ha evaluado en varios ECA y aproximadamente la mitad informó una disminución de los síntomas de dolor(76). La crioterapia preoperatoria(77), así como la crioterapia y la compresión combinadas(78), también demostraron efectos beneficiosos. Se cree que el efecto de la terapia de frío es el resultado de la disminución de la hinchazón de los tejidos blandos y los espasmos musculares, así como un efecto sobre el umbral del dolor(79). Una complicación informada causada por la aplicación prolongada de hielo en la rodilla es la parálisis del nervio peroneo. Esas parálisis informadas fueron todas transitorias y se resolvieron espontáneamente(80).
Dispositivos de movilidad pasiva continua
El uso de dispositivos de movimiento pasivo continuo (CPM) para el alivio del dolor postoperatorio es controvertido. Hay estudios que demuestran una disminución del uso de narcóticos en pacientes tratados con CPM(81,82) y otro que no mostró ningún efecto sobre el uso de analgésicos(83). Múltiples estudios han demostrado que el uso de un CPM no afecta a la amplitud de movimiento ni a la laxitud anterior después de la reconstrucción del LCA(84). Dado el costo asociado con la CPM y la falta de efecto sobre los resultados funcionales generales, es difícil justificar su uso como un simple complemento de control del dolor sin evidencia de apoyo definitiva de nivel 1(85).
Electroestimulación nerviosa transcutánea (TENS)
La TENS es otra modalidad complementaria para el control del dolor. En el sistema nervioso central, la TENS activa áreas en el tronco del encéfalo y la médula espinal que contienen receptores de serotonina, muscarínicos y opioides(86).
Tras una artroscopia de rodilla, los pacientes que usaron TENS durante un promedio de 4 días tuvieron una disminución del dolor postoperatorio que fue significativa al segundo día y recuperaron la movilidad preoperatoria, la fuerza isocinética en flexión y extensión, y el volumen de la pierna 1 mes antes que los pacientes tratados con placebo(87).
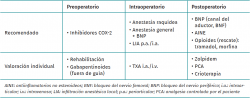
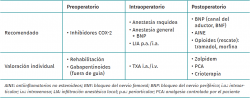
Se presenta en la Tabla 1 un resumen basado en lo detallado durante esta revisión narrativa sobre el control del dolor perioperatorio en la cirugía artroscópica de rodilla.
Conclusiones
El manejo óptimo del dolor postoperatorio después de la cirugía artroscópica de rodilla sigue siendo un tema controvertido sin un enfoque ampliamente aceptado.
Basándonos en la presente revisión, podemos realizar las siguientes recomendaciones:
- La rehabilitación preoperatoria puede facilitar la recuperación postoperatoria.
- La administración preventiva, en el periodo preoperatorio, de inhibidores de la COX-2 y gabapentinoides es efectiva en disminuir el dolor tras una artroscopia de rodilla.
- La utilización de LIA p.a. e i.a. es efectiva para reducir el dolor postoperatorio y puede desempeñar un papel vital en los regímenes multimodales de control del dolor.
- El nuevo enfoque se orientaría hacia protocolos de analgesia multimodal con el objetivo de mejorar el control del dolor en el postoperatorio inmediato con combinaciones de diferentes fármacos a bajas dosis.
- El cambio en el paradigma del control del dolor trata de evitar el incremento y potencial abuso de opioides y opiáceos.
- Los BNP son la medida analgésica más efectiva, por lo que deberían ser considerados la técnica de referencia. Se recomienda optar por un bloqueo del canal aductor para evitar la debilidad de cuádriceps que produciría un bloqueo femoral.
- El TXA ha mostrado resultados prometedores para reducir la incidencia de hemartrosis y la gravedad del dolor en el periodo postoperatorio temprano después de una artroscopia de rodilla.
Como en toda cirugía ortopédica, la elección de los protocolos analgésicos debe ser individualizada, buscando la mayor efectividad con la menor tasa de efectos adversos y complicaciones.
Información del artículo
Cita bibliográfica
Autores
Maximiliano Ibañez
Hospital Universitario Quirón Dexeus. Barcelona
Laura Valls
Hospital Universitario de Igualada. Barcelona
Sergi Gil
Hospital Universitario de Igualada. Barcelona
Juan Ignacio Erquicia
Hospital Universitario de Igualada. Barcelona
iMove Traumatología. Clínica Mi Tres Torres. Barcelona
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de interés.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Chmielewski TL, Jones D, Day T, Tillman SM, Lentz TA, George SZ. The association of pain and fear of movement/reinjury with function during anterior cruciate ligament reconstruction rehabilitation. J Orthop Sports Phys Ther. 2008;38(12):746-53.
-
2United States Acute Pain Management Guideline Panel: Acute Pain Management: Operative or Medical Procedures and Trauma. Pub. no. 92-0032. Rockville, Maryland: United States Department of Health and Human Services, Public Health Service Agency for Health Care Policy and Research; 1992.
-
3Davey MS, Hurley ET, Anil U, et al. Pain Management strategies after anterior cruciate ligament reconstruction: a systematic review with network meta-analysis. Arthroscopy. 2021;37(4):1290-300.
-
4Malige A, Bram JT, Maguire KJ, McNeely LW, Ganley TJ, Williams BA. Decreased prescribing of postoperative opioids in pediatric ACL reconstruction: treatment trends at a single center. Orthop J Sports Med. 2021;9(2):2325967120979993.
-
5Morris BJ, Mir HR. The opioid epidemic: impact on orthopaedic surgery. JAAOS. 2015;23(5):267-71.
-
6Moucha CS, Weiser MC, Levin EJ. Current strategies in anesthesia and analgesia for total knee arthroplasty. J Am Acad Orthop Surg. 2016;24:60-73.
-
7Gaffney CJ, Pelt CE, Gililland JM, Peters CL. Perioperative pain management in hip and knee arthroplasty. Orthop Clin North Am. 2017;48:407-19.
-
8Woolf CJ, Chong MS. Preemptive analgesia — treating postoperative pain by preventing the establishment of central sensitization. Anesth Analg. 1993;77:362-79.
-
9Raja SN, Meyer RA, Campbell JN. Peripheral mechanisms of somatic pain. Anesthesiology. 1988;68:571-90.
-
10Ferreira Valente MA, Pais Ribeiro JL, Jensen MP. Validity of four pain intensity rating scales. Pain. 2011;152(10):2399-404.
-
11Maddison R, Prapavessis H, Clatworthy M. Modeling and rehabilitation following anterior cruciate ligament reconstruction. Ann Behav Med. 2006;31(1):89-98.
-
12Von Korff M, Simon G. The relationship between pain and depression. Br J Psychiatry Suppl. 1996;30:101-8.
-
13Jianda X, Yuxing Q, Yi G, Hong Z, Libo P, Jianning Z. Impact of preemptive analgesia on inflammatory responses and rehabilitation after primary total knee arthroplasty: a controlled clinical study. Sci Rep. 2016;6:30354.
-
14Graham DJ. COX-2 inhibitors, other NSAIDs, and cardiovascular risk: the seduction of common sense. JAMA. 2006;296(13):1653-6.
-
15Bhala N, Emberson J, Merhi A, et al. Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs: meta-analyses of individual participant data from randomized trials. Lancet. 2013;382(9894):769-79.
-
16Mallet C, Barrière DA, Ermund A, et al. TRPV1 in brain is involved in acetaminophen-induced antinociception. PLoS One. 2010;5(9):e12748.
-
17Shelbourne KD, Wilckens JH, Mollabashy A, DeCarlo M. Arthrofibrosis in acute anterior cruciate ligament reconstruction. The effect of timing of reconstruction and rehabilitation. Am J Sports Med. 1991;19(4):332-6.
-
18Treschan TA, Taguchi A, Ali SZ, et al. The effects of epidural and general anesthesia on tissue oxygenation. Anesth Analg. 2003;96(6):1553-7.
-
19Pugely AJ, Martin CT, Gao Y, Mendoza-Lattes S, Callaghan JJ. Differences in shortterm complications between spinal and general anesthesia for primary total knee arthroplasty. J Bone Joint Surg Am. 2013;95(3):193-9.
-
20Fettes PD, Jansson JR, Wildsmith JA. Failed spinal anaesthesia: mechanisms, management, and prevention. Br J Anaesth. 2009;102(6):739-48.
-
21Horlocker TT. Complications of regional anesthesia and acute pain management. Anesthesiol Clin. 2011;29(2):257-78.
-
22Tetzlaff JE, Dilger JA, Abate J, Parker RD. Preoperative intra-articular morphine and bupivacaine for pain control after outpatient arthroscopic anterior cruciate ligament reconstruction. Reg Anesth Pain Med. 1999 May-Jun;24(3):220-4.
-
23Kristensen PK, Pfeiffer-Jensen M, Storm JO, Thillemann TM. Local infiltration analgesia is comparable to femoral nerve block after anterior cruciate ligament reconstruction with hamstring tendon graft: a randomized controlled trial. Knee Surg Sports Traumatol Arthrosc. 2014 Feb;22(2):317-23.
-
24Mayr HO, Entholzner E, Hube R, Hein W, Weig TG. Pre- versus postoperative intraarticular application of local anesthetics and opioids versus femoral nerve block in anterior cruciate ligament repair. Arch Orthop Trauma Surg. 2007 May;127(4):241-4.
-
25Mehdi SA, Dalton DJ, Sivarajan V, Leach WJ. BTB ACL reconstruction: femoral nerve block has no advantage over intraarticular local anaesthetic infiltration. Knee Surg Sports Traumatol Arthrosc. 2004 May;12(3):180-3.
-
26Iamaroon A, Tamrongchote S, Sirivanasandha B, et al. Femoral nerve block versus intra-articular infiltration: a preliminary study of analgesic effects and quadriceps strength in patients undergoing arthroscopic anterior cruciate ligament reconstruction. J Med Assoc Thai. 2016 May;99(5):578-83.
-
27Koh IJ, Chang CB, Seo ES, Kim SJ, Seong SC, Kim TK. Pain management by periarticular multimodal drug injection after anterior cruciate ligament reconstruction: a randomized, controlled study. Arthroscopy. 2012;28(5):649-57.
-
28Wakai A, Winter DC, Street JT, Redmond PH. Pneumatic tourniquets in extremity surgery. J Am Acad Orthop Surg. 2001;9(5):345-35.
-
29Flatt AE. Tourniquet time in hand surgery. Arch Surg. 1972;104(2):190-2.
-
30Saunders KC, Louis DL, Weingarden SI, Waylonis GW. Effect of tourniquet time on postoperative quadriceps function. Clin Orthop Relat Res. 1979;(143):194-9.
-
31Lin ZX, Woolf SK. Safety, efficacy, and cost-effectiveness of tranexamic acid in orthopedic surgery. Orthopedics. 2016;39(2):119-30.
-
32Chiang ER, Chen KH, Wang ST, et al. Intra-articular injection of tranexamic acid reduced postoperative hemarthrosis in arthroscopic anterior cruciate ligament reconstruction: a prospective randomized study. Arthroscopy. 2019;35(7):2127-32.
-
33Felli L, Revello S, Burastero G, et al. Single intravenous administration of tranexamic acid in anterior cruciate ligament reconstruction to reduce postoperative hemarthrosis and increase functional outcomes in the early phase of postoperative rehabilitation: a randomized controlled trial. Arthroscopy. 2019;35(1):149-57.
-
34Ma R, Wu M, Li Y, et al. The comparative efficacies of intravenous administration and intra-articular injection of tranexamic acid during anterior cruciate ligament reconstruction for reducing postoperative hemarthrosis: a prospective randomized study. BMC Musculoskelet Disord. 2021;22(1):114.
-
35Baverel L, Cucurulo T, Lutz C, et al. Anesthesia and analgesia methods for outpatient anterior cruciate ligament reconstruction. Orthop Traumatol Surg Res. 2016;102(8s):S251-s255.
-
36Soffin EM, Waldman SA, Stack RJ, Liguori GA. An evidence-based approach to the prescription opioid epidemic in orthopedic surgery. Anesth Analg. 2017;125(5):1704-13.
-
37Beck JJ, Cline K, Sangiorgio S, Serpa R, Shifflett KA, Bowen RE. Prospective Study of acute opioid use after adolescent anterior cruciate ligament reconstruction shows no effect from patient- or surgical-related factors. J Am Acad Orthop Surg. 2020;28(7):293-300.
-
38Anderson AB, Balazs GC, Brooks DI, Potter BK, Forsberg JA, Dickens JF. Prescription patterns and risk factors for prolonged opioid dependence in elective anterior cruciate ligament reconstruction in a military population. Orthop J Sports Med. 2020;8(6):2325967120926489.
-
39Jansson H, Narvy SJ, Mehran N. Perioperative pain management strategies for anterior cruciate ligament reconstruction. JBJS Rev. 2018;6(3):e3.
-
40Vorobeichik L, Brull R, Joshi GP, Abdallah FW. Evidence basis for regional anesthesia in ambulatory anterior cruciate ligament reconstruction: part I-femoral nerve block. Anesth Analg. 2019;128(1):58-65.
-
41Min H, Ouyang Y, Chen G. Anterior cruciate ligament reconstruction with the use of adductor canal block can achieve similar pain control as femoral nerve block. Knee Surg Sports Traumatol Arthrosc. 2020;28(8):2675-86.
-
42Williams BA, Kentor ML, Vogt MT, et al. Reduction of verbal pain scores after anterior cruciate ligament reconstruction with 2-day continuous femoral nerve block: a randomized clinical trial. Anesthesiology. 2006;104(2):315-27.
-
43American Society of Anesthesiologists Task Force on Acute Pain Management: Practice guidelines for acute pain management in the perioperative setting: An updated report by the American Society of Anesthesiologists Task Force on Acute Pain Management. Anesthesiology. 2012;116(2):248-73.
-
44Astur DC, Aleluia V, Veronese C, et al. A prospective double blinded randomized study of anterior cruciate ligament reconstruction with hamstrings tendon and spinal anesthesia with or without femoral nerve block. Knee. 2014 Oct;21(5):911-5.
-
45Mall NA, Wright RW. Femoral nerve block use in anterior cruciate ligament reconstruction surgery. Arthroscopy. 2010 Mar;26(3):404-16.
-
46Magnussen RA, Pottkotter K, Stasi SD, et al. Femoral nerve block after anterior cruciate ligament reconstruction. J Knee Surg. 2017 May;30(4):323-8.
-
47Luo TD, Ashraf A, Dahm DL, Stuart MJ, McIntosh AL. Femoral nerve block is associated with persistent strength deficits at 6 months after anterior cruciate ligament reconstruction in pediatric and adolescent patients. Am J Sports Med. 2015 Feb;43(2):331-6.
-
48Swank KR, DiBartola AC, Everhart JS, Kaeding CC, Magnussen RA, Flanigan DC. The effect of femoral nerve block on quadriceps strength in anterior cruciate ligament reconstruction: a systematic review. Arthroscopy. 2017 May;33(5):1082-91.e1.
-
49Widmer B, Lustig S, Scholes CJ, et al. Incidence and severity of complications due to femoral nerve blocks performed for knee surgery. Knee. 2013 Jun;20(3):181-5.
-
50Manickam B, Perlas A, Duggan E, Brull R, Chan VW, Ramlogan R. Feasibility and efficacy of ultrasound-guided block of the saphenous nerve in the adductor canal. Reg Anesth Pain Med. 2009;34(6):578-80.
-
51Abdallah FW, Whelan DB, Chan VW, et al. Adductor canal block provides noninferior analgesia and superior quadriceps strength compared with femoral nerve block in anterior cruciate ligament reconstruction. Anesthesiology. 2016 May;124(5):1053-64.
-
52Dauri M, Fabbi E, Mariani P, et al. Continuous femoral nerve block provides superior analgesia compared with continuous intra-articular and wound infusion after anterior cruciate ligament reconstruction. Reg Anesth Pain Med. 2009 Mar-Apr;34(2):95-9.
-
53Vintar N, Rawal N, Pohar M, Veselko M. Intraarticular patient-controlled analgesia improves early rehabilitation after knee surgery. Coll Antropol. 2010 Sep;34(3):941-5.
-
54Woods GW, O’Connor DP, Calder CT. Continuous femoral nerve block versus intraarticular injection for pain control after anterior cruciate ligament reconstruction. Am J Sports Med. 2006 Aug;34(8):1328-33.
-
55Moutzouros V, Jildeh TR, Khalil LS, et al. A Multimodal protocol to diminish pain following common orthopedic sports procedures: can we eliminate postoperative opioids? Arthroscopy. 2020;36(8):2249-57.
-
56Bourne MH. Analgesics for orthopedic postoperative pain. Am J Orthop (Belle Mead NJ). 2004;33(3):128-35.
-
57Beck PR, Nho SJ, Balin J, et al. Postoperative pain management after anterior cruciate ligament reconstruction. J Knee Surg. 2004;17(1):18-23.
-
58Mardani-Kivi M, Karimi Mobarakeh M, Haghighi M, et al. Celecoxib as a preemptive analgesia after arthroscopic knee surgery; a triple-blinded randomized controlled trial. Arch Orthop Trauma Surg. 2013;133(11):1561-6.
-
59Secrist ES, Freedman KB, Ciccotti MG, Mazur DW, Hammoud S. Pain Management after outpatient anterior cruciate ligament reconstruction: a systematic review of randomized controlled trials. Am J Sports Med. 2016;44(9):2435-47.
-
60Ge H, Liu C, Shrestha A, Wu P, Cheng B. Do nonsteroidal anti-inflammatory drugs affect tissue healing after arthroscopic anterior cruciate ligament reconstruction? Med Sci Monitor. 2018;24:6038-43.
-
61Tsai WC, Hsu CC, Chen CP, Chen MJ, Lin MS, Pang JH. Ibuprofen inhibition of tendon cell migration and down-regulation of paxillin expression. J Orthop Res. 2006;24(3):551-8.
-
62Li Q, Zhang Z, Cai Z. High-dose ketorolac affects adult spinal fusion: a meta-analysis of the effect of perioperative nonsteroidal anti-inflammatory drugs on spinal fusion. Spine. 2011;36(7):E461-8.
-
63Blomquist J, Solheim E, Liavaag S, Baste V, Havelin LI. Do nonsteroidal anti-inflammatory drugs affect the outcome of arthroscopic Bankart repair? Scand J Med Sci Sports. 2014;24(6):e510-4.
-
64Proffen BL, Nielson JH, Zurakowski D, Micheli LJ, Curtis C, Murray MM. The Effect of perioperative ketorolac on the clinical failure rate of meniscal repair. Orthop J Sports Med. 2014;2:5.
-
65Peltoniemi MA, Hagelberg NM, Olkkola KT, Saari TI. Ketamine: a Review of clinical pharmacokinetics and pharmacodynamics in anesthesia and pain therapy. Clin Pharmacokinet. 2016;55(9):1059-77.
-
66Zhu T, Gao Y, Xu X, Fu S, Lin W, Sun J. Effect of ketamine added to ropivacaine in nerve block for postoperative pain management in patients undergoing anterior cruciate ligament reconstruction: a randomized trial. Clin Ther. 2020;42(5):882-91.
-
67Tompkins M, Plante M, Monchik K, Fleming B, Fadale P. The use of a non benzodiazepine hypnotic sleep-aid (Zolpidem) in patients undergoing ACL reconstruction: a randomized controlled clinical trial. Knee Surg Sports Traumatol Arthrosc. 2011;19(5):787-91.
-
68O’Hagan ET, Hübscher M, Miller CB, et al. Zolpidem reduces pain intensity postoperatively: a systematic review and meta-analysis of the effect of hypnotic medicines on post-operative pain intensity. Syst Rev. 2020;9(1):206.
-
69Wiffen PJ, Derry S, Bell RF, et al. Gabapentin for chronic neuropathic pain in adults. Cochrane Database Syst Rev. 2017;6(6):CD007938.
-
70Sills GJ. The mechanisms of action of gabapentin and pregabalin. Curr Opin Pharmacol. 2006;6(1):108-13.
-
71Kavak Akelma F, Baran Akkuş I, Altinsoy S, Özkan D, Ergil J. The effects of pregabalin and adductor canal block on postoperative pain in arthroscopic anterior cruciate ligament reconstruction. Turk J Med Sci. 2020;50(1):195-204.
-
72Nimmaanrat S, Tangtrakulwanish B, Klabklay P, Boonriong T. Perioperative administration of pregabalin in patients undergoing arthroscopic anterior cruciate ligament reconstruction: does it help to relieve postoperative pain? J Med Assoc Thai. 2012;95(10):1297-301.
-
73Chisholm MF, Cheng J, Fields KG, et al. Perineural dexamethasone with subsartorial saphenous nerve blocks in ACL reconstruction. Knee Surg Sports Traumatol Arthrosc. 2017;25(4):1298-306.
-
74Walder B, Schafer M, Henzi I, Tramèr MR. Efficacy and safety of patient controlled opioid analgesia for acute postoperative pain. A quantitative systematic review. Acta Anaesthesiol Scand. 2001;45:795-804.
-
75Dias AS, Rinaldi T, Barbosa LG. The impact of patients controlled analgesia undergoing orthopedic surgery. Braz J Anesthesiol. 2016;66:265-71.
-
76Konrath GA, Lock T, Goitz HT, Scheidler J. The use of cold therapy after anterior cruciate ligament reconstruction. A prospective, randomized study and literature review. Am J Sports Med. 1996 Sep-Oct;24(5):629-33.
-
77Koyonos L, Owsley K, Vollmer E, Limpisvasti O, Gambardella R. Preoperative cryotherapy use in anterior cruciate ligament reconstruction. J Knee Surg. 2014 Dec;27(6):479-84.
-
78Waterman B, Walker JJ, Swaims C, et al. The efficacy of combined cryotherapy and compression comparedwith cryotherapy alone following anterior cruciate ligament reconstruction. J Knee Surg. 2012 May;25(2):155-60.
-
79Kowal MA. Review of physiological effects of cryotherapy. J Orthop Sports Phys Ther. 1983;5(2):66-73.
-
80Drez D, Faust DC, Evans JP. Cryotherapy and nerve palsy. Am J Sports Med. 1981 Jul-Aug;9(4):256-7.
-
81McCarthy MR, Yates CK, Anderson MA, Yates-McCarthy JL. The effects of immediate continuous passive motion on pain during the inflammatory phase of soft tissue healing following anterior cruciate ligament reconstruction. J Orthop Sports Phys Ther. 1993;17(2):96-101.
-
82McCarthy M, Buxton B, Yates C. Effects of continuous passive motion on anterior laxity following ACL reconstruction with autogenous patellar tendon grafts. J Sport Rehabil. 1993;2:171-8.
-
83Smith T, Davies L. The efficacy of continuous passive motion after anterior cruciate ligament reconstruction: a systematic review. Phys Ther Sport. 2007;8:141-52.
-
84Richmond JC, Gladstone J, MacGillivray J. Continuous passive motion after arthroscopically assisted anterior cruciate ligament reconstruction: comparison of short- versus long-term use. Arthroscopy. 1991;7(1):39-44.
-
85Wright RW, Preston E, Fleming BC, et al. A systematic review of anterior cruciate ligament reconstruction rehabilitation: part I: continuous passive motion, early weight bearing, postoperative bracing, and home-based rehabilitation. J Knee Surg. 2008;21(3):217-24.
-
86Sluka K. The neurobiology of pain and foundations for electrical stimulation. En: Robinson A, Snyder-Mackler L (eds.). Clinical Electrophysiology. Baltimore, MD: Lippincott, Williams and Wilkins; 1995. p. 490.
-
87Jensen JE, Conn RR, Hazelrigg G, Hewett JE. The use of transcutaneous neural stimulation and isokinetic testing in arthroscopic knee surgery. Am J Sports Med. 1985;13(1):27-33.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- La importancia del control del dolor
- Aprendiendo del dolor para mejorar al paciente
- Manejo perioperatorio del dolor en cirugía artroscópica de hombro
- Manejo perioperatorio del dolor en artroscopia de codo
- Analgesia perioperatoria en cirugía artroscópica de muñeca y mano
- Analgesia perioperatoria en artroscopia de cadera
- Analgesia perioperatoria en cirugía artroscópica de rodilla
- Manejo perioperatorio del dolor en artroscopia de tobillo
- Dolor neuropático posquirúrgico en traumatología
- Técnica de aplicación del parche de capsaicina 179 mg
- SLAP de tipo 3: desgarro en asa de cubo
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.