Doble fascículo en el ligamento cruzado anterior. ¿Sigue indicado?
Double bundle anterior cruciate ligament reconstruction. Is it still indicated?
Resumen:
Duplicando el concepto, el modelo de reconstrucción en doble fascículo (RDF) del ligamento cruzado anterior (LCA) vincula ambos huesos de la rodilla mediante 2 elementos estabilizadores en el fémur: un fascículo que alcanza la zona más proximal de la huella femoral denominado anteromedial (AM), que se tensa en flexión; y un segundo fascículo que alcanza la zona más distal de la huella denominado posterolateral (PL) y está tenso cerca de la extensión. Pueden estar configurados entre 2 puntos de anclaje en cada hueso (2 fascículos-4 túneles) o bien tener un anclaje común en la tibia, desplegándose hacia 2 anclajes en el fémur.
Aunque biomecánicamente el planteamiento teórico es superior, a corto y medio plazo, tanto las reconstrucciones monofasciculares (RMF) como las RDF tienen resultados similares en las escalas de valoración subjetiva. Pero las RDF resultan superiores cuando se miden los aspectos físicos de la estabilidad conseguida (KT-1000 y pivot shift). Además, la valoración de los resultados quirúrgicos a largo plazo apunta que las RDF podrían reducir el número de rerroturas de la plastia de LCA. Las RDF consisten en una reconstrucción del isométrico fascículo AM, al que se añade unas fibras específicas con comportamiento PL. Y esta aportación anatómica y cinemática podría ser la clave de su superioridad en los resultados quirúrgicos a largo plazo.
Abstract:
Duplicating the concept, the double bundle anterior cruciate ligament (ACL) reconstruction (DBR) model links the knee bones by means of 2 stabilizing elements: a bundle that reaches the most proximal area of the femoral footprint named anteromedial (AM), that becomes tight in flexion, and a second one that reaches the most distal area of the footprint named the posterolateral (PL), that becomes tight near the extension. They can be configured between 2 anchorage points in each bone (2 fascicles-4 tunnels) or they can have a common anchorage in the tibia unfolding towards 2 anchorages in the femur.
Although biomechanically, the theoretical approach is superior, in the short to medium term both single bundle reconstruction (SBR) and DBR have similar functional outcomes. But DBR results are higher when measuring the biomechanical aspects of the stability achieved (KT-1000 and pivot-shift). In addition, the assessment of long-term outcomes suggest that DBR may reduce the number of ACL graft re-injuries. The basis of DBR is to add specific fiber with PL behaviour to a reconstruction of the isometric AM bundle. And this kinematic contribution could be the key to their superiority in long-term surgical outcomes.
Conceptos anatómicos y biomecánicos
No puede entenderse la existencia de este modelo de reconstrucción del ligamento cruzado anterior (LCA) sin resaltar sus virtudes biomecánicas. Por esta razón, a modo de prólogo en este capítulo, es adecuado convenir con el/la lector/a el significado de algunos conceptos.
Podemos entender la rodilla como el movimiento relativo de un sólido (fémur) que en cada momento se mueve teniendo la base en la tibia. Aunque este movimiento es tridimensional, principalmente se produce un giro respecto a un eje aproximadamente transversal al plano sagital (movimiento de flexoextensión). Pero, a su vez, este eje de rotación es móvil, siguiendo una trayectoria desde una posición alta en extensión hasta una más baja en flexión(1,2). Además, asociado a ese movimiento de flexoextensión la rodilla presenta un movimiento de rotación y deslizamiento. El LCA es uno de los ligamentos que trabaja estabilizando este movimiento combinado.
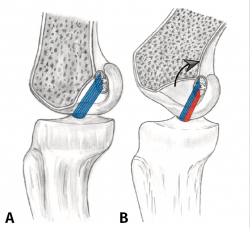
Podemos simplificar el LCA como un conjunto de fibras representadas por su fibra central. El eje de flexoextensión de la rodilla es aproximadamente transepicondilar y, como se ha dicho, además se mueve. Por esta razón, en cada momento del giro hay un subgrupo de fibras que se están tensando, reclutándose para la función estabilizadora. Pero, a su vez inevitablemente, otro grupo de fibras se destensan, dejando de participar en la estabilización(3) (Figura 1). Esencialmente, el grupo de fibras de la zona más proximal de la huella femoral se denominan anteromediales (AM) y son reclutadas para el trabajo estabilizador según avanza la flexión. El grupo de fibras que alcanza la zona más distal de la huella se denominan posterolaterales (PL) y están tensas cerca de la extensión, relajándose con el movimiento de flexión (Figura 2).
figura2.png

Figura 2. En la región proximal de la huella (sombreada en azul) se insertan las fibras surgidas del área anteromedial (AM) de la tibia, correspondientes al fascículo AM. En la región distal de la huella (sombreada en rojo) se insertan las fibras surgidas del área posterolateral (PL) de la tibia, correspondientes al fascículo PL.
Un modelo de reconstrucción monofascicular (RMF) del LCA es aquel que vincula ambos huesos (fémur y tibia) mediante un elemento estabilizador con un único anclaje en cada hueso. Biomecánicamente, el comportamiento estabilizador está determinado principalmente por la localización del punto medio de su única inserción en el fémur.
Un modelo de reconstrucción en doble fascículo (RDF) del LCA es aquel que vincula ambos huesos (fémur y tibia) mediante 2 elementos estabilizadores en el fémur. Pueden estar distribuidos entre 2 puntos de anclaje en cada hueso (2 fascículos-4 túneles) o bien tener un anclaje común en la tibia, desplegándose hacia 2 anclajes en el fémur (2 fascículos-3 túneles). Biomecánicamente, el comportamiento estabilizador está determinado principalmente por la localización de los puntos medios de cada una de sus 2 inserciones en el fémur.
Conceptualmente, estos modelos de reconstrucción no están asociados a ningún procedimiento quirúrgico de manera unívoca (transtibial versus transportal, dentro-fuera versus fuera-dentro, etc.).
Reconstrucción del ligamento cruzado anterior mediante doble fascículo y biomecánica
Durante las 2 últimas décadas del siglo XX, el tratamiento de la inestabilidad anterior de la rodilla era la RMF del LCA(4). Atendiendo al principio biomecánico de la isometría, estas RMF buscaban reproducir al fascículo AM de la huella femoral. Incluso antes, ya había sido descrito el LCA como un ligamento compuesto por subgrupos de fibras organizadas funcionalmente en 2 e incluso 3 fascículos(5). Pero la instrumentación de la cirugía (equipamiento óptico, motorización, etc.) y, sobre todo, los dispositivos de fijación eran muy básicos en comparación con los del momento actual. El gran salto de los cirujanos ortopédicos que nos preceden había sido el viraje desde la cirugía abierta a la artroscópica.
Una característica de las RMF practicadas durante ese tiempo era la posibilidad de situar el túnel femoral demasiado vertical (incluso en el techo de la escotadura). Evidentemente, situar la plastia más vertical no cuestiona su competencia en el control de la laxitud anteroposterior. Pero puede permitir una laxitud residual rotatoria cerca de la extensión (por la ausencia de fibras de la plastia con comportamiento PL)(6,7,8).
Este hecho clínico y la constatación de que las RMF no parecen prevenir el avance de la artrosis(9,10) han provocado la búsqueda de modelos de reconstrucción más eficientes. En este contexto, se ha promulgado la RDF(11,12). Esencialmente, una RDF resulta de añadir a una RMF con un túnel en la región más proximal de la huella (más isométrica) un grupo de fibras que estabilicen la rodilla en extensión y colocadas sobre la región PL de la huella(13).
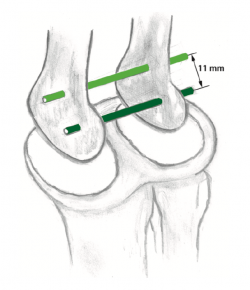
Desde el punto de vista técnico, los túneles de los fascículos en el fémur siempre son 2. El fascículo AM ocupa la región más proximal y el fascículo PL el área más distal y anterior de la huella insercional femoral. De esta manera, queda asegurado que la reconstrucción del LCA tiene un subgrupo de fibras que estabilizan en flexión (fascículo AM) y un subgrupo de fibras que estarán tensas en extensión (fascículo PL). No es posible el comportamiento dual y antagónico de la misma fibra. La tensión de las fibras está determinada por 2 factores. Inicialmente, por la tensión con la que han sido fijadas. Pero, en cuanto la rodilla se mueve, es la posición relativa respecto al eje que gira la que determina si se tensa o se relaja. Mediante estudio con resonancia magnética y en rodillas de espécimen en situación de descarga, la distancia entre el eje de extensión y el de flexión puede ser de 11 mm(2) (Figura 3). Podría considerarse una distancia suficiente para provocar un momento de fuerza variable en las fibras del LCA.
La huella insercional femoral dispone de suficiente superficie para alojar 2 túneles independientes. Esta superficie varía desde 83 hasta 196,8 mm2(14). Una RMF de 9 mm de diámetro ocupa un área de 63,5 mm2 y una RDF ocupa un área de 58,11 mm2. Parece cierto afirmar, con independencia del modelo de reconstrucción utilizado, que apenas se utiliza la mitad de la huella insercional original(15). La altura del paciente podría ser un factor limitante para este modelo de reconstrucción. Una altura mayor de 160 cm en hombres y de 155 en mujeres permite las RDF(16).
Unos de los condicionantes de la cirugía de reconstrucción del LCA mediante injerto autólogo son la longitud y el diámetro de los tendones extraídos. No parece que haya relación entre el tamaño de los tendones extraídos y las huellas insercionales. Por lo tanto, es poco probable que se reproduzcan el tamaño y la anatomía del LCA nativo(17). Aunque la altura del paciente tiene correlación con el diámetro de los tendones, el 55,1% de los tendones extraídos en 1.682 reconstrucciones del LCA fueron menores de 8 mm de diámetro(18). El hecho de que las rodillas sean constitucionalmente diferentes en tamaño provoca que se realicen RMF de diámetros similares en pacientes con diferente talla o índice de masa corporal. Este hecho se intenta paliar aumentando el número de veces que se doblan sobre sí mismos los tendones extraídos. Pero este intento de aumentar su diámetro va en detrimento de la longitud de tendón enterrado en el hueso, al que debe unirse mediante las fibras de Sharpey(19).
Como se ha dicho previamente, la RDF no ocupa más huella que la RMF, sino que permite distribuir mejor el material de injerto extraído en la huella original, aumentando su eficiencia. De esta manera, cobra mucho sentido separar los túneles en correlación positiva con la talla del paciente para aumentar la superficie de la huella funcional en el fémur. De esta manera, se aumenta la posibilidad de que todas las fibras AM sean más específicamente AM y las fibras PL sean más específicamente PL, evitando que el movimiento de la rodilla provoque asimetrías en los porcentajes de fibras que se tensan y relajan derivadas de un único anclaje femoral de las RMF (Figura 4).
figura4.png
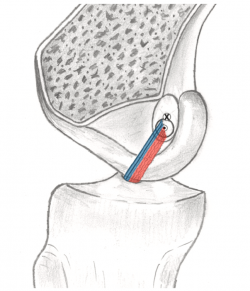
Figura 4. Las reconstrucciones monofasciculares son más sensibles a un desigual reparto de las funciones estabilizadoras de las fibras. En la imagen, el túnel centrado en el punto negro provoca que, con la flexión, sea un subgrupo mayoritario de fibras las que se relajen (sombreadas en rojo) y minoritario las que se tensan (sombreadas en azul). X: eje de rotación en ese momento.
Otro aspecto técnico de las RDF es el número de túneles tibiales a realizar. Originalmente, la técnica se describió labrando 2 túneles en la tibia(11). Puesto que hay cierta correlación entre el tamaño de la huella insercional y la altura(18), en pacientes con talla baja pueden surgir dificultades técnicas. Puede resultar difícil labrar 2 túneles independientes en la tibia sin riesgo de rozamiento de la plastia con la escotadura o con el cóndilo lateral. Se puede dar también una confluencia de los túneles. Además, para algunos cirujanos resulta interesante preservar restos insercionales del LCA original que “enfunden” la emergencia de la plastia en la articulación desde la tibia. Por estas razones, estudios biomecánicos han validado las RDF mediante un único túnel tibial. Siguen teniendo un mejor control de la rotación que las RMF(8) y son equiparables a las RDF mediante 2 túneles en la tibia(20).
Reconstrucción del ligamento cruzado anterior mediante doble fascículo y resultados
Durante la primera década del siglo XXI la cirugía ortopédica ha buscado aumentar la eficiencia de las RMF ante la inestabilidad rotatoria. En este sentido, se ha propuesto posicionar el túnel femoral en una posición más centrada en la huella. En estudios biomecánicos realizados en laboratorio se ha demostrado que horizontalizando las fibras de la RMF (a las 10:30 como referencia horaria en una rodilla derecha), se dota a la reconstrucción de mayor capacidad de reproducir maniobras de pivot-shift negativas en los especímenes cadavéricos(21).
Este tipo de estudios han provocado que en paralelo a la cirugía de RDF, la mayoría de los cirujanos han optado por seguir realizando RMF realizando el túnel femoral en el centro de la huella. Pero este hecho abre una nueva perspectiva de la valoración de los resultados quirúrgicos de la reconstrucción del LCA. No hay duda de que están validadas tanto las RDF como las RMF. Y, dentro de estas últimas, tanto las isométricas (túnel femoral en área AM) como las que se realizan perforando el túnel en el centro de la huella. Todas estabilizan la rodilla en los plazos cortos y medios. Pero en las revisiones de los resultados quirúrgicos, hoy en día se da valor específico a los índices de rerroturas a largo plazo o la reincorporación precoz a la vida activa de manera segura.
En las revisiones de los resultados clínicos, tanto las RMF como las RDF tienen resultados similares en las escalas de valoración subjetiva. Pero las RDF resultan superiores cuando se miden los aspectos físicos de la estabilidad conseguida (KT-1000 y pivot-shift)(22,23). Además, se empieza apuntar que las RDF podrían reducir el número de rerroturas(22). En esta misma dirección apuntan revisiones posteriores de los resultados quirúrgicos de la reconstrucción del LCA. En un estudio prospectivo aleatorizado con 10 años de seguimiento, las RDF presentaron un menor índice de rerroturas cuando se compararon con RMF con el túnel centrado en la huella(24).
Este cambio en la localización del túnel femoral podría, en consecuencia, no ser inocuo. Recientemente se han comparado con esta nueva visión (índice de rerroturas) 1.016 RMF con el túnel en posición AM frente a 464 RMF con el túnel en posición central de la huella. La colocación del túnel central resultó en una tasa de revisión significativamente (3,5 veces) mayor en comparación con la colocación de un túnel AM (p = 0,001)(25). Habría 2 razones para explicar este hecho. La primera es que, puesto que no está demostrado que una misma fibra tenga 2 comportamientos biomecánicos diferentes, centrar el túnel en la huella supone incorporar fibras al grupo PL pero restándolas de la función estabilizadora AM. En segundo lugar, porque, bajo el punto de vista de la isometría, las fibras que se insertan en la zona central de la huella están sometidas a alteraciones de su longitud que pueden ser superiores a los 7 mm(26,27). Las RDF consisten en una reconstrucción del isométrico fascículo AM, al que se añaden unas fibras específicas con comportamiento PL. Y esta podría ser la clave de su superioridad en los resultados quirúrgicos tanto a corto como a largo plazo.
Conclusiones
El objetivo de las reconstrucciones del LCA es restituirlo tanto anatómicamente como funcionalmente. Resulta dudoso que sensu stricto pueda restituirse la anatomía original. Además, hay algunas cuestiones cinemáticas que hoy en día no se tienen en cuenta en la valoración de las reconstrucciones practicadas.
La RDF es una técnica que cualitativamente aporta ventajas biomecánicas. Los resultados clínicos medidos mediante escalas de valoración subjetiva no son unívocamente superiores a las RMF. Pero los atractivos fundamentos biomecánicos de las RDF, junto al desarrollo tecnológico, sugieren que es una propuesta quirúrgica de futuro.
Figuras
Figura 1. A: en el momento de la fijación todas las fibras del ligamento cruzado anterior están tensas; B: asociado al movimiento de flexión, un porcentaje de las fibras se relajan porque disminuye la distancia entre sus inserciones.
Figura 2. En la región proximal de la huella (sombreada en azul) se insertan las fibras surgidas del área anteromedial (AM) de la tibia, correspondientes al fascículo AM. En la región distal de la huella (sombreada en rojo) se insertan las fibras surgidas del área posterolateral (PL) de la tibia, correspondientes al fascículo PL.
Figura 3. Disposición de los ejes de rotación en extensión y en flexión(2). El eje en extensión (mostrado en verde claro) ocupa una posición alta. El eje al final de la flexión (mostrado en verde oscuro) ocupa una posición más distal y posterior. La distancia media entre ambos es 11 mm.
Figura 4. Las reconstrucciones monofasciculares son más sensibles a un desigual reparto de las funciones estabilizadoras de las fibras. En la imagen, el túnel centrado en el punto negro provoca que, con la flexión, sea un subgrupo mayoritario de fibras las que se relajen (sombreadas en rojo) y minoritario las que se tensan (sombreadas en azul). X: eje de rotación en ese momento.
Información del artículo
Cita bibliográfica
Autores
Iñaki Mediavilla
Servicio de Cirugía Ortopédica y Traumatología. Hospital de Basurto. Bilbao, Bizkaia
Universidad del País Vasco. Bilbao
Mikel Aramberri
Alai Sports Medicine Clinic. Madrid
Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario Ramón y Cajal. Madrid
Eric Margalet
Institut Margalet of Arthroscopy. Barcelona
Institut Margalet de Cirugía Artroscòpica. Marbella
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de intereses.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Frankel VH, Burstein VH, Brooks DB. Biomechanics of internal derangement of the knee: pathomechanics as determined by analysis of the instant centers of motion. J Bone Joint Surg. 1971;53A:945-62.
-
2Iwaki H, Pinskerova V, Freeman MA. Tibiofemoral movement 1: the shape and relative movement of the femur and tibia in the unloaded cadaver knee. J Bone Joint Surg. 2000;82B:1189-95.
-
3Amis AA. The functions of the fibre bundles of the anterior cruciate ligament in anterior drawer, rotational laxity and the pivot shift. Knee Surg Sports Traumatol Arthrosc. 2012;20:613-20.
-
4Clancy W, Nelson D, Reider B, Narechania RG. Anterior cruciate ligament reconstruction using one-third patellar ligament, augmented by extra-articular tendon transfers. J Bone Joint Surg (Am). 1986;64:352-9.
-
5Norwood LA, Cross MJ. Anterior cruciate ligament: functional anatomy of its bundles in rotatory instabilities. Am J Sports Med. 1979;7:23-6.
-
6Lee MC, Seong SC, Lee S, Chang CB, Park YK, Jo H, Kim CH. Vertical femoral tunnel placement results in rotational knee laxity after anterior cruciate ligament reconstruction. Arthroscopy. 2007;23(7):771-8.
-
7Ristanis S, Giakas G, Papageorgiou CD, Moraiti T, Stergiou N, Georgoulis AD. The effects of anterior cruciate ligament reconstruction on tibial rotation during pivoting after descending stairs. Knee Surg Sports Traumatol Arthrosc. 2003;11:360-5.
-
8Yagi M, Wong EK, Kanamori A, Debski RE, Fu FH, Woo SL. Biomechanical analysis of an anatomic anterior cruciate ligament reconstruction. Am J Sports Med. 2002;30:660-6.
-
9Hogervorst T, Pels Rijcken TH, Rucker D, van der Hart CP, Taconis WK. Changes in bone scans after anterior cruciate ligament reconstruction: a prospective study. Am J Sports Med. 2002;30:823-33.
-
10Jonsson H, Riklund-Ahlstrom K, Lind J. Positive pivot shift after ACL reconstruction predicts later osteoarthrosis. Acta Orthop Scand. 2004;75:594-9.
-
11Colombet P, Robinson J, Jambou S, Allard M, Bousquet V, de Lavigne C. Two-bundle, four- tunnel anterior cru- ciate ligament reconstruction. Knee Surg Sports Traumatol Arthrosc. 2005;9:1-8.
-
12Yasuda K, Kondo E, Ichiyama H, Kitamura N, Tanabe Y, Tohyama H, Minami A. Anatomic reconstruction of the anteromedial and posterolateral bundles of the anterior cruciate ligament using hamstring tendon grafts. Arthroscopy 2004;20:1015-25.
-
13Sakane M, Fox RJ, Woo SL, Livesay GA, Li G, Fu FH. In situ forces in the anterior cruciate ligament and its bundles in response to anterior tibial loads. J Orthop Res. 1997;15:285-93.
-
14Kopf S, Musahl V, Tashman S, Szczodry M, Shen W, Fu FH. A systematic review of the femoral origin and tibial insertion morphology of the ACL. Knee Surg Sports Traumatol Arthrosc. 2009 Mar;17(3):213-9.
-
15Mediavilla I, Aramberri M, Guerrero A, Soler F. Conceptos biomecánicos de la cirugía reconstructiva del ligamento cruzado anterior. Rev Esp Artrosc Cir Articul. 2017;24(2):160-70.
-
16Tashiro Y, Okazaki K, Iwamoto Y. Evaluating the distance between the femoral tunnel centers in anatomic double-bundle anterior cruciate ligament reconstruction using a computer simulation. Open Access J Sports Med. 2015 Jun 25;6:219-24.
-
17Iriuchishima T, Ryu K, Yorifuji H, Aizawa S, Fu FH. Commonly used ACL autograft areas do not correlate with the size of the ACL footprint or the femoral condyle. Knee Surg Sports Traumatol Arthrosc. 2014 Jul;22(7):1573-9.
-
18Ramkumar PN, Hadley MD, Jones MH, Farrow LD. Hamstring Autograft in ACL Reconstruction: a 13-Year Predictive Analysis of Anthropometric Factors and Surgeon Trends Relating to Graft Size. Orthop J Sports Med. 2018 Jun 19;6(6).
-
19Rodeo SA, Arnoczky SP, Torzilli PA, Hidaka C, Warren RF. Tendon-healing in a bone tunnel. A biomechanical and histological study in the dog. J Bone Joint Surg Am. 1993;75:1795-803.
-
20Drews BH, Seitz AM, Huth J, Bauer G, Ignatius A, Dürselen L. ACL double-bundle reconstruction with one tibial tunnel provides equal stability compared to two tibial tunnels. Knee Surg Sports Traumatol Arthrosc. 2017 May;25(5):1646-52.
-
21Kondo E, Merican AM, Yasuda K, Amis AA. Biomechanical comparison of anatomic double-bundle, anatomic single-bundle, and nonanatomic single-bundle anterior cruciate ligament reconstructions. Am J Sports Med. 2011 Feb;39(2):279-88.
-
22Tiamklang T, Sumanont S, Foocharoen T, Laopaiboon M. Double-bundle versus single-bundle reconstruction for anterior cruciate ligament rupture in adults. Cochrane Database Syst Rev. 2012;11:CD008413.
-
23Mundi R, Bhandari M. Cochrane in CORR (®): Double-bundle Versus Single-bundle Reconstruction for Anterior Cruciate Ligament Rupture in Adults (Review). Clin Orthop Relat Res. 2016 May;474(5):1099-101.
-
24Järvelä S, Kiekara T, Suomalainen P, Järvelä T. Double-Bundle Versus Single-Bundle Anterior Cruciate Ligament Reconstruction: a Prospective RandomizedStudy With 10-Year Results. Am J Sports Med. 2017 Sep;45(11):2578-85.
-
25Clatworthy M, Sauer S, Roberts T. Transportal central femoral tunnel placement has a significantly higher revision rate than transtibial AM femoral tunnel placement in hamstring ACL reconstruction. Knee Surg Sports Traumatol Arthrosc. 2019 Jan;27(1):124-9.
-
26Smith JO, Yasen S, Risebury MJ, Wilson AJ. Femoral and tibial tunnel positioning on graft isometry in anterior cruciate ligament reconstruction: a cadaveric study. J Orthop Surg (Hong Kong). 2014 Dec;22(3):318-2.
-
27Lubowitz JH. Anatomic ACL reconstruction produces greater graft length change during knee range-of-motion than transtibial technique. Knee Surg Sports Traumatol Arthrosc. 2014 May;22(5):1190-5.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Puesta al día sobre el ligamento cruzado anterior: un nuevo número monográfico
- ¿Qué está de moda ahora en el ligamento cruzado anterior?
- Lesiones del ligamento cruzado anterior en pacientes esqueléticamente inmaduros
- Lesiones parciales del ligamento cruzado anterior
- Límites de la osteotomía en la ligamentoplastia de cruzado anterior
- Revisión del estado actual de las plastias empleadas en la reconstrucción ligamentosa en cirugía de rodilla
- Cirugía de revisión del ligamento cruzado anterior. ¿Uno o dos tiempos?
- Doble fascículo en el ligamento cruzado anterior. ¿Sigue indicado?
- Retorno al deporte tras la reconstrucción del ligamento cruzado anterior
- Refuerzos anterolaterales en la reconstrucción del ligamento cruzado anterior
- Reconstrucción del ligamento cruzado anterior con técnica de ahorro fisario intra-extraarticular con autoinjerto de cintilla iliotibial en pacientes esqueléticamente inmaduros
- Cirugía de revisión del ligamento cruzado anterior con injerto de tendón cuadricipital y tenodesis extraarticular lateral con fascia lata
- Rotura completa del fascículo posterolateral del ligamento cruzado anterior
- Neovasos hacia el fragmento luxado de una lesión en asa de cubo meniscal
- Reparación artroscópica de lesión meniscal con forma de asa de cubo
- Avulsión de su inserción en la rótula del ligamento patelofemoral medial
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.