Reinserción directa en roturas del ligamento cruzado anterior
Direct reattachment in anterior cruciate ligament ruptures
Resumen:
El enfoque terapéutico de las roturas del ligamento cruzado anterior (LCA) ha evolucionado en los últimos 50 años. La publicación de malos resultados con la técnica de reparación directa (popularizada en los años setenta) motivó su abandono en favor de técnicas de reconstrucción con plastias, aunque el interés por la reinserción del LCA se ha reavivado recientemente por el desarrollo de nuevas técnicas quirúrgicas y la mejora del instrumental y los implantes empleados en ellas.
Las ventajas de la reparación directa frente a la reconstrucción incluyen la ausencia de morbilidad en la zona donante, una menor agresividad quirúrgica, la preservación del tejido nativo, un aparente menor tiempo de recuperación y la facilidad para realizar una cirugía de revisión en caso de rerrotura. Las técnicas de reinserción podrían estar indicadas en el caso de roturas proximales del ligamento (tipos 1 o 2 de la clasificación de Sherman) con buena calidad de tejido, siempre y cuando se trate de cirugía en agudo o con poco tiempo de evolución sobre adultos de mayor edad que no practiquen deportes de contacto.
En esta publicación se describen la técnica de reinserción directa al fémur con un implante sin nudos y la técnica de suspensión cortical. En ambos casos, la reparación se acompaña de un refuerzo sintético, pudiendo valorarse además la asociación de un refuerzo extraarticular anterolateral.
La técnica de sutura directa se está popularizando y puede ser una herramienta más en la cirugía de las lesiones del LCA. Si bien los resultados son esperanzadores, todavía no están bien definidas las indicaciones en cuanto a la cronología y el grado de actividad, la edad y la demanda deportiva de los pacientes. Son necesarios ensayos clínicos bien diseñados, incluyendo el tratamiento conservador, que ayuden en la toma de decisiones. Es fundamental seleccionar adecuadamente la rotura y el paciente para obtener el mejor resultado posible.
Abstract:
The therapeutic approach to anterior cruciate ligament (ACL) tears has evolved over the past 50 years. The publication of poor results with the direct repair technique (popularized in the 1970s) led to its abandonment in favour of plasty reconstruction techniques, although interest in ACL reattachment has recently been rekindled by the development of new surgical techniques and improved instruments and implants.
The advantages of direct repair over reconstruction include the absence of donor site morbidity, less surgical aggressiveness, preservation of native tissue, an apparently shorter recovery time, and the ease of performing revision surgery in case of re-rupture. Reattachment techniques may be indicated in the case of proximal ligament ruptures (types 1 or 2 of the Shermanclassification) with good tissue quality, provided that surgery is performed in the acute or short term in older adults who do not play contact sports.
The present study describes the direct femoral reattachment technique with a knotless implant and the cortical suspension technique. In both cases, repair is accompanied by synthetic reinforcement, and the addition of anterolateral extra-articular reinforcement may also be considered.
The direct suture technique is gaining popularity, and may be an additional tool in the surgery of ACL injuries. While the results are encouraging, the indications are not yet well established in terms of chronology and activity level, patient age and sporting demands. Well-designed clinical trials, including conservative treatment, are needed to help in decision-making. Proper selection of the tear and of the patient is essential to secure the best possible result.
Introducción
El enfoque terapéutico de las roturas del ligamento cruzado anterior (LCA) ha evolucionado en los últimos 50 años y es que, como ocurre recurrentemente en nuestra especialidad, algunas técnicas ya abandonadas por sus malos resultados reviven con la mejora de los materiales e instrumentaciones. De esta forma, en el caso de la cirugía del LCA estamos siendo testigos de un creciente interés por su reparación directa como alternativa a la cirugía reconstructiva.
En los años setenta se popularizó la técnica descrita por Feagin(1) de reinserción directa del LCA mediante una artrotomía seguida de una inmovilización prolongada. El tratamiento de la patología meniscal y el resto de las lesiones asociadas no era, evidentemente, el que se realiza actualmente. Los resultados iniciales fueron buenos, pero su revisión a medio plazo mostró unos resultados decepcionantes, con alta tasa de dolor (71%) e inestabilidad residual (94%)(2). Estos malos resultados publicados hicieron que se abandonase la reinserción directa en favor de técnicas de reconstrucción con plastias.
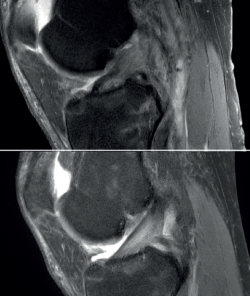
Hoy sabemos, gracias al estudio histológico de los remanentes del LCA tras su rotura, que este ligamento posee cierta capacidad intrínseca para su cicatrización espontánea, como demuestran la presencia de yemas vasculares, terminaciones nerviosas y células con capacidad de curación en dichos restos(3). Otra prueba de esta capacidad reparativa propia está en los buenos resultados funcionales publicados para algunos pacientes tratados de forma conservadora, especialmente cuando se trata de sujetos de mayor edad y menor demanda deportiva(4) (Figura 1).
A pesar de ello, es cierto que la cicatrización completa del LCA sin tratamiento quirúrgico tras su rotura es poco habitual, entre otros motivos por la presencia de líquido sinovial en el interior de la articulación, lo que dificulta la formación de un hematoma contenido entre ambos cabos del ligamento roto (paso previo necesario para la cicatrización tisular). Para superar este ambiente articular hostil y mejorar los resultados de la reconstrucción del LCA, desde hace unos años algunos autores(5) recomiendan preservar los restos del ligamento roto, aprovechando la biología de este para facilitar su integración en los túneles óseos y mejorar la propiocepción.
En esta publicación presentamos dos técnicas para la reparación del LCA, que llevan al máximo la idea de preservar el remanente, exprimiendo su potencial curativo con el objetivo de conseguir la cicatrización de este en su huella femoral.
Indicaciones
Las ventajas de la reparación directa frente a la reconstrucción ligamentosa incluyen la ausencia de morbilidad en la zona donante, la menor agresividad quirúrgica, la preservación del tejido nativo, un menor tiempo de recuperación y la menor complejidad de una eventual cirugía de revisión en caso de fracaso(6).
La reparación primaria del LCA encuentra su principal indicación en las roturas completas o parciales de alto grado de tipos 1 o 2 de la clasificación original de Sherman(7), es decir, en las avulsiones de la inserción femoral (tipo 1) o en las roturas proximales que dejan un 75-90% de ligamento distal intacto (tipo 2), siendo imprescindible en cualquier caso una buena calidad del tejido remanente. Hay que señalar que la incidencia de este tipo de roturas parece ser mayor en individuos mayores de 35 años(7), lo que no supone un problema, dado que la incidencia de rerroturas tras la reparación del LCA es mayor en pacientes más jóvenes, por debajo de los 21 años(8,9).
En cuanto al momento de la cirugía, esta se realiza idealmente dentro de las 6 semanas siguientes a la rotura(10,11,12), aunque también se han publicado buenos resultados reparando roturas cronificadas en las que el muñón del LCA roto queda cicatrizado sobre el ligamento cruzado posterior (LCP)(13,14).
También es importante añadir que los resultados de la reparación del LCA parecen mejorar asociando otras técnicas, como son el refuerzo con una cinta sintética de sutura (InternalBrace®), que ha demostrado mejores resultados biomecánicos en estudios cadavéricos(11), o los procedimientos de refuerzo anterolaterales (tenodesis extraarticular, reparación del ligamento anterolateral)(15,16).
Técnica de fijación directa al fémur
Instrumental
Para realizar la técnica es necesario contar con 2 suturas de lazo cerrado (FiberLink® de Arthrex, Naples, FL; UltraLoop® de Smith & Nephew, Andover, MA), un pasador de suturas (Scorpion® de Arthrex; FirstPass Mini® de Smith & Nephew), 2 implantes roscados sin nudo de 4,75 mm con sus respectivos punzones (SwiveLock® 4,75 mm de Arthrex, HealiCoil® de Smith & Nephew), una cinta (FiberTape® de Arthrex, UltraTape® de Smith & Nephew) y una broca de 2,4 mm. El procedimiento debe ser realizado por un cirujano experimentado en artroscopia de rodilla.
Técnica quirúrgica
El paciente es colocado en decúbito supino y la pierna es cubierta y preparada para una artroscopia de rodilla a gusto del cirujano, como si fuese a realizar una plastia de LCA. Se realizan los portales anterolateral y anteromedial de forma habitual y se explora la articulación. Al explorar el compartimiento central se debe confirmar tanto con visión directa como con palpación que la lesión es proximal y que la calidad del tejido es buena; si el tejido es friable y desgarra fácilmente, no está indicada la reparación. Si el remanente del LCA está adherido al LCP, debe disecarse para conseguir que el LCA quede libre y pueda ser manipulado para llevarlo hasta su zona de inserción. Para esto es mejor utilizar un periostotomo romo de artroscopia de hombro, aunque podrían utilizarse también un sinoviotomo, vaporizador o aplicador de plasma, siempre y cuando se tenga cuidado para no romper o quemar el tejido y hacerlo inviable. Si hay lesiones concomitantes en meniscos o cartílagos, deben tratarse antes para evitar posiciones forzadas de varo y valgo una vez completada la reparación.
Luego de haber confirmado la lesión proximal del LCA y la buena calidad del remanente de este, y haber tratado cualquier lesión acompañante en los otros compartimientos, se realiza un portal anteromedial accesorio. Es importante resecar ampliamente la grasa de Hoffa para mejorar la visión, facilitar el paso de los hilos y evitar que estos queden adheridos a partes blandas. Conviene utilizar una cánula, idealmente flexible (PassPort® de Arthrex) para evitar que los hilos queden atascados en las partes blandas, aunque no es indispensable. El uso de cánulas largas, como las de hombro, no es idóneo, ya que queda demasiado trayecto fuera de la piel y condiciona mucho el uso del instrumental.
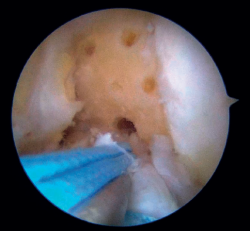
Una vez obtenida una buena visión del compartimiento central, se prepara la zona de la huella femoral del LCA para dejar hueso expuesto y se realizan microperforaciones en la pared medial del cóndilo lateral para dejar un lecho sangrante que favorezca la cicatrización del ligamento (Figura 3). Estas microperforaciones pueden hacerse con instrumental específico o con el punzón del implante. La ventaja de hacerlo con el punzón es que en este mismo momento puede dejarse preparado el punto de inserción del implante y se utiliza un solo instrumental para todo el proceso (Figura 4). Este paso puede hacerse tras haber preparado la sutura en el ligamento, aunque haciéndolo antes se evita que los hilos estén en el camino. El punto ideal para la fijación es justo anterior a la huella nativa del LCA, aunque si la rotura es parcial o Sherman I puede llevarse a la huella anatómica sin dificultad.
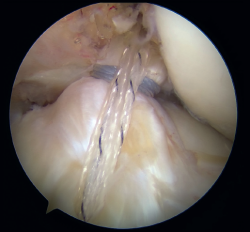
Tras esto, se identifican los fascículos anteromedial y posterolateral del LCA para suturar cada uno por separado. Con un pasador de suturas se pasa una sutura con lazo cerrado a modo de cincha a través del fascículo anteromedial en su zona más distal y se lleva el cabo sin lazo de forma alternante (medial a lateral, lateral a medial y así sucesivamente) hasta la zona más proximal, pudiendo dar habitualmente 3 o 4 pases de la sutura. Puede que el hilo haga un nudo sobre sí mismo durante la sutura si no se está atento a su entrada y salida. Para solventarlo, basta con deshacer el nudo con una pinza recuperadora y repetir el paso en caso de ser necesario.
Al finalizar, se recupera el hilo a través del portal anteromedial accesorio. Tras esto, se repite el proceso, esta vez en el fascículo posterolateral. Para evitar que se rompa el primer hilo con el paso del segundo, debe confirmarse que la entrada y la salida en el ligamento son muy posteriores e, idóneamente, algo proximales a las utilizadas para el fascículo anteromedial. Luego de haber llegado a la zona más proximal tras 3 o 4 pases, se recupera de igual forma a través del portal anteromedial accesorio.
Fuera de la rodilla se cargan los hilos en un implante de anclaje sin nudos con una cinta que funcionará como refuerzo anterior al LCA cuando sea fijada en la tibia. Una vez cargado el implante, se inserta en la zona previamente preparada. Este paso se facilita si se hace con la visión desde el portal anteromedial, ya que da mejor perspectiva de la zona (Figura 5). Una vez insertado el implante, se cortan los hilos de la sutura al nivel de la pared del cóndilo.
Con la visión en el portal anterolateral, se coloca la guía tibial del LCA en la zona central de su inserción distal y se realiza un túnel con una broca canulada de 2,4 mm por la que se pasa un nitinol con extremo en lazo, el cual se recupera por el portal anteromedial accesorio. El nitinol sirve como recuperador, para cargar a través de él la cinta y pasarla a través del túnel tibial. Una vez recuperada la cinta, se fija en la cortical tibial con un implante de anclaje sin nudos o un botón, dando la tensión a la cinta con la rodilla en extensión casi completa. Si se usa un implante roscado, es importante verificar que no queden espiras del implante protruyendo en la cortical, pues esto podría ocasionar molestias en el futuro.
Es importante confirmar bajo visión artroscópica la tensión del LCA tanto en el rango de movimiento completo como con el uso de palpador y las maniobras de Lachmann y cajón anterior (Figura 6).
Técnica de suspensión cortical
Instrumental
Para la realización de esta técnica son necesarias una cánula de artroscopia corta (PassPort®, Arthrex), guías de brocado femoral y tibial para el LCA, brocas de 4,5 y 2,4 mm, 2 suturas recuperadoras (EthiBond Loop® #5, Johnson & Johnson, NJ), una pinza pasadora (Knee Scorpion®, Arthrex; FirstPass Mini, Smith & Nephew), suturas específicas (FiberRing®, Arthrex), un sistema de suspensión cortical (ACL Repair TightRope®, Arthrex), un implante de biotenodesis (SwiveLock® 4,75 mm, Arthrex; HealiCoil, Smith & Nephew) y el instrumental preciso para realizar alguna técnica de estimulación de la médula ósea. Como alternativa al dispositivo de suspensión cortical de Arthrex podría emplearse el sistema LigaBrace® de Smith & Nephew, cuya técnica presenta algunas diferencias respecto a la detallada a continuación.
Técnica quirúrgica
El paciente puede colocarse en la misma posición que cada cirujano prefiera para la cirugía de reconstrucción del LCA. Al igual que en la técnica de fijación directa, este procedimiento comienza utilizando los portales anteriores habituales en artroscopia de rodilla: un portal anterolateral, alto, y otro anteromedial estándar. De igual manera, el LCA se examina con un palpador, para confirmar su rotura y la idoneidad de esta para ser reparada.
El siguiente paso consiste en introducir por el portal anteromedial el instrumental necesario para realizar varias perforaciones de aproximadamente 1 mm de profundidad en la huella insercional femoral, con el objetivo ya comentado de obtener un lecho sangrante que facilite la cicatrización del LCA. Estas perforaciones pueden realizarse de forma manual (con punzones de micro- o nanofracturas) o motorizada (PowerPick®, Arthrex), y este paso suele resultar más sencillo flexionando la rodilla a unos 100°.
Una vez estimulada la médula ósea, colocamos una cánula corta de silicona (PassPort®) en el portal anteromedial, con la ayuda de unas pinzas vasculares. Esta cánula nos ayudará a organizar los hilos de sutura y dificultará la interposición de la grasa de Hoffa y otras partes blandas entre ellos. Con el mismo objetivo de facilitar el manejo de las suturas (y el brocado del túnel femoral), se añade ahora un portal medial accesorio, en posición medial al anteromedial.
El túnel femoral se realiza desde este portal medial accesorio con una broca de punta de lanza de 4,5 mm de diámetro, desde la porción más anterior de la huella insercional del LCA hasta atravesar la cortical lateral del fémur. Completado el túnel, la misma broca servirá para dejar un hilo recuperador a través del túnel femoral, al estar provista de ojal. Es importante asegurar entre sí los dos cabos de este hilo por el exterior de la rodilla, para evitar perder alguno de ellos durante la cirugía.
El túnel tibial se realiza con una guía introducida por la cánula del portal anteromedial, pasando una broca canulada de 2,4 mm desde la cortical medial de la tibia hasta la región más anterior de la huella tibial del LCA, poniendo cuidado en dañar lo menos posible las fibras del ligamento durante este paso.
Una vez brocado el túnel, se retira la aguja guía del interior de la broca, para introducir a través de ella otro hilo recuperador. Este hilo es extraído mediante una pinza de agarre introducida por la cánula del portal anteromedial al exterior de la rodilla (Figura 7), donde es igualmente asegurado, como ya se hizo con el hilo recuperador femoral.
A continuación, también a través de la cánula, se introduce una pinza de sutura artroscópica (Knee Scorpion®, FirstPass® Mini) cargada con una sutura de ultraalta resistencia específica para esta técnica (FiberRing®). Utilizando la pinza, el hilo de sutura atraviesa el muñón del LCA por su tercio distal, saliendo sus dos cabos por la cánula tras extraer el instrumento de la articulación. Retirando este primer hilo, los pasos se repiten de forma idéntica con una segunda sutura, que atraviesa ahora el ligamento en una posición más proximal. Es muy importante que estas dos suturas atraviesen completamente todo el espesor del LCA.
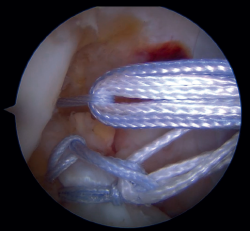
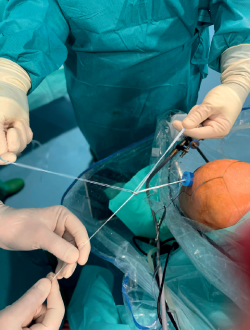
La atención pasa ahora al exterior de la rodilla, donde el bucle del sistema de suspensión cortical (ACL Repair TightRope®) se asegura al LCA utilizando los FiberRing®. Este dispositivo se trata de un botón de suspensión cortical con lazo de longitud variable, que incorpora además una cinta de alta resistencia. Para fijarlo, en primer lugar, se pasa la sutura marcada como “1” en la tarjeta a través del hilo recuperador de uno de los FiberRing® y, seguidamente, se repite el paso a través del hilo recuperador del FiberRing® restante. Tras esto, este hilo que atraviesa los anillos del sistema FiberRing® se pasa a través del lazo cerrado marcado como “2” en la tarjeta. Por último, este hilo se pasa a través del nitinol marcado como “3”, se sujeta con firmeza la tarjeta y se tira del nitinol para que el hilo del TightRope® pase a través de la pletina cortical. En este momento, quedan en el exterior de la rodilla parte del bucle, el botón y los hilos conectados a este (suturas de tracción del bucle, suturas de ascenso del botón y cinta de alta resistencia), a la espera de ser introducidos en la articulación (Figura 8).
El siguiente paso consiste en extraer el hilo recuperador femoral por la cánula del portal anteromedial, cargando en él las suturas de tracción y volteo, pero no la cinta de alta resistencia. Tirando del hilo recuperador las suturas del ACL Repair TightRope® atravesarán el túnel femoral (Figura 9), hasta salir por la piel. Usando entonces las suturas de ascenso, el botón se avanza igualmente a través del túnel, hasta voltearlo sobre la cortical femoral lateral (lo que puede verificarse traccionando con firmeza de la cinta de alta resistencia, que todavía sale por la cánula). En este momento, solo queda tirar de forma alterna de ambas suturas de tracción del bucle, para acortar este y que el muñón del LCA se reduzca hasta contactar con su huella nativa.
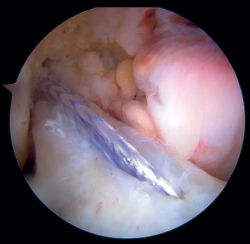
Como último paso del procedimiento, la cinta de alta resistencia conectada al botón cortical se extrae por el portal anteromedial, donde se encuentra el hilo recuperador del túnel tibial. Cargando la cinta en el hilo y traccionando de él, la cinta queda ahora por delante del ligamento reparado y sale por la cortical anteromedial de la tibia, donde se fija con la rodilla completamente extendida con un implante de tenodesis (SwiveLock®, HealiCoil®). Terminado el procedimiento, se recomienda revisar con el palpador la tensión del ligamento y el InternalBrace®, así como la ausencia de pinzamientos y limitaciones en la movilidad de la rodilla (Figura 10).
Manejo postoperatorio
Se permite tanto la movilidad libre como el apoyo inmediato con una ortesis articulada bloqueada en extensión para la carga, salvo que haya alguna lesión concomitante que impida el apoyo completo o la movilidad precoz(17), aunque no todos los autores sugieren el uso de la ortesis(18). Desde el primer momento, el paciente puede realizar ejercicios isométricos de cuádriceps y ejercicios de movilidad para recuperar el rango de movimiento completo. De usarse, la ortesis puede retirarse de forma progresiva una vez se recupera la función protectora del cuádriceps. Se permiten ejercicios de impacto de forma progresiva a partir de los 3 meses y actividad sin restricciones (incluyendo actividades deportivas) una vez que se consigue un control neuromuscular completo, alrededor de los 4 a 6 meses tras la cirugía(19).
Discusión
La técnica de sutura directa se está popularizando y puede ser una herramienta más en la cirugía de las lesiones del LCA. En el momento actual, esta opción de tratamiento está indicada para roturas proximales del LCA (tipos 1 y 2 de la clasificación de Sherman)(7), con una buena calidad de tejido remanente, siendo ideal realizarla en las 6 primeras semanas tras la lesión. Algunos aspectos que todavía no están totalmente claros son, precisamente, la ventana de oportunidad quirúrgica (algunos autores han publicado buenos resultados reparando roturas cronificadas)(13,14), la edad de los pacientes (a día de hoy se recomienda ser prudentes en la indicación en los más jóvenes, por su mayor riesgo de fracaso)(8,9) y el nivel de actividad de estos.
Es verdad que los resultados publicados hasta la fecha son esperanzadores, pero no es menos cierto que gran parte de las publicaciones parten de grupos de trabajo con un interés especial en esta técnica (con muestras pequeñas y seguimiento corto)(17) y no necesariamente han sido reproducidas de forma generalizada(20,21). Son necesarios más estudios sobre los resultados y la tasa de rerrotura entre la reconstrucción estándar y la sutura directa, pero también comparada con grupos de tratamiento conservador, para poder generalizar esta técnica.
Si bien puede ser una técnica menos agresiva quirúrgicamente, la asociación sistemática de una tenodesis extraarticular anterolateral a la reparación directa, como proponen algunos autores, puede hacer la cirugía no tan conservadora(15,16). La justificación de que, en caso de un fracaso, la cirugía de revisión es más sencilla (comparándose más con una reconstrucción primaria que con una cirugía de revisión) no debe hacernos olvidar que el paciente ha pasado ya por una cirugía y un postoperatorio prolongados.
El LCA tiene capacidad de cicatrización. El problema fundamental puede ser la formación de un espacio entre en muñón proximal y la pared del cóndilo lateral en la huella de inserción. Este espacio, ocupado por líquido sinovial, puede inhibir la formación de un hematoma organizado y la adecuada cicatrización del ligamento. El problema puede ser más mecánico que biológico(3). El desarrollo de técnicas específicas como las expuestas puede mejorar esta situación (Figura 11), pero no asegura la cicatrización ni la ausencia de una solución de continuidad entre los cabos que la dificulte(22).
La posibilidad de reparar una rotura del LCA depende tanto de las características de la propia rotura como del paciente. En cuanto a la rotura, atendiendo a la clasificación de Sherman, el 22% de las roturas del LCA se consideran de tipo 1 (avulsiones de la inserción femoral), de las que el 90% presentan una calidad tisular suficiente para indicar su reparación(23).
La probabilidad de conseguir un buen resultado tras la reparación del LCA disminuye según aumenta el tiempo transcurrido entre la lesión y la cirugía, por el deterioro progresivo de la histología del remanente(24), pero por suerte no es preciso esperar a que la rodilla recupere su movilidad completa tras la rotura del ligamento para proceder a dicha reparación.
A pesar de que la precocidad en el tratamiento quirúrgico se relaciona con un mayor riesgo de rigidez postoperatoria tras la reconstrucción del LCA según algunos estudios(25), esto no supone una preocupación con las técnicas de reparación, ya que, de hecho, los pacientes a los que se les repara el LCA tienen un mayor rango de movilidad en el postoperatorio inmediato que a quienes se les reconstruye el ligamento, al tratarse de una cirugía menos agresiva que evita el fresado de túneles de gran diámetro y la morbilidad propia de la obtención de autoinjertos. El único factor que se ha relacionado con una reducción en el arco de movilidad postoperatorio es la reparación de lesiones meniscales asociadas (al igual que sucede con las reconstrucciones), mientras que, curiosamente, la presencia de lesiones condrales no parece afectar a dicha movilidad(6).
A las características de la lesión hay que añadir las del paciente: pacientes más jóvenes y activos pueden tener un riesgo mayor de rerrotura tras una reparación directa(20). Es fundamental seleccionar adecuadamente la rotura y el paciente para obtener el mejor resultado posible.
Conclusiones
Las técnicas de reparación directa del LCA se están popularizando pese a que las indicaciones no están claramente descritas, dada la ausencia de ensayos clínicos bien diseñados que incluyan el tratamiento conservador y ayuden en la toma de decisiones(26). La reinserción directa es una técnica segura y puede ser una opción menos agresiva quirúrgicamente, con menor tiempo de recuperación y con buenos resultados en pacientes mayores, de no alta demanda, que presenten roturas proximales de tipo 1 de Sherman con buena calidad de tejido, tratados de forma aguda, asociando el uso de un InternalBrace® y valorando la necesidad de asociar una técnica de refuerzo extraarticular anterolateral.
La actitud del cirujano frente a las innovaciones en nuestra especialidad necesita de una mente abierta, pero también de una visión crítica. La generalización en el uso de estas técnicas debe basarse en estudios comparativos con técnicas de reconstrucción probadas.
Material adicional
Se puede consultar la videotécnica que acompaña a este artículo en el siguiente Vídeo:
Figuras
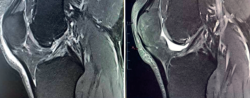
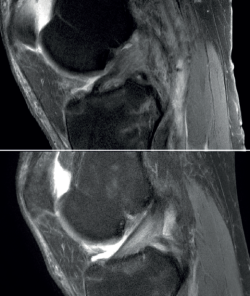
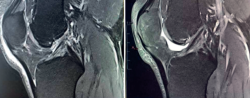
Figura 1. Rotura de ligamento cruzado anterior (LCA). A: imagen sagital de resonancia magnética (RM) de rotura aguda al diagnóstico; B: control de RM a los 12 meses de evolución con tratamiento conservador con evidente mejoría en la imagen del ligamento.
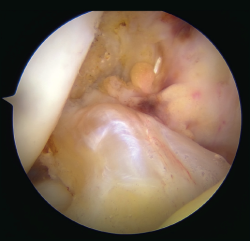
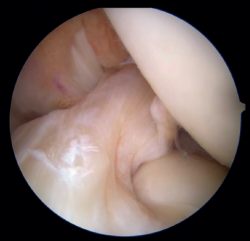
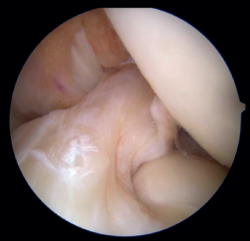
Figura 2. Imagen de rotura del ligamento cruzado anterior (LCA) de tipo 1 de Sherman con buena calidad del tejido. Rodilla derecha, visión desde el portal anterolateral.
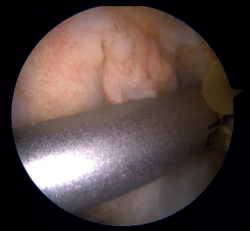
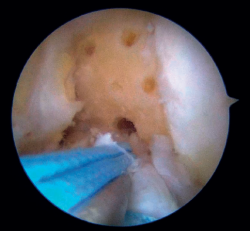
Figura 3. Microperforaciones en la pared medial del cóndilo femoral externo, adyacente a la inserción del ligamento cruzado anterior (LCA) para estimular la cicatrización de la reinserción. Rodilla izquierda, visión desde el portal anteromedial.
Figura 4. Perforación con punzón en la pared medial del cóndilo femoral externo para posterior colocación del implante sin nudos en la técnica de fijación femoral con implante. Rodilla izquierda, visión desde el portal anterolateral.
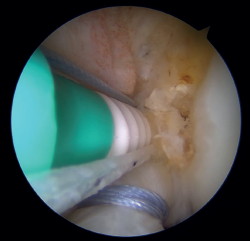
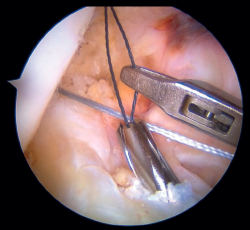
Figura 5. Fijación de suturas en el cóndilo femoral externo mediante implante sin nudos (SwiveLock®, Arthrex). Rodilla izquierda, visión desde el portal anterolateral.
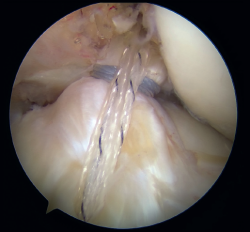
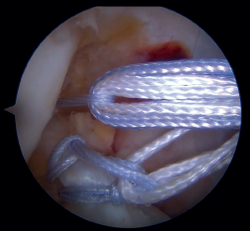
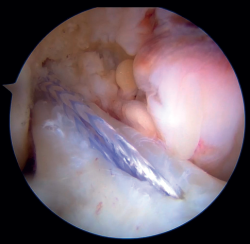
Figura 6. Imagen final de la reparación tras la colocación del InternalBrace® con cinta de alta resistencia. Rodilla izquierda, visión desde el portal anterolateral.
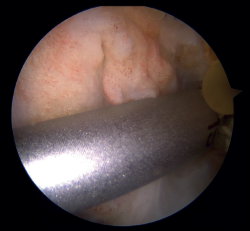
Figura 7. Tunelización tibial con broca canulada de 2,4 mm para el paso del nitinol y colocación del InternalBrace® con cinta de alta resistencia. Rodilla derecha, visión desde el portal anterolateral.
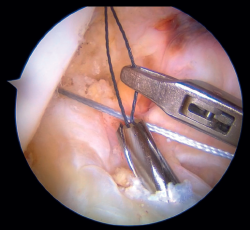
Figura 8. Introducción del sistema de fijación cortical incluyendo la cinta de alta resistencia para el refuerzo InternalBrace®. Rodilla derecha.
Figura 9. Paso del sistema de fijación cortical tras solidarizarlo a las suturas pasadas por el ligamento cruzado anterior (LCA). Rodilla derecha, visión desde el portal anterolateral.
Figura 10. Resultado final de la reparación directa del ligamento cruzado anterior (LCA) con sistema de fijación cortical e InternalBrace® con cinta de alta resistencia. Rodilla derecha, visión desde el portal anterolateral.
Figura 11. Aspecto pre- (imagen izquierda) y postoperatorio (imagen derecha) de una rotura del ligamento cruzado anterior (LCA) sometida a reparación directa.
Información del artículo
Cita bibliográfica
Autores
Diego García-Germán Vázquez
Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario HM Torrelodones. Universidad San Pablo CEU. Torrelodones. Madrid
Clínica DKF. Madrid
Servicio de Cirugía Ortopédica y Traumatología. Hospital Central de la Cruz Roja San José y Santa Adela. Madrid
Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario Puerta de Hierro-Majadahonda. Majadahonda. Madrid
Javier Ruiz Diaz
Ibermutua. Oviedo
Hospital Ibermutua Asturias
Jaime Dalla Rosa Nogales
Hospital Quirónsalud Málaga
Hospital Vithas Parque San Antonio. Málaga
Complejo Hospitalario Integral Privado (CHIP). Málaga
Agencia Sanitaria Costa del Sol. Marbella, Málaga
Pablo Crespo Hernández
Sección de Miembro Inferior. Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario Ramón y Cajal, Madrid
Editor invitado
Hospital Universitario HM-Sanchinarro. Madrid
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de interés.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Feagin JA, Curl WW. Isolated tear of the anterior cruciate ligament: 5-year follow-up study. Am J Sports Med. 1976;4(3):95-100.
-
2Sherman MF, Lieber L, Bonamo JR, Podesta L, Reiter I. The long-term followup of primary anterior cruciate ligament repair. Defining a rationale for augmentation. Am J Sports Med. 1991;19(3):243-55.
-
3Nguyen DT, Ramwadhdoebe TH, van der Hart CP, Blankevoort L, Tak PP, van Dijk CN. Intrinsic healing response of the human anterior cruciate ligament: An histological study of reattached ACL remnants. J Orthop Res. 2014;32(2): 296-301.
-
4Hetsroni I, Delos D, Fives G, Boyle BW, Lillemoe K, Marx RG. Nonoperative treatment for anterior cruciate ligament injury in recreational alpine skiers. Knee Surg Sports Traumatol Arthrosc. 2013;21(8):1910-4.
-
5Van Keulen LZ, Hoogeslag RAG, Brouwer RW, Huis In't Veld R, Verdonschot N. The importance of continuous remnant preservation in anterior cruciate ligament reconstruction. Knee Surg Sports Traumatol Arthrosc. 2022;30(5):1818-27.
-
6Van Der List JP, DiFelice GS. Range of motion and complications following primary repair versus reconstruction of the anterior cruciate ligament. Knee. 2017;24(4):798-807.
-
7Sherman MF, Lieber L, Bonamo JR, Podesta L, Reiter I. The long-term followup of primary anterior cruciate ligament repair. Defining a rationale for augmentation. Am J Sports Med. 1991;19(3):243-55.
-
8Vermeijden HD, Yang XA, van der List JP, DiFelice GS. Role of age on success of arthroscopic primary repair of proximal anterior cruciate ligament tears. Arthroscopy. 2021;37(4):1194-201.
-
9Rilk S, Goodhart GC, van der List JP, et al. Anterior cruciate ligament primary repair revision rates are increased in skeletally mature patients under the age of 21 compared to reconstruction, while adults (>21 years) show no significant difference: a systematic review and meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2024. Epub ahead of print.
-
10Douoguih WA, Apseloff NA, Murray JC, Kelly RL, Svoboda SJ. Suture-augmented anterior cruciate ligament repair for proximal avulsion or high-grade partial tears shows similar side-to-side difference and no clinical differences at two years versus conventional anterior cruciate ligament reconstruction for mid-substance tears or poor anterior cruciate ligament tissue quality. Arthroscopy. 2024;40(3):857-67.
-
11Wilson WT, Hopper GP, Banger MS, Blyth MJG, Riches PE, MacKay GM. Anterior cruciate ligament repair with internal brace augmentation: a systematic review. Knee. 2022;35:192-200.
-
12Douoguih WA, Zade RT, Bodendorfer BM, Siddiqui Y, Lincoln AE. Anterior cruciate ligament repair with suture augmentation for proximal avulsion injuries. Arthrosc Sports Med Rehabil. 2020;2(5):e475-e480.
-
13Van der List JP, DiFelice GS. Preservation of the anterior cruciate ligament: a treatment algorithm based on tear location and tissue quality. Am J Orthop (Belle Mead NJ). 2016;45(7):e393-e405.
-
14Rilk S, Vermeijden HD, van der List JP, DiFelice GS. Anterior cruciate ligament primary repair is a valid treatment option for proximal tears with good to excellent tissue quality in the acute, sub-acute and delayed setting - A letter to the editor. J ISAKOS. 2024;9(4):740-1.
-
15Deviendri R, van der Veen HC. Isolated lateral extra-articular tenodesis enhance better rotatory knee joint stability post-primary ACL repair: four cases report and literature review. Int J Surg Case Rep. 2021;84:106167.
-
16Ferretti A, Carrozzo A, Saithna A, et al. Comparison of primary repair of the anterior cruciate ligament and anterolateral structures to reconstruction and lateral extra-articular tenodesis at 2-year follow-up. Am J Sports Med. 2023;51(9):2300-12.
-
17Jonkergouw A, van der List JP, DiFelice GS. Arthroscopic primary repair of proximal anterior cruciate ligament tears: outcomes of the first 56 consecutive patients and the role of additional internal bracing. Knee Surg Sports Traumatol Arthrosc. 2019;27(1):21-8.
-
18Wu J, Kator JL, Zarro M, Leong NL. Rehabilitation principles to consider for anterior cruciate ligament repair. Sports Health. 2022;14(3):424-32.
-
19Heusdens CHW, Hopper GP, Dossche L, Roelant E, Mackay GM. Anterior cruciate ligament repair with Independent Suture Tape Reinforcement: a case series with 2-year follow-up. Knee Surg Sports Traumatol Arthrosc. 2019;27(1):60-7.
-
20Gagliardi AG, Carry PM, Parikh HB, Traver JL, Howell DR, Albright JC. ACL repair with suture ligament augmentation is associated with a high failure rate among adolescent patients. Am J Sports Med. 2019;47(3): 560-6.
-
21Osti M, El Attal R, Doskar W, Höck P, Smekal V. High complication rate following dynamic intraligamentary stabilization for primary repair of the anterior cruciate ligament. Knee Surg Sports Traumatol Arthrosc. 2019;27(1):29-36.
-
22Bachmaier S, DiFelice GS, Sonnery-Cottet B, et al. Treatment of acute proximal anterior cruciate ligament tears—Part 2. The role of internal bracing on gap formation and stabilization of repair techniques. Orthop J Sports Med. 2020;8(1):2325967119897423.
-
23Van der List JP, DiFelice GS. Preoperative magnetic resonance imaging predicts eligibility for arthroscopic primary anterior cruciate ligament repair. Knee Surg Sports Traumatol Arthrosc. 2018;26(2):660-71.
-
24Margarian AM, Fleming BC, Harrison SL, Mastrangelo AN, Badger GJ, Murray MM. Delay of 2 or 6 weeks adversely affects the functional outcome of augmented primary repair of the porcine anterior cruciate ligament Am J Sports Med. 2010;38(12):2528-34.
-
25Hopper H, Adsit M, Reiter CR, et al. Female sex, older age, earlier surgery, anticoagulant use, and meniscal repair are associated with increased risk of manipulation under anesthesia or lysis of adhesions for arthrofibrosis after anterior cruciate ligament reconstruction: A systematic review. Arthroscopy. 2024;40(5):1687-99.
-
26Engebretsen L. Editorial commentary: The anterior cruciate ligament cannot be reliably repaired: studies with a control group are needed! Arthroscopy. 2020;36(2):613-4.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Aprendiendo de los mejores
- El esfuerzo de todos
- Inclusión de la porción larga del bíceps en las reparaciones del manguito rotador
- Técnica quirúrgica del Latarjet artroscópico fijado con botones
- Plicatura artroscópica del ligamento colateral lateral del codo
- Tratamiento asistido por artroscopia de las fracturas de la articulación metacarpofalángica de los dedos
- Técnica quirúrgica de artroscopia de cadera sin pivote perineal
- Reinserción directa en roturas del ligamento cruzado anterior
- Aplicación de aloinjertos osteocondrales frescos en la rótula. Técnica quirúrgica
- Ligamentoplastia artroscópica para la inestabilidad lateral de tobillo
- Dos asas que asir: doble lesión meniscal en asa de cubo
Más en Google Scholar


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.