Todo lo que nos puede aportar la impresión de tejidos blandos en 3D
Introducción
El desarrollo de nuevas tecnologías nos ha aportado a nivel científico nuevas realidades médicas. Actualmente, la velocidad a la que estas se desarrollan hace que nuestra capacidad de adaptación a ellas tenga que ser muy rápida.
La impresión en 3 dimensiones (3D) nos ofrece una perspectiva nueva: el concepto de volumen.
Hasta ahora, la información aportada por las diversas técnicas diagnósticas nos daba una visión en 2 planos y el cirujano es el que debía reconstruir las relaciones espaciales de manera conceptual para obtener un modelo mental en 3D. Esto ha cambiado, ya que gracias a la impresión en 3D, el modelo tridimensional se puede materializar.
Tanto es así que actualmente la tecnología nos permite imprimir multitud de materiales, de sintéticos a biológicos (bioimpresión), de diferente textura, dureza y flexibilidad, lo que hace que nuestro abanico de desarrollo e innovación sea extremadamente amplio.
En el campo de la cirugía ortopédica y traumatología, la aplicación más frecuentemente usada de esta tecnología ha sido en la reconstrucción ósea, a diferencia de otras especialidades como la cirugía cardiaca o vascular, entre otras, en las que predomina la impresión de tejidos blandos y órganos(1).
Así pues, pensamos que la impresión en 3D de tejidos blandos en la patología del pie y el tobillo nos brinda una herramienta con gran potencial de aplicabilidad en el diagnóstico, el tratamiento y la planificación quirúrgica de nuestros pacientes.
Impresión en 3D de tejidos blandos
La tecnología en 3D tiene una larga trayectoria; los primeros diseños se realizaron a finales de los ochenta y principios de los noventa(2).
Actualmente, está comprobado que la tecnología en 3D tiene utilidad científica en el ámbito de todas las especialidades médicas, existiendo muchas publicaciones al respecto.
Si bien la tecnología de impresión en 3D se desarrolló inicialmente para fabricar estructuras compuestas de materiales no biológicos como plásticos, cerámicas y metales, los avances recientes han hecho posible también la impresión en 3D de materiales de base biológica(3).
Impresión en 3D de materiales biocompatibles. Bioingeniería
La pérdida o lesión de tejidos en el pie y el tobillo puede significar en ocasiones un daño irreparable de la extremidad, precisando a veces incluso la amputación.
Para poder realizar la regeneración de tejidos y su sustitución, utilizamos injertos autólogos o heterólogos, con sus ventajas y sus inconvenientes. Actualmente, la tendencia se dirige a obtener tejidos biológicos de una manera reproducible y son los bioingenieros y la ingeniería de tejidos los que investigan la creación de estos nuevos biotejidos(4).
Así pues, el objetivo de la ingeniería de tejidos es imprimir tejidos artificiales biocompatibles en 3D; estos están compuestos de 3 partes: la primera un andamio o malla (scaffold), la segunda las células; y la tercera un microambiente que imite el entorno del cuerpo humano(5).
• Los andamios o mallas (scaffold) pueden ser polímeros, hidrogeles, metálicos o cerámicos, deben ser citocompatibles, dar soporte al crecimiento, la fijación, la proliferación y la migración celular, y poder imprimirse en la forma y medida que precisemos. Las células se pueden incorporar en soluciones poliméricas o hidrogeles directamente sin cambiar significativamente su viabilidad y bioactividad. Los polímeros deben cumplir varios requisitos básicos para la impresión en 3D de órganos y tejidos: ser biocompatibles (no ser tóxicos, sin reacción inmunológica), bioimprimibles (usando bioimpresoras 3D), bioestables o reticulables, con propiedades mecánicas suficientemente fuertes, biodegradables (la tasa de biodegradación debe coincidir con la nueva velocidad de generación de tejidos y órganos), suturables con redes nerviosas y vasculares del huésped, permeables a nutrientes y gases, bioalmacenables antes de imprimirse y esterilizables.
Los polímeros pueden ser naturales, sintéticos o híbridos. Los polímeros naturales, como el alginato, el colágeno, la gelatina, el ácido hialurónico o el fibrinógeno, tienen como principal ventaja para la bioimpresión de órganos y tejidos en 3D que pueden atrapar células viables y agentes bioactivos antes de ser imprimidos, protegen las células y los agentes bioactivos durante la impresión en 3D y forman sustratos semipermeables después de la impresión en 3D.
Antes de la impresión en 3D, las células y los agentes bioactivos normalmente se incrustan en soluciones de polímeros naturales o hidrogeles. Durante la impresión en 3D, las cadenas de polímeros naturales pueden proteger a las células del estrés de la impresión y proporcionar a las células ambientes en 3D prediseñados similares a los de un órgano nativo. Después de la impresión en 3D, las cadenas de polímeros pueden reticularse física, química o enzimáticamente para formar sustratos semipermeables. Estos sustratos semipermeables son permeables a nutrientes, gases (por ejemplo, oxígeno) y metabolitos de las células.
La mayoría de los polímeros sintéticos se han aplicado como estructuras de soporte sin entrar en contacto directo con las células vivas. Los 3 polímeros sintéticos más utilizados son: polyoxyethylene (PEG), polylactic colicoglid acid (PLGA) y polyurethane (PU). Tienen excelente capacidad de impresión en 3D, por su compatibilidad con tejidos in vivo y su estabilidad estructural para la bioimpresión de órganos en 3D.
Los polímeros híbridos son el gelatin-methacryloyl (GE-IMA) y el hyaluronic acid-methacrylate (HAMA), y tienen propiedades de los 2 grupos(6).
• Las células son las del tejido que se quiera crear, incluso se puede imprimir más de un tipo de célula a la vez. Actualmente, se están imprimiendo células de tendones de ratas y músculos primarios humanos para producir modelos de tejido muscular y tendinoso en 3D. El tejido muscular impreso se contrae después de la estimulación eléctrica, demostrando funcionalidad biológica. Podríamos demostrar que la tecnología de bioimpresión en 3D abre las puertas para producir estructuras de tejido en 3D funcionales. El desarrollo de tejidos humanos in vitro se utiliza para estudios biológicos básicos y para el descubrimiento de fármacos(7).
• Los factores de crecimiento favorecen un microentorno similar al entorno del cuerpo humano, para dirigir la adhesión, la proliferación y la diferenciación celular.
Los tejidos y órganos artificiales se imprimen depositando estos 3 elementos capa por capa. Se imprimen o bien conjuntamente o por separado.
Durante los últimos 16 años se han desarrollado 4 diferentes técnicas de bioimpresión de tejidos y órganos; estas son: impresión con inyección de tinta, extrusión, láser y la combinación de las mismas. Cada una tiene sus ventajas y sus inconvenientes(8).
Con esta tecnología, se han realizado grandes esfuerzos en el desarrollo de la bioimpresión en vasos, nervios, tendones, músculos, huesos, cartílagos y otros tejidos. Hasta la fecha, la tecnología de bioimpresión en 3D se ha utilizado para generar piel, cartílago, hueso y tejidos vasculares(9). Se han trasplantado con éxito tejidos de piel y cartílago fabricados in situ en seres humanos(10).
Hablaremos ahora del concepto de 4D: consiste en imprimir en 3D biomateriales que, por sus características intrínsecas, se puedan transformar por un estímulo externo. Crearemos órganos o tejidos impresos que se transforman en el tiempo, siendo materiales bioactivos sensibles que producirían la reparación o la sustitución de tejidos dañados. Un ejemplo sería la piel: imprimiendo mallas con materiales 4D no solo crecería piel nueva sobre la malla, sino que la propia malla se transformaría de la mejor forma para integrarse en la piel(11,12).
El objetivo de la bioimpresión es el de regenerar, crear tejidos y órganos funcionantes, pero quedan por abordar una serie de desafíos importantes antes de que esto se convierta en una realidad.
Impresión en 3D de materiales sintéticos
La impresión en 3D de materiales sintéticos la utilizamos para imprimir al detalle la anatomía del pie y el tobillo, tanto en modelos sanos como patológicos.
Los datos se obtienen de las imágenes de la tomografía computarizada (TC) y de la resonancia magnética (RM); estos se digitalizan y procesan informáticamente y luego se imprimen en 3D. Inicialmente, las impresoras funcionaban con un solo material de un color fijo y de unas propiedades mecánicas concretas. Sin embargo, actualmente ya existen nuevas opciones de materiales e impresión en 3D a todo color, con las que el color y las propiedades físicas, como la rigidez y la dureza, se pueden especificar punto por punto.
Los datos de la TC y la RM se proporcionan en un formato de fichero DICOM® (Digital Imaging and Communications in Medicine), que captura la densidad de cada tejido por separado. Estos datos se procesan en un programa informático de imágenes médicas, que agrupa las regiones de imagen con una densidad similar, para identificar y separar diferentes tipos de tejidos: huesos, piel, músculos, vasos sanguíneos...; a este proceso se le denomina “segmentación”(13).
Después de la segmentación de la imagen, se guarda cada tipo de tejido en un fichero geométrico independiente, el color del cual se puede especificar de manera única dentro del programa de la impresora e imprimir independientemente.
La impresora en 3D imprime a partir de un modelo digital y de una manera aditiva, utilizando un programa software que corta el modelo en capas delgadas y utiliza esa información para depositar material, capa por capa, donde se necesita y así crear el objeto(14).
Cada impresora tiene su proceso de impresión y utiliza unos tipos de materiales concretos, según las características del modelo que se quiera imprimir. Esto permite lograr, mediante combinaciones de 2 o más materiales, piezas con múltiples características, desde rígidas a flexibles, transparentes u opacas, incluyendo varios colores, todos en la misma impresión. Así es como se obtienen los modelos anatómicos de tejidos blandos y duros en una misma pieza.
En nuestros prototipos, los materiales utilizados son resinas líquidas fotopolimerizables que, con la aplicación de luz ultravioleta (UV), solidifican capa a capa. La familia de materiales Agilus30TM son fotopolímeros similares al caucho, tienen un valor de Shore-A (unidad de dureza) de 30, que permite crear estructuras blandas que combinadas con otros materiales nos permiten obtener mayor o menor grado de dureza. La familia de materiales VeroTM son materiales rígidos y opacos que permiten conseguir diferentes colores haciendo combinaciones entre los diferentes disponibles (amarillo, cian, magenta, blanco y negro). Para hacer las estructuras blandas y diferenciarlas entre ellas (ligamentos, músculos, vasos) combinamos los 2 tipos de materiales, Agilus y Vero. En la parte ósea solo utilizamos la familia VeroTM. En cuanto a la impresora, la Stratasys® J750 nos permite tener cargados 6 materiales diferentes para realizar cada impresión. Esto hace que podamos combinar los diferentes tipos de materiales (familia Vero™ para colores opacos, familia Tango™ y Agilus30™ para materiales blandos y familia VeroClear™ para materiales transparentes) para conseguir más de 360.000 colores diferentes, varios grados de dureza y un amplio rango de transparencia/opacidad según la composición que le damos a cada una de las partes que se quiere imprimir. La resolución de la Stratasys® J750 es de 14 micras o 27 micras por capa, según el modo de impresión que seleccionamos. Esto permite lograr un alto nivel de detalle en la impresión de modelos que, combinado con la variedad de colores y de texturas que se pueden conseguir, permiten obtener unos modelos que recrean con gran detalle la parte que estamos imprimiendo.
La impresión en 3D está marcando el comienzo de una nueva era en modelos anatómicos médicos con un nivel de complejidad, realismo y sofisticación que antes no eran posibles.
Aplicación
Actualmente, la aplicación de la impresión de tejidos blandos en el pie es poco utilizada, básicamente porque la tecnología no está completamente desarrollada y, además, es difícil ampliar nuestra visión de cuánto nos puede llegar a ofrecer.
En la práctica clínica actuamos principalmente en la estructura ósea, pero en muchas ocasiones debemos complementar esta actuación añadiendo gestos en las partes blandas o incluso solo hemos de actuar en estas partes blandas(15).
Hoy en día existen otras especialidades médicas en las que este tipo de impresión en 3D es usada de forma habitual y que están mucho más familiarizadas y avanzadas en su aplicación. Y, siendo realistas, es muy difícil procesar la información de las partes blandas del pie y el tobillo, como son los vasos, los nervios, los músculos, los tendones y los ligamentos, en las imágenes 2D de TC y RM, incluso cuando estas imágenes se reconstruyen en 3D en una pantalla(16). Por este motivo, la evolución se encaminará a la impresión de modelos globales y no será sorprendente ver que los traumatólogos utilicemos, cada día con mayor frecuencia, los modelos impresos en 3D.
Modelos anatómicos completos
Una de las utilidades de la impresión en 3D en las partes blandas es la creación de modelos anatómicos completos. Actualmente, con más de 360.000 colores y materiales de diferentes texturas, dureza y flexibilidad, las impresoras en 3D permiten diferenciar cada zona anatómica, de tejido blando (como vasos, nervios, músculos, tendones, ligamentos) y de hueso duro, mejorando el realismo y la complejidad de los modelos. Así, se pueden generar prototipos de estructuras anatómicas blandas con más o menos flexibilidad y de tejido óseo con más o menos dureza. La impresión conjunta de partes óseas y blandas nos puede ayudar a realizar diagnósticos precisos, planificaciones y simulaciones quirúrgicas.
Los modelos anatómicos son una de las herramientas más útiles en la planificación global de cualquier cirugía. Nos ayudan a localizar los tendones, ligamentos, vasos y nervios cercanos a nuestras vías de abordaje, con el fin de poder optimizar nuestra habilidad y el tiempo quirúrgico, tomando las decisiones más críticas antes de iniciar la intervención.
Nos permiten diseñar la estrategia quirúrgica en la reparación de lesiones de las partes blandas y en las planificaciones de la cirugía ósea, valorar la reducción o las osteotomías a realizar y decidir previamente el tipo, el tamaño y la colocación más adecuada de los implantes necesarios en la zona a tratar, minimizando el daño tisular y preservando la capacidad vascular del tejido óseo.
Son modelos ultrarreales de la anatomía de cada paciente para que los cirujanos podamos practicar el procedimiento una y otra vez antes de operar al paciente.
En situaciones de alta complejidad, donde actuamos con equipos multidisciplinarios, este tipo de entrenamiento nos facilita la coordinación, la planificación y la toma de decisiones.
En cirugía, la tendencia actual es a realizar incisiones más pequeñas y vías de abordaje más directas: cirugía percutánea y mínimamente invasiva para minimizar la lesión tisular. Estos modelos nos permiten localizar exactamente la zona lesional y planificar estos miniabordajes, con el objetivo de identificar las estructuras anatómicas que pudieran ser dañadas durante la cirugía.
Modelos anatómicos funcionales
Si nos basamos en que las cirugías de pie y tobillo son cada día más complejas y que biomecánicamente el pie funciona como un engranaje equilibrado entre estructuras óseas, ligamentosas y tendinosas, ¿por qué no darles valor a todas estas estructuras en el momento en el que estudiamos una patología o lesión del pie y el tobillo?
La biomecánica del pie y el tobillo es una de las más complejas de las distintas regiones anatómicas del cuerpo humano, su funcionalidad varía si se está en movimiento, en apoyo o en descarga, y su estudio comporta una gran habilidad mental en 3D y en movimiento para entender su funcionamiento.
Una de las características de la impresión en 3D es la capacidad de imprimir las diversas estructuras por separado, con una dureza y una flexibilidad diferentes según los materiales empleados, para posteriormente adaptarlos en un único conjunto. Esto nos permite realizar prototipos anatómicos funcionales que nos permitirán recrear los movimientos del pie y el tobillo, y poder analizarlos desde una visión biomecánica, evaluando el distinto comportamiento de las diversas estructuras tanto articulares como tendinosas en movimiento. Así, en un futuro, la exploración dinámica de estos modelos anatómicos nos recreará las lesiones por impingement o inestabilidades ligamentosas.
Esta aplicación de la impresión en 3D no está actualmente desarrollada, pero supondría un gran avance para poder detectar y diagnosticar la patología intrínseca del pie en movimiento y en 3D, llegando a una comprensión más precisa, y detectar los mecanismos biomecánicos lesionales y poder planificar tratamientos ortopédicos y quirúrgicos más adecuados.
Formación
Actualmente, las enseñanzas sobre anatomía humana se realizan mediante prácticas en maniquíes, modelos animales y cadáveres humanos. Todos estos modelos tienen limitaciones importantes: los maniquíes actualmente son modelos poco reales, se limitan a recrear la anatomía normal básica, sin producir variaciones patológicas, tienen un alto costo y no se pueden producir en masa. Los modelos animales no replican la anatomía humana, siendo útiles en el aprendizaje de gestos quirúrgicos, como cortar, suturar, etc. Los cadáveres humanos son escasos y proporcionan un rango patológico limitado. Además, tanto los modelos de entrenamiento en animales como los de cadáveres son costosos y precisan entornos controlados.
El grupo de M. K. O'Reilly et al. realizaron un estudio con estudiantes de medicina donde compararon 2 grupos. Se les impartía la misma formación práctica en anatomía de la extremidad inferior, unos en la sala de disección y otros con modelos impresos en 3D. Los resultados mostraron que no existieron diferencias en las pruebas formativas, pero los 2 grupos estuvieron de acuerdo en que su aprendizaje se mejoró mediante el uso interactivo de modelos anatómicos(17).
Por este motivo, los modelos anatómicos impresos con tecnología en 3D están revolucionando el mundo de la docencia. Su coste más asequible, la posibilidad de imprimir en masa, su recreación anatómica normal y patológica, a medida y real están en la línea del nuevo avance en la formación de las nuevas generaciones.
Comunicación médico-paciente
Una de las ventajas de la creación de modelos anatómicos completos en 3D es la mejora de la comunicación entre médico y paciente. El paciente entiende mejor el diagnóstico y el tratamiento que se le va a realizar. Cuanto más realista es el modelo y más se asemeje a la realidad, mejor comprensión y más tranquilidad, facilitando al paciente el entendimiento de su lesión y de todo el proceso y el tratamiento que se le va a realizar. Existen estudios que muestran que tener modelos impresos en 3D aumenta la comprensión del paciente en un 50%, por lo que el beneficio es considerable en su atención personalizada, además de facilitar todo el proceso del consentimiento informado, porque permite que el paciente comprenda exactamente lo que vamos a hacer(18).
Indicaciones
Las indicaciones de la impresión en 3D de partes blandas centrada en el pie y el tobillo pueden ser muchas y diversas. La mayoría de ellas están en desarrollo y no existen estudios que certifiquen su indicación. La práctica clínica y los futuros nuevos estudios serán los que sienten las bases de las indicaciones del uso de la impresión en 3D en este campo.
mact.1301.fs2105007-figura1.png
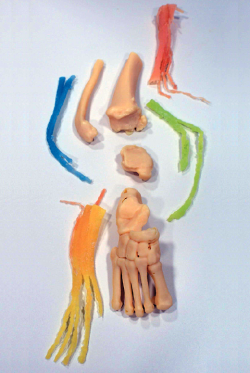
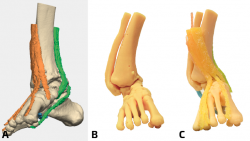
Figura 1. Grave deformidad en pie y tobillo. Se ha realizado la impresión del modelo anatómico completo, para la realización del estudio y la planificación quirúrgica de corrección de la misma. Modelo anatómico óseo y partes blandas sin ensamblar. En azul, peroneo lateral largo y peroneo lateral corto. En verde, tibial posterior, flexor hallucis longus. En naranja, tendón de Aquiles. En amarillo, extensor hallucis longus, extensor digiti longus y tibial anterior. En beis, huesos de la tibia, el peroné, el astrágalo y el calcáneo, junto al resto de las estructuras óseas del pie.
Hemos detallado unas primeras indicaciones en el uso de esta tecnología; estas son:
1. Las alteraciones congénitas pueden ser múltiples y variadas. En una deformidad congénita la anatomía siempre es anormal. La impresión en 3D de partes blandas y óseas conjuntas nos permitirá estudiar las posibilidades terapéuticas y los riesgos de la cirugía.
2. En las graves deformidades, los modelos en 3D de impresión de partes blandas y óseas nos permiten planificar la cirugía, personalizando los abordajes clásicos, modificándolos en pro de mejorar los resultados. Estas deformidades precisan actuaciones simultáneas a nivel óseo, ya sean osteotomías o artrodesis, y de partes blandas, como transposiciones tendinosas o reparaciones ligamentosas (Figuras 1 a 3).
3. En las lesiones traumáticas, pueden existir lesiones de partes blandas y óseas asociadas. Actualmente el gold standard de las planificaciones en 3D de las lesiones traumáticas es la planificación ósea. No obstante, la impresión en 3D de partes blandas nos permitirá evaluar los daños traumáticos vasculares y nerviosos, que son de gran importancia porque pueden comprometer la viabilidad y el futuro de la extremidad(19). Las lesiones tendinosas, ligamentosas y musculares también pueden diagnosticarse de manera efectiva, pues en ocasiones pueden pasar desapercibidas (Figura 4).
mact.1301.fs2105007-figura4.png
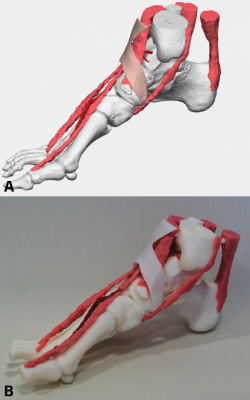
Figura 4. Arrancamiento traumático del tendón del tibial anterior (TTA). Se realizó una impresión en 3D donde se pudo objetivar el arrancamiento osteotendinoso del TTA al nivel de la base del primer metatarsiano; este sufrió una retracción y quedó anclado al retináculo. Podemos ver la relación con la arteria pedia (rojo brillante). A: imagen digital en 3D; B: imagen del modelo anatómico óseo y de partes blandas.
4. En las infecciones, nos permite localizar colecciones o abscesos, su tamaño, profundidad, extensión y el origen de los mismos, y los trayectos fistulosos que estos presentan. Nos permite ver la cantidad del tejido dañado. Con esto conseguimos realizar una valoración prequirúrgica del abordaje y del desbridamiento a realizar, sin dejar dudas a la eliminación de todo el tejido infeccioso.
5. La cirugía tumoral es una de las grandes indicaciones en la impresión en 3D de partes blandas. Los tumores del aparato locomotor precisan de una exhaustiva planificación tanto prequirúrgica como intraquirúrgica. Tener un modelo anatómico impreso con partes blandas y óseas asociadas tiene muchas ventajas: permite ver el tamaño y las características de la lesión tumoral, la afectación de las partes blandas y/o del tejido óseo, y realizar un estudio de la extensión local real de la lesión.
Valorar el compromiso de las estructuras vasculares y nerviosas, y el cálculo de los márgenes de resección con la máxima seguridad; así como planificar, si es preciso, la reconstrucción de los defectos óseos y/o de las partes blandas para restituir la funcionalidad del pie y tobillo, evitando amputaciones(20).
6. Una de las indicaciones más útiles es el pie de Charcot en pacientes diabéticos, en el que se producen destrucciones articulares y deformidades muy graves(21).
Para devolver a estos pies su funcionalidad, la impresión en 3D ósea y de partes blandas nos facilita la valoración global del pie, pudiendo determinar el riesgo vascular al poder imprimir las arterias y la localización de las mismas (información obtenida de las imágenes de angio-RM); de esta manera, podemos valorar si se precisa realizar una revascularización antes de la cirugía ortopédica correctiva.
También nos permite determinar los recorridos y las inserciones tendinosas que muy frecuentemente están completamente alteradas por la desestructuración ósea, a la vez que nos es útil a la hora de valorar el tamaño y la profundidad de las úlceras.
7. La cirugía de preservación articular se fundamenta en la realización de osteotomías supra- o inframaleolares, para modificar el eje de carga, descargar las presiones articulares del tobillo o del pie y reparar las lesiones de las partes blandas ligamentosas que pudieran existir. La impresión en 3D de partes blandas nos permite realizar la planificación quirúrgica evitando el riesgo vascular y nervioso.
Pero un tema más novedoso sería la valoración prequirúrgica de la variación en la disposición de las estructuras tendinosas y ligamentosas después de las correcciones quirúrgicas realizadas para modificar los ejes, orientándose en los posibles resultados funcionales que pudiéramos obtener tras la intervención. Otra indicación importante radica en las ventajas que nos ofrece la impresión de biomateriales osteocondrales en la regeneración del cartílago articular.
La cirugía de las prótesis de tobillo es muy demandante. La elección del paciente es muy selectiva y los implantes protésicos tienen sus limitaciones biomecánicas para su correcto funcionamiento. Por este motivo, el paciente ideal no puede presentar desaxaciones en el miembro inferior y debe mantener una correcta estabilidad ligamentosa.
La impresión de modelos anatómicos selectivos completos permite practicar previamente este tipo de cirugía tan demandante. Además, permite planificar las correcciones de las partes blandas como liberaciones o reparaciones ligamentosas.
8. Existen grandes deformidades funcionales que se presentan en el pie y el tobillo, secundarias a lesiones de partes blandas. En el pie, los ligamentos son los principales estabilizadores de la bóveda plantar; así pues, una lesión del ligamento en hamaca o del ligamento de Lisfranc nos puede llevar a un pie plano. En el caso del pie y el tobillo, las inestabilidades ligamentosas son en ocasiones difíciles de diagnosticar. La impresión en 3D de estas estructuras ligamentosas nos podría facilitar un diagnóstico etiológico de la deformidad o la inestabilidad y realizar un tratamiento más preciso del mismo.
En muchos pacientes con inestabilidad lateral de tobillo, existen otras alteraciones como la morfología ósea de un pie cavo varo, asociado a una lesión del retináculo de los tendones peroneos, y, el conjunto de todas estas lesiones, pueden ser evaluadas con un modelo de impresión global de todo el pie y tobillo.
Otras deformidades asociadas son las provocadas por alteraciones musculotendinosas, secundarias a enfermedades neurológicas que producen paresia o espasticidad. En la cirugía de las transposiciones tendinosas, que es miniinvasiva, la impresión en 3D nos sería de una gran utilidad para practicarlas previamente y poder evitar lesiones vasculares y/o nerviosas durante su ejecución in vivo.
Conclusiones
Nos encontramos en el inicio de una nueva realidad.
En un futuro, estas técnicas que ahora son tan novedosas serán habituales. Quedan por lograr muchos más avances en la aplicación de la impresión en 3D, también en el proceso técnico de creación de modelos y la recopilación de datos clínicos adicionales sobre el impacto final de toda esta evolución tecnológica.
El diagnóstico y la planificación quirúrgica en la cirugía de pie y tobillo requiere un compromiso con la innovación y pensamos que este es el camino a un futuro con mejores recursos y mejorando la excelencia del manejo de nuestros pacientes.
La impresión en 3D es el camino a la regeneración y al reemplazo de tejidos y órganos.
Figuras
Figura 1. Grave deformidad en pie y tobillo. Se ha realizado la impresión del modelo anatómico completo, para la realización del estudio y la planificación quirúrgica de corrección de la misma. Modelo anatómico óseo y partes blandas sin ensamblar. En azul, peroneo lateral largo y peroneo lateral corto. En verde, tibial posterior, flexor hallucis longus. En naranja, tendón de Aquiles. En amarillo, extensor hallucis longus, extensor digiti longus y tibial anterior. En beis, huesos de la tibia, el peroné, el astrágalo y el calcáneo, junto al resto de las estructuras óseas del pie.
Figura 2. A: imagen anterior digital EN 3D donde se puede observar que el tendón tibial posterior discurre anterior al maléolo tibial; B: imagen anterior del modelo anatómico óseo; C: imagen anterior del modelo anatómico óseo y de partes blandas.
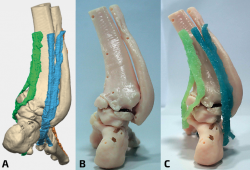
Figura 3. A: imagen posterior digital en 3D; B: imagen posterior del modelo anatómico óseo; C: imagen posterior del modelo anatómico óseo y de partes blandas.
Figura 4. Arrancamiento traumático del tendón del tibial anterior (TTA). Se realizó una impresión en 3D donde se pudo objetivar el arrancamiento osteotendinoso del TTA al nivel de la base del primer metatarsiano; este sufrió una retracción y quedó anclado al retináculo. Podemos ver la relación con la arteria pedia (rojo brillante). A: imagen digital en 3D; B: imagen del modelo anatómico óseo y de partes blandas.
Cita bibliográfica
Autores
Magdalena Edo Llobet
Unidad de Pie y Tobillo. Servicio de Cirugía Ortopédica y Traumatología. Fundacio Althaia - Xarxa Asistencial Universitaria de Manresa. Barcelona
Unidad de Pie y Tobillo. Hospital Universitari Bellvitge. L’Hospitalet de Llobregat, Barcelona
Albert Pérez Fernández
Equipo de Pie y Tobillo. Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario de Bellvitge, Hospitalet de Llobregat, España
Unidad Funcional de Pie Diabético. Hospital Universitario de Bellvitge. Hospitalet de Llobregat. Barcelona
Óscar Pablos González
Equipo de Pie y Tobillo. Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario de Bellvitge. Universidad de Barcelona. L’Hospitalet de Llobregat, Barcelona
Elena Cañas Miguel
Equipo de Pie y Tobillo. Servicio de Cirugía Ortopédica y Traumatología. Hospital Universitario de Bellvitge. Universidad de Barcelona. L’Hospitalet de Llobregat, Barcelona
Unidad Funcional de Pie Diabético. Hospital Universitario de Bellvitge. Hospitalet de Llobregat. Barcelona
Referencias bibliográficas
-
1Ganguli A, Pagan-Diaz GJ, Grant L, Cvetkovic C, Bramlet M, Vozenilek J, et al. 3D printing for preoperative planning and surgical training: a review. Biomed Microdevices. 2018 Aug 4;20(3):65.
-
2Michalski MH, Ross JS. The shape of things to come: 3D printing in medicine. JAMA. 2014;312:2213-4.
-
3Murphy SV, Atala A. 3D bioprinting of tissues and organs. Nat Biotechnol. 2014;32:773-85.
-
4Jammalamadaka U, Tappa K. Recent Advances in Biomaterials for 3D Printing and Tissue Engineering. J Funct Biomater. 2018 Mar 1;9(1):22.
-
5Walton RL, Seelaus R, Robinson BR. Subtotal Nasal Reconstruction Using a Custom 3-Dimensional Porous Polyethylene Construct. Plast Reconstr Surg Glob Open. 2019 Dec 11;7(12):e2568.
-
6Wang X. Advanced Polymers for Three-Dimensional (3D) Organ Bioprinting. Micromachines (Basel). 2019 Nov 25;10(12):814.
-
7Laternser S, Keller H, Leupin O, Rausch M, Graf-Hausner U, Rimann M. A Novel Microplate 3D Bioprinting Platform for the Engineering of Muscle and Tendon Tissues. SLAS Technol. 2018 Dec;23(6):599-613.
-
8Wang J. Development of a Combined 3D Printer and Its Application in Complex Organ Construction. Master’s Thesis. Beijing, China: Tsinghua University; 2014.
-
9Skardal A, Mack D, Kapetanovic E, Atala A, Jackson JD, Yoo J, Soker S. Bioprinted amniotic fluid-derived stem cells accelerate healing of large skin wounds. Stem Cells Transl Med. 2012 Nov;1(11):792-802.
-
10Cui X, Breitenkamp K, Finn MG, Lotz M, D'Lima DD. Direct human cartilage repair using three-dimensional bioprinting technology. Tissue Eng Part A. 2012;18:1304-12.
-
11Akbari S, Zhang YF, Wang D, Ge Q. 4D Printing and Its Biomedical Applications. En: Mohammed Maniruzzaman (ed.). 3D and 4D Printing in Biomedical Applications. Wiley; 2019. pp. 343-372.
-
12Gao F, Xu Z, Liang Q, Liu B, Li H, Wu Y, et al. Direct 3D printing of high strength biohybrid gradient hydrogel scaffolds for efficient repair of osteochondral defect. Adv Funct Material. 2018;28(13):1706644.
-
13Chepelev L, Wake N, Ryan J, Althobaity W, Gupta A, Arribas E, et al.; RSNA Special Interest Group for 3D Printing. Radiological Society of North America (RSNA) 3D printing Special Interest Group (SIG): guidelines for medical 3D printing and appropriateness for clinical scenarios. 3D Print Med. 2018 Nov 21;4(1):11.
-
14Squelch A. 3D printing and medical imaging. J Med Radiat Sci. 2018 Sep;65(3):171-2.
-
15Zamborsky R, Kilian M, Jacko P, Bernadic M, Hudak R. Perspectives of 3D printing technology in orthopaedic surgery. Bratisl Lek Listy. 2019;120(7):498-504.
-
16Bauermeister AJ, Zuriarrain A, Newman MI. Three-Dimensional Printing in Plastic and Reconstructive Surgery: A Systematic Review. Ann Plast Surg. 2016 Nov;77(5):569-76.
-
17O’Reilly MK, Reese S, Herlihy T, Geoghegan T, Cantwell CP, Feeney RN, Jones JF. Fabrication and assessment of 3D printed anatomical models of the lower limb for anatomical teaching and femoral vessel access training in medicine. Anat Sci Educ. 2016 Jan-Feb;9(1):71-9.
-
18Rengier F, Mehndiratta A, von Tengg-Kobligk H, Zechmann CM, Unterhinninghofen R, Kauczor HU, Giesel FL. 3D printing based on imaging data: review of medical applications. Int J Comput Assist Radiol Surg. 2010 Jul;5(4):335-41.
-
19Itagaki MW. Using 3D printed models for planning and guidance during endovascular intervention: a technical advance. Diagn Interv Radiol. 2015;21:338-41.
-
20Park JW, Kang HG, Lim KM, Park DW, Kim JH, Kim HS. Bone tumor resection guide using three-dimensional printing for limb salvage surgery. J Surg Oncol. 2018;1-8.
-
21Giovinco NA, Dunn SP, Dowling L, Smith C, Trowell L, Ruch JA, Armstrong DG. A novel combination of printed 3-dimensional anatomic templates and computer-assisted surgical simulation for virtual preoperative planning in Charcot foot reconstruction J Foot Ankle Surg. 2012;51(3):387-93.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Introducción
- Generalidades, técnicas innovadoras: presente y futuro
- Todo lo que nos puede aportar la tomografía axial computarizada en carga en los problemas del pie y el tobillo
- Todo lo que nos puede aportar la tomografía computarizada dinámica
- Todo lo que nos puede aportar la impresión ósea en 3D
- Todo lo que nos puede aportar la impresión de implantes-guías quirúrgicas en 3D
- Todo lo que nos puede aportar la impresión de tejidos blandos en 3D
Más en PUBMED
Más en Google Scholar


La Monografía de Actualización de la SEMCPT está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.